DIGITAL TRANSFORMATION OF THE HEALTHCARE INDUSTRY
Development of digitalization of the Federal Service for Surveillance in Healthcare in the period 2018–2023
1 — Federal Service for Surveillance in Healthcare, 4, bld. 1, Slavyanskaya Square, Moscow, 109074, Russian Federation.
The article summarizes the results of the last five years of development of informatization of Roszdravnadzor, which significantly changed communications between government bodies, organizations, citizens, and department employees.
Keywords: automated information system, AIS “Roszdravnadzor”, public services of Roszdravnadzor, Unified portal of public services, optimization and automation of public licensing services, departmental information systems, register of mandatory requirements, register of licenses on the Internet portal of Roszdravnadzor, automated system for entering information “Selective control”, introduction of medicines into civil circulation
В 2024 году Федеральная служба по надзору в сфере здравоохранения отмечает свое 20-летие. На протяжении этих двух десятилетий Росздравнадзор уделял особое внимание вопросам информатизации. Первые подсистемы автоматизированной информационной системы (АИС) «Росздравнадзор» были введены в эксплуатацию в уже 2005 году – информационная система начала создаваться фактически с момента образования Росздравнадзора.
Современные тенденции развития вычислительной техники и средств электронных коммуникаций существенно ускорили возможности обмена информацией, ее накопления, обработки и доведения до конечных пользователей. Ранее, при формировании различных информационных систем органами власти, было не предусмотрено взаимодействие между ними. Но за последние годы налаживание взаимодействия между информационными системами государственных органов приобрело ключевое значение. Организация информационного взаимодействия позволила по-новому посмотреть на процесс оказания государственных услуг и создание электронных сервисов для граждан и организаций.
За последние пять лет развития информатизации Росздравнадзора была существенно усовершенствована система коммуникации между государственными органами, организациями, гражданами, а также сотрудниками ведомства.
Одним из важнейших компонентов информационной системы является инфраструктура, в которой она функционирует. В последнее время к информационно-коммуникационной инфраструктуре предъявляются серьезные требования по информационной безопасности. В 2019 году завершилось создание системы защиты информации Росздравнадзора. В полном объеме были оснащены средствами защиты информации и аттестованы территориальные органы Росздравнадзора. С 2019 года центральный аппарат, все территориальные органы Росздравнадзора и лицензирующие органы субъектов Российской Федерации стали взаимодействовать исключительно в защищенной сети, исключающей несанкционированный доступ к информационной системе сторонних пользователей.
Проведенные работы исключили возможность неправомерного доступа, несанкционированного копирования, предоставления и(или) распространения информации и персональных данных, обеспечили санкционированную доступность и целостность информации. В итоге обеспечено предотвращение или снижение величины ущерба, наносимого Росздравнадзору, вследствие реализации угроз безопасности защищаемой информации за счет неправомерного или случайного уничтожения, изменения, блокирования, копирования, распространения защищаемой информации или от иных неправомерных действий.
В частности, принятые меры проявили себя в период с 24 февраля 2022 года. Информационная система справилась с отражением массовых DDOS-атак, работа сотрудников в системе и пользователей интернет-портала Росздравнадзора не были блокированы. Для мониторинга ситуации был разработан дашборд, на котором отражается вся необходимая информация по DDOS-атакам (рис. 1).
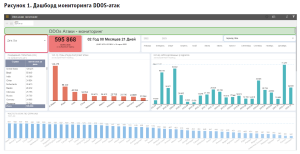
Серьезные задачи перед информационными системами государственных органов были поставлены в 2020 году в связи с начавшейся пандемией новой коронавирусной инфекции. Для принятия Правительством Российской Федерации оперативных решений и контроля за организацией оказания медицинской помощи в изменившихся условиях необходимо было экстренно перестроить информационные системы на сбор новых данных в ежедневном режиме, а также обеспечить предоставление полной информации в оперативном режиме широкому кругу пользователей.
Подготовленная инфраструктура позволила в период пандемии оперативно настроить информационную систему и перевести необходимое количество сотрудников на дистанционную работу с информационной системой в защищенном режиме. Также во время пандемии, ввиду отсутствия физической возможности общения, необходимо было обеспечить оперативную коммуникацию между сотрудниками. Решением стала система видео-конференц-связи (ВКС). Оперативно развернутая ВКС позволила при определенной изоляции активно решать вопросы коммуникации между сотрудниками службы и обеспечить взаимодействие с территориальными органами Росздравнадзора по субъектам Российской Федерации, лицензирующими органами субъектов Российской Федерации, иными федеральными органами исполнительной власти, аппаратом Правительства Российской Федерации и другими организациями. Отдельное место в системе коммуникаций занимает электронная почта и мессенджеры. В связи с импортозамещением и информационной безопасностью в государственных органах данный вопрос встал очень остро.
С начала 2023 года Росздравнадзор принял участие в реализации проекта Минцифры России по внедрению в федеральных органах исполнительной власти автоматизированного рабочего места государственного служащего (ФОИВ АРМ ГС). Эта система в полной мере обеспечивает сотрудников всеми необходимыми средствами коммуникации: электронной почтой и мессенджером, рабочим календарем и иными средствами индивидуальной и коллективной организации работы. С конца 2023 года все сотрудники центрального аппарата Росздравнадзора, территориальных органов и подведомственных учреждений используют АРМ ГС в своей работе.
В отношении развития информационной системы необходимо отметить следующее. В связи с практической невозможностью проведения контрольно-надзорных мероприятий в период пандемии с 2020 года и введением Правительством Российской Федерации моратория на проведение контрольно-надзорных мероприятий1 основными задачами последних лет было смещение акцента на проведение профилактических мероприятий и развитие информационного пространства при оказании разрешительных функций, что нашло отражение в постановлении Правительства Российской Федерации от 12.03.2022 № 353 «Об особенностях разрешительной деятельности в Российской Федерации».
Указом Президента Российской Федерации от 21.07.2020 № 474 «О национальных целях развития Российской Федерации на период до 2030 года» в целях осуществления прорывного развития Российской Федерации, увеличения численности населения страны, повышения уровня жизни граждан, создания комфортных условий для их проживания, а также раскрытия таланта каждого человека, определены национальные цели развития Российской Федерации на период до 2030 года, в том числе цифровая трансформация, и установлены целевые показатели, характеризующие достижение национальных целей к 2030 году, в частности, увеличение доли массовых социально значимых услуг, доступных в электронном виде, до 95%. За период 2021–2023 годов на Едином портале государственных услуг (ЕПГУ) Росздравнадзором в обновленном виде было выведено 19 государственных услуг для оказания в электронном виде (таблица). Далее необходимо остановиться на некоторых из них более детально. С 30 июля 2021 года, в связи с принятием постановления Правительства Российской Федерации № 12792, стартовал проект по проведению на территории Российской Федерации эксперимента по оптимизации и автоматизации процессов разрешительной деятельности, в том числе лицензирования, который задал правила оптимизации оказания государственных услуг в части сокращения сроков их оказания и минимизации предоставления заявителем документов при подаче заявления на предоставление услуги. Постановлением установлены сроки проведения эксперимента с 1 августа 2021 года по 1 июля 2022 года, которые в дальнейшем были продлены, а также ведомства-участники, одним из которых стала Федеральная служба по надзору в сфере здравоохранения.
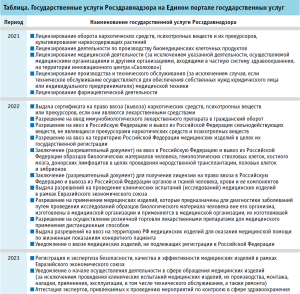
В план реализации проекта по оптимизации одними из первых были включены услуги Росздравнадзора по лицензированию отдельных видов деятельности, как наиболее массовые, востребованные и социально значимые.
В рамках реализации Федерального закона от 27.12.2019 № 478-ФЗ «О внесении изменений в отдельные законодательные акты Российской Федерации в части внедрения реестровой модели предоставления государственных услуг по лицензированию отдельных видов деятельности» постановлением Правительства Российской Федерации от 29.12.2020 № 2343 «Об утверждении Правил формирования и ведения реестра лицензий и типовой формы выписки из реестра лицензий» были установлены правила формирования и ведения лицензирующими органами реестров лицензий на виды деятельности, подлежащие лицензированию.
Также были определены направления оптимизации деятельности лицензирующих органов, в частности, процедур предоставления и внесения изменений в лицензию, в том числе сокращение бумажного документооборота, связанного с оформлением и выдачей лицензий. В ряде случаев упрощена процедура внесения изменений в реестр лицензий, при которой не требуется подача заявления со стороны лицензиата и введены элементы проактивного режима.
Росздравнадзор вошел в пилотный проект, поскольку его информационная система во многом уже была готова к его реализации.
С 1 января 2021 года Росздравнадзором была внедрена реестровая модель по пяти видам лицензируемой деятельности в сфере здравоохранения. Ключевым изменением явилось то, что юридически значимым источником сведений о предоставленных лицензиях юридическим лицам и индивидуальным предпринимателям стал информационный ресурс Росздравнадзора – реестр лицензий в электронном виде. Предоставление лицензии на бумажном носителе было отменено.
По итогам предоставления государственной услуги формируется запись в информационной системе Росздравнадзора и отражается в соответствующем ресурсе на интернет-портале Росздравнадзора (рис. 2). По организации можно самостоятельно сформировать выписку из реестра лицензий по конкретному виду осуществляемой деятельности.
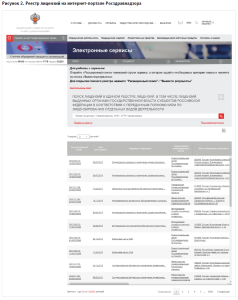
Одним из важных моментов проекта по оптимизации и автоматизации процессов разрешительной деятельности, в том числе лицензирования, был переход на единообразные формы подачи заявлений (на предоставление, внесение изменений в лицензию и досрочное прекращение, получение выписки из реестра лицензий) исключительно в электронном виде с использованием новых форм-концентраторов, размещенных на Едином портале государственных и муниципальных услуг (ЕПГУ) и их интеграции с ведомственными информационными системами. Были полностью сокращены документы, предоставляемые соискателями лицензии и лицензиатами. При подаче через ЕПГУ теперь предоставляется заявление, перечень объектов осуществления деятельности и перечень работ/услуг при оказании соответствующего вида деятельности на конкретном объекте. Все остальные документы анализируются в процессе оценки соответствия непосредственно на лицензируемых объектах, и предварительно информация запрашивается в ЕГИСЗ Минздрава России.
Также были сокращены сроки предоставления лицензии в три раза – с 45 рабочих дней до 15 рабочих дней. И в настоящее время срок оказания услуг планируется уменьшить до пяти рабочих дней.
До 2022 года соискатели лицензии и лицензиаты могли подать заявление как на бумажном носителе, так и в электронном виде через ЕПГУ. В целом в 2021 году в электронном виде было подано всего 50 заявлений. Оптимизация и автоматизация государственных услуг по лицензированию позволили сократить срок.
С 2022 года все процедуры, связанные процессом лицензирования, осуществляются исключительно в электронном виде. Одновременно с этим были приняты положения, которые внесли дополнительные требования к организации межведомственного информационного взаимодействия при осуществлении процессов лицензирования и формирования реестров лицензий. В частности, были утверждены правила формирования и ведения единого реестра учета лицензий (ЕРУЛ). Этот реестр, оператором которого является Минэкономразвития России, создан в целях информационного обеспечения организации и осуществления лицензирования и присвоения номеров лицензиям в едином формате в процессе их предоставления. Реестр формируется на основании информации, предоставляемой лицензирующими органами и является централизованным ресурсом, содержащим подробные сведения о лицензируемых видах деятельности, в том числе: их перечень, информацию о работах (услугах), которые возможно осуществлять в рамках соответствующего вида деятельности, перечень документов, необходимых для оценки соответствия соискателя лицензии (лицензиата) лицензионным требованиям, информацию о видах контроля (надзора), осуществляемых в отношении лицензируемого вида деятельности. Кроме того, в реестр включена информация о лицензирующих органах и их территориальных подразделениях, осуществляющих лицензирование.
Также частью 3 статьи 136 Федерального закона от 11.06.2021 № 170-ФЗ «О внесении изменений в отдельные законодательные акты Российской Федерации в связи с принятием Федерального закона «О государственном контроле (надзоре) и муниципальном контроле в Российской Федерации» была установлена обязанность объединения содержащихся в реестре лицензий записей по юридическим лицам и индивидуальным предпринимателям, имеющим две и более лицензии на осуществление одного и того же лицензируемого вида деятельности, в единую запись о предоставлении лицензии до 1 марта 2022 года.
Эти изменения потребовали внесения существенных изменений в ведомственные информационные системы c целью проведения интеграционных процессов с ЕРУЛ и нормализации данных по лицензиям. Одновременно с работой по развитию информационной системы Росздравнадзор на регулярной основе принимал участие в мероприятиях, проводимых Минэкономразвития России и в составе соответствующих отраслевых групп по внедрению механизма оптимизации и систематизации обязательных требований, регламентирующих деятельность в сфере охраны здоровья граждан («регуляторная гильотина»), в том числе и напрямую касающихся процессов лицензирования.
Росздравнадзором проведена инвентаризация всех действующих обязательных для бизнеса требований с целью их оптимизации и проверки на соответствие современным реалиям. По результатам этой работы часть устаревших норм была отменена. При нынешнем уровне технологического развития устаревшие обязательные требования являются одним из основных препятствий для развития бизнеса, и при этом не достигается ключевая цель этих требований – безопасность жизни и здоровья граждан.
В целях обеспечения открытости и предсказуемости обязательных требований в 2021 году Минэкономразвития России был разработан информационный ресурс, содержащий все обязательные требования – реестр обязательных требований (РОТ). Реестр стал единой платформой, на которой собрана информация обо всех обязательных требованиях к бизнесу, которые проверяются в рамках контроля (надзора) и при выдаче разрешений. Федеральные органы исполнительной власти вносят информацию об обязательных требованиях по видам контроля (надзора) и разрешительной деятельности, вошедшим в план-график формирования реестра. Сведения, которые размещаются на публичном портале, включают информацию о содержании обязательных требований, об актах, которыми они утверждены, ответственности за их нарушение, а также полезную информацию, которая должна помочь предпринимателям обеспечить их соблюдение. Данные из реестра обязательных требований используются в информационной системе Росздравнадзора при формировании отказов в предоставлении или внесении изменений в лицензию в случае нарушения соответствующих обязательных требований.
В настоящее время, в связи с функциональной ограниченностью единых форм подачи заявлений на ЕПГУ по лицензированию, разработанных Минцифрой России, Росздравнадзором проводится работа по переводу этих форм в новый формат с использованием визуального конструктора услуг. Это позволит учесть большинство замечаний, собранных за время работы существующих форм подачи и реализовать клиентоцентричный подход при предоставлении государственных услуг.
Не менее значимой работой по развитию информационной системы Росздравнадзора было создание подсистемы ввода в гражданский оборот лекарственных препаратов и услуги по получению разрешения на ввод в гражданский оборот иммунобиологических лекарственных препаратов и их интеграция с федеральной государственной информационной системой мониторинга движения лекарственных препаратов.
С 29 ноября 2019 года сведения о вводимых в гражданский оборот лекарственных препаратах (за исключением иммунобиологических лекарственных препаратов) представляются в АИС «Росздравнадзор» в электронном виде через интернет-портал Росздравнадзора https://roszdravnadzor.gov.ru/services/vk_ais (рис. 3).
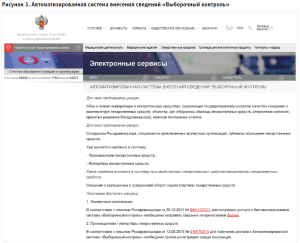
За период с 29 ноября 2019 года по 31 декабря 2023 года в систему «Ввод в гражданский оборот» АИС Росздравнадзора поступили сведения на ввод в гражданский оборот 1 209 672 серий (партий) лекарственных препаратов 46 411 торговых наименований общим количеством 25 320 971 498 упаковок и 140 964 серий фармацевтических субстанций 4897 торговых наименований общим количеством 559 809 563,088 кг.
С 29 ноября 2019 года усилен государственный контроль за качеством иммунобиологических лекарственных препаратов, в первую очередь, вакцин, ввод в гражданский оборот которых осуществляется на основании разрешения Росздравнадзора, выдаваемого на основании заключения государственных лабораторий после прохождения экспертизы качества иммунобиологических лекарственных препаратов и анализа представленных заявителем документов.
Для оказания государственной услуги «Выдача разрешения на ввод в гражданский оборот серии или партии иммунобиологического лекарственного препарата» был разработан и размещен на интернет-портале Росздравнадзора (с ноября 2019 года) соответствующий электронный сервис (рис. 4).

Также в рамках эксперимента по оптимизации и автоматизации процессов разрешительной деятельности, в том числе лицензирования, в 2022 году эта государственная услуга была выведена на ЕПГУ.
Разрешения, выданные Росздравнадзором на ввод в гражданский оборот серии или партии иммунобиологического лекарственного препарата, учитываются в соответствующем реестре информационной системы и публикуются на интернет-портале Росздравнадзора. Это первая государственная услуга Росздравнадзора, оказание которой нормативно закреплено без дублирования на бумажных носителях – исключительно в электронном виде – от подачи заявления до направления разрешения, подписанного электронной подписью и ведения юридически значимого электронного реестра выданных разрешений.
Еще одним элементом интеграции стало информационное взаимодействие с АИС «Росздравнадзор» информационных лабораторных систем ФГБУ «ИМЦЭУАОСМП» Росздравнадзора и ФГБУ «НЦЭСМП» Минздрава России. В рамках этой интеграции обеспечена передача экспертных заключений по иммунобиологическим лекарственным препаратам в Росздравнадзор в электронном виде, что позволило сократить срок взаимодействия и перейти на безбумажный документооборот.
На базе двух вышеупомянутых информационных ресурсов по вводу в гражданский оборот формирующихся на основе Государственного реестра лекарственных средств строится информационная система Росздравнадзора по контролю качества и мониторинга лекарственных средств.
Помимо этого, Росздравнадзором на ежедневной основе осуществляется направление сведений о препаратах, введенных в гражданский оборот в разрезе ЖНВЛП, препаратах, используемых при сердечно-сосудистых и онкологических заболеваниях, в аналитическую витрину Координационного центра Правительства Российской Федерации.
Эти сведения совместно с информацией из федеральной государственной информационной системы мониторинга движения лекарственных препаратов позволяют оценивать ситуацию по дефектуре лекарственных препаратов в онлайн режиме.
С 29 ноября 2019 года законность нахождения серии или партии лекарственного препарата в розничной сети можно проверить через информационный портал Росздравнадзора www.roszdravnadzor.ru. Медицинская и фармацевтическая организация при приемке товара, а также любой покупатель путем обращения к электронному сервису «Ввод лекарственных препаратов в гражданский оборот в Российской Федерации» на информационном портале Росздравнадзора может в том числе по торговому наименованию и номеру серии проверить наличие сведений о данной серии лекарственного препарата в информационной системе и подтвердить его законность нахождения в гражданском обороте. При необходимости эти сведения возможно распечатать в форме выписки.
Завершение работ по интеграции АИС «Росздравнадзор» с федеральной государственной информационной системой мониторинга движения лекарственных препаратов позволило обеспечить контроль за движением лекарственных препаратов от производителя до конечного потребителя и реализовать в автоматизированном режиме блокировку обращения лекарственных препаратов в системе маркировки в случае выявления недоброкачественных лекарственных препаратов.
Базисом информационного взаимодействия систем является единый понятийный аппарат – нормативно-справочная информация.
С 2020 года АИС Росздравнадзора начала интегрироваться с единым цифровым контуром здравоохранения на основе Федерального реестра нормативно-справочной информации (ФРНСИ) Единой государственной информационной системы в сфере здравоохранения (ЕГИСЗ). Росздравнадзор обеспечивает формирование отраслевых справочников ФРНСИ на основе сведений из Единого реестра лицензий, Государственного реестра медицинских изделий и организаций (индивидуальных предпринимателей), осуществляющих производство и изготовление медицинских изделий, номенклатурной классификации медицинских изделий, оцифрованных порядков оказания медицинской помощи населению и других информационных ресурсов. Эти справочники используются при формировании Федерального реестра медицинских организаций (ФРМО) и Федерального реестра медицинских работников (ФРМР).
Росздравнадзор, в свою очередь, использует различные справочники ФРНСИ и сведения из ФРМО и ФРМР для осуществления лицензионных процедур по медицинской деятельности, не запрашивая их у медицинских организаций. В планах работ 2024 года – расширить это взаимодействие на фармацевтические организации, которые с конца 2023 года также подлежат внесению в ФРМО.
В рамках одной статьи сложно охватить все решения, которые были разработаны и введены в эксплуатацию за последние пять лет. Разработаны процессы межведомственного документооборота, подключения к сервисам межведомственного электронного взаимодействия. Отдельными блоками стоят задачи по межгосударственному информационному взаимодействию в рамках Евразийской экономической комиссии (ЕЭК). Росздравнадзор подключен к общим процессам ЕЭК и осуществляет информационное взаимодействие при регистрации медицинских изделий в рамках Евразийского экономического союза, формировании, ведении и использовании единой информационной базы данных мониторинга безопасности, качества и эффективности медицинских изделий, формировании, ведении и использовании единой информационной базы данных лекарственных средств, не соответствующих требованиям по качеству, а также фальсифицированных и (или) контрафактных лекарственных средств, выявленных на территориях государств-членов Евразийского экономического союза, а также в формировании иных информационных ресурсов ЕЭК.
Не меньшее количество электронных сервисов и интеграционных процессов было реализовано в рамках сферы обращения медицинских изделий во исполнение нормативно-правовых актов Правительства Российской Федерации, принятых за последние пять лет. Это сервис для представления производителем (изготовителем) медицинского изделия (его уполномоченным представителем) или лицом, осуществляющим ввоз на территорию Российской Федерации медицинских изделий, сведений в уполномоченный федеральный орган исполнительной власти, сервисы для подачи заявления по государственным услугам «Ввоз не подлежащих регистрации медицинских изделий», «Выдача разрешения для ввоза на территорию Российской Федерации незарегистрированного медицинского изделия для оказания медицинской помощи по жизненным показаниям конкретного пациента», «Выдача разрешения на применение медицинских изделий, которые предназначены для диагностики заболеваний путем проведения исследований образцов биологического материала человека вне его организма, изготовлены в медицинской организации и применяются в медицинской организации, их изготовившей» и ряд других сервисов. Вместе с этим, в 2023 году был подготовлен проект постановления Правительства Российской Федерации «Об утверждении Правил государственной регистрации медицинских изделий и признании утратившими силу некоторых актов Правительства Российской Федерации» в котором отражен новый подход к процедуре регистрации медицинских изделий с возможностью использования современных информационных технологий.
Во исполнение распоряжения Правительства Российской Федерации от 21.10.2023 № 3102-р «Об утверждении концепции создания и функционирования единой цифровой платформы Российской Федерации «ГосТех» и иных нормативно-правовых актов с конца 2022 года Росздравнадзором начат проект по переводу действующей АИС «Росздравнадзор» на платформу «ГосТех». Одними из первых информационных ресурсов, с учетом новых подходов, отраженных в нормативных документах, запланированных для перевода на новую платформу, являются регистрация медицинских изделий по национальной процедуре и процедуре Евразийского экономического союза. В настоящее время завершается опытная эксплуатация разработанных компонентов системы. Мы приобретаем новый опыт и начинаем реализовывать новые подходы на новой информационной платформе, интегрируясь в единое информационное пространство государства.
______________________________________________________________________
1 Постановление Правительства Российской Федерации от 10.03.2022 № 336 «Об особенностях организации и осуществления государственного контроля (надзора), муниципального контроля».
2 Постановление Правительства РФ от 30.07.2021 № 1279 «О проведении на территории Российской Федерации эксперимента по оптимизации и автоматизации процессов разрешительной деятельности, в том числе лицензирования».
