CLINICAL TRIAL
Application of a new intraoperative classification for PAS
1 — Federal State Budgetary Institution “National Medical Research Center of Obstetrics, Gynecology and Perinatology named after Academician V.I. Kulakov” Ministry of Health of Russia, 4, Akademika Oparina st., Moscow, 117997, Russian Federation.
ORCID: https://orcid.org/0000-0002-8159-6373
2 — Federal State Budgetary Institution “National Medical Research Center of Obstetrics, Gynecology and Perinatology named after Academician V.I. Kulakov” Ministry of Health of Russia, 4, Akademika Oparina st., Moscow, 117997, Russian Federation.
ORCID: https://orcid.org/0000-0002-2206-1002
3 — Federal State Budgetary Institution “A.N. Bakulev National Medical Research Center for Cardiovascular Surgery” Ministry of Health of the Russian Federation, 8, bld 7, Leninsky Prospekt, Moscow, 119049, Russian Federation.
ORCID: https://orcid.org/0000-0001-6140-1930
4 — Federal State Budgetary Institution “National Medical Research Center of Obstetrics, Gynecology and Perinatology named after Academician V.I. Kulakov” Ministry of Health of Russia, 4, Akademika Oparina st., Moscow, 117997, Russian Federation.
5 — Federal State Budgetary Institution “National Medical Research Center of Obstetrics, Gynecology and Perinatology named after Academician V.I. Kulakov” Ministry of Health of Russia, 4, Akademika Oparina st., Moscow, 117997, Russian Federation.
6 — Federal State Budgetary Institution “National Medical Research Center of Obstetrics, Gynecology and Perinatology named after Academician V.I. Kulakov” Ministry of Health of Russia, 4, Akademika Oparina st., Moscow, 117997, Russian Federation.
ORCID: https://orcid.org/0000-0003-0025-3182
7 — Federal State Budgetary Institution “National Medical Research Center of Obstetrics, Gynecology and Perinatology named after Academician V.I. Kulakov” Ministry of Health of Russia, 4, Akademika Oparina st., Moscow, 117997, Russian Federation.
ORCID: https://orcid.org/0000-0001-8382-9671
8 — Federal State Budgetary Institution “National Medical Research Center of Obstetrics, Gynecology and Perinatology named after Academician V.I. Kulakov” Ministry of Health of Russia, 4, Akademika Oparina st., Moscow, 117997, Russian Federation.
ORCID: https://orcid.org/0000-0002-4332-430X
Placenta accreta spectrum is a formidable complication of pregnancy, provoking massive bleeding, early and delayed complications, increasing the risks of maternal mortality. Despite this, the successes achieved in solving this problem increasingly allow us to pay attention to organ-preserving techniques that contribute to the preservation of reproductive function. The authors of the article present a study to identify the correlation of placental invasion with the volume of blood loss based on a new intraoperative classification.
Keywords: pregnancy, placenta accretion, metroplasty, organ-preserving operations
Background.
Врастание плаценты – осложнение беременности, связанное с аномальным ее прикреплением, проявляется в неспособности отделения плаценты от стенки матки, что приводит к массивной кровопотере, перинатальным осложнениям, повышает риск материнской смертности. Увеличение распространенности данной акушерской патологии напрямую связано с увеличением частоты операций кесарева сечения [1, 2]. Так, в США в 50-е годы регистрировался один случай врастания на 10 тыс. родов, в 80-е годы – уже четыре случая, а во втором десятилетии 2000-х годов – 18,7 случаев [3]. Наряду с этим, частота случаев врастания плаценты варьирует от 1,7 до 900 на 100 тыс. родов (в среднем 189 на 100 тыс.), что связано с вариабельностью формулировки диагноза и его клинического подтверждения [4].
Для оценки глубины врастания плаценты наиболее часто используют классификацию FIGO (включающую клинические и морфологические критерии). Выделяют несколько степеней врастания плаценты:
I степень (placenta acсreta) – поверхностное прикрепление плаценты к мышечному слою матки;
II степень (placenta increta) – ворсины прорастают мышечный слой, без признаков распространения за пределы серозного слоя матки;
III степень (placenta percreta) – плацента прорастает все слои матки [5, 6].
Все патологические варианты прикрепления плаценты объединены в один термин – placenta accreta spectrum disorders (PAS) [7].
Основными методами, позволяющими диагностировать и планировать хирургическую тактику, являются методы визуальной диагностики – УЗИ и МРТ. Они помогают акушеру-гинекологу избежать массивной кровопотери за счет планирования этапов оперативного вмешательства с учетом всех рисков и подготовки к операции [8, 9].
С 2014 года в ФГБУ «НМИЦАГП им. В.И. Кулакова Минздрава России» прооперировано 520 пациенток с врастанием плаценты в рамках клинических апробаций и оказания высокотехнологичной медицинской помощи.
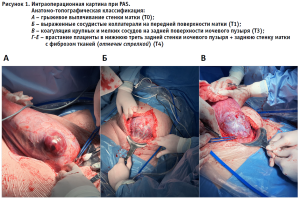
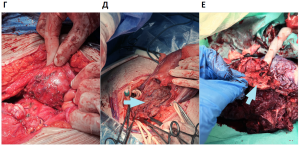
С 2020 года внедрена в практику и активно используется интраоперационная анатомо-топографическая классификация, предложенная Х. Палациусом:
тип 1 – плацента достигает серозной оболочки или выходит за ее пределы с наличием новообразованных сосудов между маткой, плацентой и мочевым пузырем (верхняя задняя часть мочевого пузыря);
тип 2 – плацента достигает серозной оболочки или выходит за ее пределы с инвазией плаценты в параметрий;
тип 3 – плацента прорастает в задненижнюю область мочевого пузыря;
тип 4 – плацента прорастает в задненижнюю область мочевого пузыря с добавлением интенсивного фиброза между мочевым пузырем и маткой [10].
Цель исследования
Выявление корреляции инвазии плаценты с объемом кровопотери на основании новой интраоперационной классификации.
Материалы и методы
Авторами проведен проспективный анализ данных 231 беременной в возрасте от 20 до 40 лет (35,1 ± 4,5) с диагнозом «врастание плаценты». Пациентки находились на обследовании и лечении в ФГБУ «НМИЦАГП им. В.И. Кулакова Минздрава России» в период с 1 января 2020 года по 1 октября 2022 года.
В ходе исследования анализировались следующие показатели:
- возраст матери;
- предшествующие операции на матке;
- особенности течения предыдущих беременностей;
- предшествующие операции кесарева сечения;
- объем кровопотери;
- экстирпация матки;
- перевязка внутренних подвздошных сосудов.
Пациентки были разделены на группы по объему кровопотери и на группы по анатомо-топографической классификации. Были определены типы инвазии плаценты: первая группа (Т1), n = 75; вторая группа (Т2), n = 13; третья группа (Т3), n = 22; четвертая группа (Т4), n = 34. Также была выделена дополнительная группа (Т0), n = 87, к которой отнесено врастание плаценты, не выходящее за пределы матки, без распространения на мочевой пузырь. Общий объем кровопотери в группе Т0 и Т1 был наименьшим и статистически значимым, составил 800 мл (700–1000 мл, р < 0,001), во 2 группе – 1500 мл (750–1500 мл, р < 0,001) и достоверно больше оказался в 3 и 4 группе: 2100 мл (1425–3375мл, р < 0,001) и 1750 мл (1200–3950, р < 0,001) соответственно. Типы инвазии коррелировали со специфическим кровоснабжением каждого из них.
Этап диагностики аномального прикрепления плаценты проводили при помощи УЗИ и МРТ. Всем пациенткам с подозрением на врастание плаценты проводилось оперативное лечение в объеме срединной лапаротомии/поперечно-надлобкового чревосечения, ультразвуковой навигации, донного кесарева сечения/корпорального кесарева сечения в нижнем маточном сегменте, комплексного компрессионного гемостаза, баллонной тампонады матки, метропластики. Во всех случаях было осуществлено патоморфологическое исследование для подтверждения диагноза. Операции проводились в условиях интраоперационной реинфузии аутоэритроцитов на аппарате «Cell-Saver 5».
Статистический анализ проводился с использованием программы StatTech v. 2.8.81. Количественные показатели оценивались на предмет соответствия нормальному распределению с помощью критерия Колмогорова-Смирнова. В случае отсутствия нормального распределения количественные данные описывались с помощью медианы (Me) и нижнего и верхнего квартилей (Q1 – Q3). Сравнение трех и более групп по количественному показателю, распределение которого отличалось от нормального, выполнялось с помощью критерия Краскела-Уоллиса, апостериорные сравнения – с помощью критерия Данна с поправкой Холма. Различия считались статистически значимыми при p < 0,05.
Результаты и обсуждение
Для описания клинико-анамнестических данных все пациентки были разделены на две группы:
- первая группа – с объемом кровопотери до 1500 мл;
- вторая группа – с объемом кровопотери более 1500 мл.
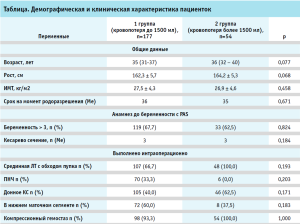
Средний возраст пациенток с подтвержденным диагнозом врастания плаценты составил 35,1 ± 4,5 года в первой группе и 36,5 ± 3,0 года – во второй. Анализ антропометрических показателей не показал различий в группах. Средний рост в первой группе составил 162,3 ± 5,7 см, во второй группе – 164,2 ± 5,3 см (р = 0,1033). ИМТ не имел значимых различий между группами и составил 27,5 ± 4,3 кг/м2 и 26,9 ± 4,6 кг/м2 соответственно (р = 0,458) (таблица).
Исследуемые пациентки были классифицированы по анатомо-топографической классификации: 75 были идентифицированы как тип 1 (Т1), 13 – как тип 2 (Т2), 22 отнесены к третьему типу (Т3) и 34 – к четвертому типу (Т4). Также была выделена дополнительная группа (Т0), n = 87, к которой отнесено врастание плаценты, не выходящее за пределы матки, без распространения на мочевой пузырь (рис.1).
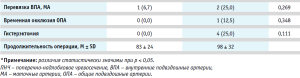
В общей сложности, 76 женщин были прооперированы с использованием модифицированного разреза по Пфанненштилю и 155 – с использованием лапаротомного разреза по средней линии живота с обходом пупка слева. Девять процентов женщин были прооперированы в экстренном порядке (7 % из них – в связи с начавшимся кровотечением и 2% – из-за начала родовой деятельности/излития околоплодных вод). Гистерэктомия была выполнена в четырех случаях (один из них – из-за врастания плаценты в шейку матки и нижнюю треть задней стенки мочевого пузыря, а остальные три – в связи прогрессирующим интраоперационным кровотечением. Органосохраняющие операции были применимы у первого и второго типа инвазии в 100 % случаев, у третьего типа – 21/22 (95,4%) случаев и у четвертого типа – 31/34 (91,1%). В 100 % случаев был применен комплексный компрессионный гемостаз. Родоразрешение пациенток проводили между 35 и 36 неделями беременности при отсутствии показаний и экстренных ситуаций как у матери, так и у плода.
При анализе объема кровопотери со степенью анатомо-топографической инвазии была выявлена статистически значимая разница между средним объемом кровопотери. В группах Т0 и Т1 объем составил 800 мл, в группе Т2 – 900 мл, Т3 – 2100 мл и в группе Т4 – 1750 мл (рис. 2).

Анатомо-топографическая классификация позволила спрогнозировать вероятность кровотечения, послеоперационных осложнений и возможность метропластики и сохранение органа. Знание анатомии малого таза, расположения сосудистых пучков позволяет использовать технику комплексного компрессионного гемостаза. Новая классификация может быть применена даже при недиагностированном врастании плаценты, выявленном интраоперационно, с использованием простых методик во время операции, таких как низведение мочевого пузыря с прицельной коагуляцией сосудов и/или их перевязкой. Применение комплексного компрессионного гемостаза за счет наложения турникетных жгутов максимально близко на основные пути кровоснабжения матки способствует механической окклюзии ее сосудов, что позволяет значительно снизить интраоперационную кровопотерю. В условиях работы турникетных жгутов и снижения кровопотери возможно проведение органосохраняющей операции.
Conclusion.
Беременные с врастанием плаценты представляют группу высокого риска по развитию массивного кровотечения и послеоперационных осложнений. В исследовании была определена взаимосвязь объема кровопотери и типа инвазии плаценты, выявленного интраоперационно. Внедрение новой интраоперационной классификации позволяет вовремя принять оптимальные решения: вызвать хирургов при сложных типах инвазии, определить хирургическую тактику, снизить объем кровопотери, сократить частоту трансфузионной терапии, уменьшить случаи тяжелой послеоперационной анемии и, самое главное, – сохранить репродуктивную функцию женщины.
_______________________________________________________________________
1 Разработчик – ООО «Статтех», Россия.
- Jauniaux E., Alfirevic Z., Bhide A. [et al.] Placenta Praevia and Placenta Accreta: Diagnosis and Management: Green-top Guideline No. 27a. BJOG. 2018: 126(1), e1-e48.
- Jauniaux E., Ayres-de-Campos D. [et al.] FIGO consensus guidelines on placenta accreta spectrum disorders: introduction. International Journal of Gynaecology and Obstetrics. 2018; 40(3):261–264. DOI:10.1002/ijgo.12406.
- Jauniaux E., Collins S., Burton G. Placenta accreta spectrum: pathophysiology and evidence-based anatomy for prenatal ultrasound imaging. American journal of obstetrics and gynecology. 2018; 218(1): 75–87.
- Balayla J., Bondarenko H. Placenta accreta and the risk of adverse maternal and neonatal outcomes. Journal of perinatal medicine. 2013; 41(2): 141–149.
- Jauniaux E., Ayres-de-Campos D., Langhoff-Roos J. [et al.] FIGO Placenta Accreta Diagnosis and Management Expert Consensus Panel. FIGO classification for the clinical diagnosis of placenta accreta spectrum disorders. Int J Gynaecol Obstet. 2019; 146(1): 20–24.
- Pegu B., Thiagaraju C., Nayak D. [et al.] Placenta accreta spectrum-a catastrophic situation in obstetrics. Obstetrics & Gynecology Science. 2021; 64(3): 239–247.
- Donovan, B., Shainker S. Placenta Accreta Spectrum. NeoReviews. 2021; 22(11): e722-e733.
- Uchevatkina P.V., Bychenko V.G., Kulabukhova E.A., Luzhinа I.A., Shmakov R.G. System of a unified approach to interpretation of magnetic resonance tomography in diagnostics of pathological placental attachment “mapi-rads” (morbidly adherent placenta imaging reporting and data system). Russian electronic journal of radiation diagnostics. 2021;11(1):174–190. DOI: 10.21569/2222-7415-2021-11-1-174-190. (In Russ.).
- Bhatia A., Palacio M., Wright A. [et al.] Lower uterine segment scar assessment at 11–14 weeks’ gestation to screen for placenta accreta spectrum in women with prior Cesarean delivery. Ultrasound in Obstetrics & Gynecology. 2022; 59(1): 40–48.
- Palacios-Jaraquemada J.M. Placenta adhesive disorders. 1st ed. Berlin: De Gruyter Editors; 2012. 171 p.
