DRUG PROVISION
Monitoring of compounding pharmacies in the Russian Federation for 2023–2024 (part 2)
1 — The State Duma of the Federal Assembly of the Russian Federation, 1, Okhotny Ryad str., Moscow, 103265, Russian Federation.
2 — The State Duma of the Federal Assembly of the Russian Federation, 1, Okhotny Ryad str., Moscow, 103265, Russian Federation.
3 — The State Duma of the Federal Assembly of the Russian Federation, 1, Okhotny Ryad str., Moscow, 103265, Russian Federation.; Federal State Budgetary Educational Institution of Higher Education “A.I. Yevdokimov Moscow State University of Medicine and Dentistry” of the Ministry of Healthcare of the Russion Federation, 20, Delegatskaya str., building 1, Moscow, 127473, Russian Federation.
ORCID: https://orcid.org/0000-0003-2397-6578
4 — The State Duma of the Federal Assembly of the Russian Federation, 1, Okhotny Ryad str., Moscow, 103265, Russian Federation.
5 — The State Duma of the Federal Assembly of the Russian Federation, 1, Okhotny Ryad str., Moscow, 103265, Russian Federation.
6 — Federal Service for Surveillance in Healthcare, 4, bld. 1, Slavyanskaya Square, Moscow, 109074, Russian Federation.
7 — Federal State Funded Educational Institution of Higher Education «Saint Petersburg State Chemical and Pharmaceutical University» of the Ministry of Health of the Russian Federation, 14, lit. A, Prof. Popov str., Saint Petersburg, 197022, Russian Federation.
ORCID: https://orcid.org/0000-0003-4609-0155
8 — Federal State Funded Educational Institution of Higher Education «Saint Petersburg State Chemical and Pharmaceutical University» of the Ministry of Health of the Russian Federation, 14, lit. A, Prof. Popov str., Saint Petersburg, 197022, Russian Federation.
ORCID: https://orcid.org/0000-0001-6297-9304
9 — Federal State Funded Educational Institution of Higher Education «Saint Petersburg State Chemical and Pharmaceutical University» of the Ministry of Health of the Russian Federation, 14, lit. A, Prof. Popov str., Saint Petersburg, 197022, Russian Federation.
ORCID: https://orcid.org/0000-0001-5061-0729
10 — Federal State Funded Educational Institution of Higher Education «Saint Petersburg State Chemical and Pharmaceutical University» of the Ministry of Health of the Russian Federation, 14, lit. A, Prof. Popov str., Saint Petersburg, 197022, Russian Federation.
ORCID: https://orcid.org/0000-0003-0256-6692
11 — Federal State Funded Educational Institution of Higher Education «Saint Petersburg State Chemical and Pharmaceutical University» of the Ministry of Health of the Russian Federation, 14, lit. A, Prof. Popov str., Saint Petersburg, 197022, Russian Federation.
ORCID: https://orcid.org/0000-0002-2805-3089
12 — Federal State Funded Educational Institution of Higher Education «Saint Petersburg State Chemical and Pharmaceutical University» of the Ministry of Health of the Russian Federation, 14, lit. A, Prof. Popov str., Saint Petersburg, 197022, Russian Federation.
ORCID: https://orcid.org/0000-0002-5483-6626
This study presents for the first time the expanded results of an independent and maximally comprehensive audit (monitoring) of medical and pharmacy organizations operating in Russia that have a license for pharmaceutical activities with the right to compounding drugs. The study is carried out in two interconnected parts. The second part presents detailed results of the analysis of a survey of existing compounding pharmacies and materials characterizing their current infrastructure, technological and personnel parameters – consolidated information. The staff composition, the volumes of demand for services (works) on the production of medicines and in-pharmacy packaging of registered medicines have been established, the areas and premises involved in their production have been determined, the level of demand for pharmaceutical substances has been studied, including the nomenclature and volumes of unmet needs for “small” packaging have been determined, the nomenclature of production from registered medicinal products has been analyzed, the “average statistical portraits” of compounding pharmacies have been updated, and the best practices of the subjects of Russia in organizing pharmaceutical business in the field of pharmacy production have been considered.
Keywords: methods of personalized medicine, health-saving technologies, high-tech healthcare, compounding pharmacies, extemporaneous drugs, prescription and compounding departments of a pharmacy organization, compounding and dispensing of medicinal products, stock preparation, in-pharmacy packaging of registered medicinal products
Background.
Данная работа является второй частью и продолжением ранее представленных расширенных результатов аудита (мониторинга) действующих в России медицинских и аптечных организаций (далее соответственно – МО, АО), имеющих лицензию на фармацевтическую деятельность с правом изготовления лекарственных препаратов для медицинского применения (далее – ЛП) за 2023–2024 годы. Анализ включает результаты обработанных 353 анкет (полностью и частично заполненных в ходе Мониторинга)1, а также обзор лучших практик субъектов России по организации фармацевтического дела в сфере аптечного изготовления ЛП (далее – Мониторинг) [1]. В связи с тем, что период проведения исследования не позволял охватить полный 2024 год, то запрос данных осуществлялся за 2023 год.
В первой части исследования [1] подробно описана методология работы, количественные и качественные показатели функционирующих МО и АО, имеющих лицензию на фармацевтическую деятельность с правом изготовления и отпуска ЛП (далее – производственные аптеки, ПА), их территориальное распределение, организационно-правовые формы. Определены основные количественные и качественные показатели по видам и подвидам производственных аптек, в том числе обладающих правом на изготовление наркотических средств и психотропных веществ.
Вторая часть исследования сосредоточена на детальном анализе ключевых аспектов функционирующих ПА, включая описание выборки, по которой установлена дополнительная информация, в том числе классификация по видам и подвидам по перечню выполняемых работ, оказываемых услуг, составляющих фармацевтическую деятельность, а также:
- уточнение кадрового состава;
- установление объемов и структуры спроса на услуги (работы) по изготовлению ЛП и внутриаптечной фасовке зарегистрированных ЛП;
- определение характеристик площадей, помещений и оснащения, задействованных при изготовлении ЛП;
- анализ уровня спроса и потребностей в фармацевтических субстанциях (далее – ФС), в том числе по номенклатуре и объемам неудовлетворенных потребностей в «малых» фасовках;
- изучение номенклатуры изготовления из зарегистрированных ЛП;
- структурирование «портретов» общественной и госпитальной ПА;
- констатацию региональных особенностей и выполнение обзора лучших практик субъектов России по организации фармацевтического дела в сфере аптечного изготовления;
- декларирование перспектив развития нормативного правового регулирования.
Представленные материалы базируются на результатах, охвативших все ПА из различных регионов страны, которые позволили выявить новые тенденции, подтвердить актуальные задачи и существующие проблематики, а также выделить перспективные проекты развития данного сектора здравоохранения.
Ключевые выводы представлены 17 декабря 2024 г. на пятом заседании Рабочей группы по подготовке к реализации норм Федерального закона от 05.12.2022 № 502-ФЗ «О внесении изменений в статью 56 Федерального закона «Об обращении лекарственных средств» при Комитете Государственной Думы по охране здоровья (далее – Рабочая группа).
Результаты и обсуждение Виды и подвиды производственных аптек по перечню выполняемых работ, оказываемых услуг, составляющих фармацевтическую деятельность. Распределение ПА по категориям: ПА, осуществляющие розничную торговлю (отпуск) ЛП населению (далее – розничные ПА) и ПА, действующие как структурные подразделения медицинских организаций (далее – больничные ПА) по количеству предоставленных анкет составили 171 и 182 адресов соответственно (рис. 1).
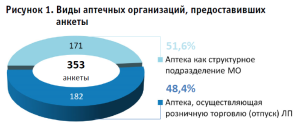
Наибольшее количество ответов от больничных ПА получены из следующих регионов: г. Санкт-Петербург, Нижегородская и Ленинградская область (доли от действующих больничных ПА 10,1%, 5,4% и 3,9% соответственно). Наибольшее количество представленных ответов от общественных ПА получены от аптек, действующих в г. Москве, Республике Татарстан и Республике Башкортостан (доли от действующих больничных ПА 5,6%, 4,0% и 2,6% соответственно).
Распределение перечня оказываемых (выполняемых) услуг (работ), составляющих фармацевтическую деятельность с правом изготовления и отпуска ЛП, показывает, что 204 (58%) ПА имело право осуществлять изготовление асептических ЛП (рис. 2).
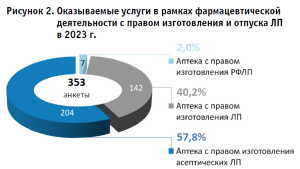
Количество сотрудников производственных аптек, задействованных при изготовлении лекарственных препаратов. Затрагивая вопрос структуры фармацевтических работников и исходя из полученных ответов респондентов установлено, что в 353 ПА при изготовлении ЛП задействовано не менее 3001 штатных единиц в штатных расписаниях (табл. 1). Отдельно выделим, что пять из семи АО, имеющих право на изготовление радиофармацевтических ЛП (далее – РФЛП), предоставили информацию о наличии шести штатных единиц провизоров-аналитиков и пяти штатных единиц провизоров-технологов. Как и в предшествующем исследовании [2], в настоящем у 157 из 353 ПА (44,5%) наблюдается дефицит и отмечается недостаточная укомплектованность провизорами-аналитиками и (или) провизорами-технологами (рис. 3). Всего специалистов с данными должностями задействовано не менее 634 единиц в штатных расписаниях (21,1% от общего числа фармацевтических работников). Наибольшая потребность и недостаточная укомплектованность наблюдается по должностям «провизор-технолог», которая указана 141 респондентом.

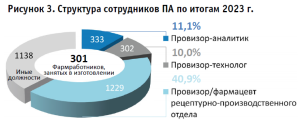
В таблице 2 представлено распределение дефицита кадров по федеральным округам. Высокая потребность наблюдается в каждом округе и наиболее ощутима в провизорах-технологах в ЮФО (57,9%) и ПФО (57,5%). Дефицит или недостаточная укомплектованность необходимыми специалистами в штате организаций неоднократно заявлялась заведующими АО, а также указывалось, что приостановка деятельности связанна именно с данным фактором. Основной причиной выступает «переток кадров» в промышленный сектор, что вызвано неконкурентным уровнем заработных плат и усугублением взаимосвязанных причин по снижению престижа профессии фармацевта в аптечном звене. Респондентами указывались случаи, когда фармацевтические работники осваивали программы переподготовки и повышения квалификации, предназначенные для сотрудников фармацевтических предприятий по инженерно-техническим направлениям, в области химии, технологии, контроля и обеспечения качества, а также организации производства лекарственных средств (далее – ЛС) с учетом правил надлежащей производственной практики (GMP).
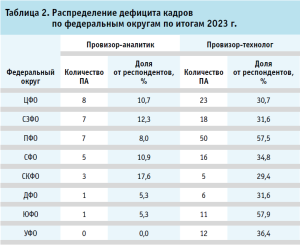
Анализ спроса и объемов изготовленных лекарственных препаратов. На рисунке 4 представлены результаты рассмотрения 353 полученных анкет (полностью и частично заполненных в ходе Мониторинга) [1] в части объемов изготовленных единиц. По итогам 2023 года установлено, что общее количество составило не менее 23,7 млн ед., из них:
- не менее 6,7 млн ед. отпущено по рецептам на ЛП, в том числе не менее 0,7 млн ед. расфасованных ФС, но отпущенных в виде изготовленных ЛП (однокомпонентные по составу);
- не менее 17,0 млн ед. отпущено по требованиям МО, где расфасованные ФС, отпускаемые в виде изготовленных ЛП (однокомпонентные по составу), составляли не менее 1,9 млн ед., а также расфасованные в условиях АО зарегистрированные ЛП (подвергнутые нарушению целостности первичной упаковки) – не менее 0,4 млн ед.
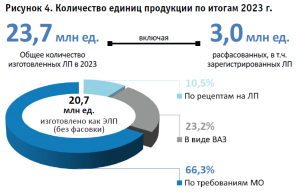
В структуре данных можно выделить, что по наиболее часто поступающим составам (рецептурам) изготовлено в форме внутриаптечной заготовки (ВАЗ) не менее 328 551 серий и отпущено не менее 5,9 млн единиц ЛПАИ как по рецептам на ЛП, так и по требованиям МО.
Определение объемов площадей и помещений, задействованных при изготовлении лекарственных препаратов. Рассматривая 353 полученные анкеты (полностью и частично заполненные в ходе Мониторинга) в части наличия производственных помещений респондентов установлено, что общая площадь производственных помещений составляет 59 243 м2, из которых 12 409 м2 приходится на «Ассистентскую» и 8044 м2 на «Асептический бокс». В случае экстраполяции результатов Мониторинга на фактическое количество общих площадей действующих ПА на сведения Единого реестра лицензий Росздравнадзора по состоянию на 10 июля 2024 года (далее – Реестр РЗН)2, общее количество площадей действующих ПА, которые нуждаются в модернизации материально-технической базы, в целом может достигать порядка 118 445 м2, из которых 24 853 м2 придется на «Ассистентскую» и 16 089 м2 – на «Асептический бокс», без учета прочих помещений. Отметим, что ранее представленные данные получились несколько ниже данных аналогичной методики, проведенной в 2023 году [2], и уточнены в настоящей работе. Примененная в работах методика позволяет осуществлять необходимые расчеты объемов затрат при реализации «типовых проектов» (только участки изготовления «традиционных ЛП») по реконструкции (модернизации) отдельно взятой или ряда действующих на территории ПА, а также предоставляет возможности концептуального определения затрат в случае необходимости организации работы с высокоопасными и токсичными веществами (участки изготовления «традиционных ЛП» с участками изготовления ЛП из высокоактивных и токсичных веществ или только участки изготовления ЛП из высокоактивных и токсичных веществ).
Исследование номенклатуры и объемов спроса на фармацевтические субстанции, а также неудовлетворенной потребности в «малых» фасовках. По итогам Мониторинга впервые выявлена динамика фактической потребности ПА России в ФС (рис. 5). Результаты представлены в консолидированном виде для аптек, изготавливающих аллопатические и РФЛП, в том числе в разрезе анатомо-терапевтическо-химической классификации (далее – АТХ) (табл. 3). Данные о потребности за 2023 год в ФС предоставили 309 респондентов, в составе которых установлена информация о 191 международном непатентованном наименовании (далее – МНН) и 44 наименованиях вспомогательных веществ.
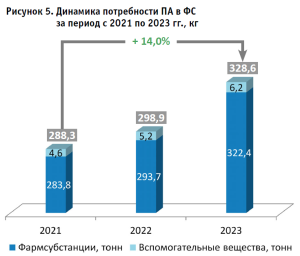
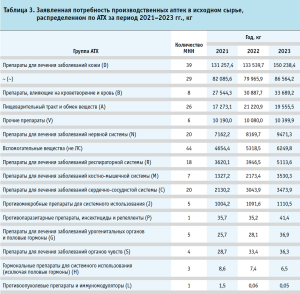
Часть доли в структуре роста спроса на ФС в 2023 году мы связываем с тем, что 12,3% респондентов за 2021 г. и 9,4% за 2022 г. не включили сведения предшествующих периодов (за 2021 год консолидированы данные от 271 респондента, за 2022 год – от 280).
В соответствии с распределением по АТХ потребности исходного сырья, используемого для изготовления ЛП, рейтинг с наибольшим и стабильным спросом как в количественном, так и в натуральном выражении возглавила группа (D) Препараты для лечения заболеваний кожи, – ее доля составляет 46,5%. Основным каналом спроса на данные ФС являются больничные аптеки – 56,9% в натуральном выражении.
Как показывают результаты исследования, наибольшую потребность ПА испытывают в МНН водорода пероксид, который в том числе используется для собственных нужд ПА в качестве дезинфицирующего средства. По итогам 2023 года, потребность МНН водорода пероксид составила 127 733 кг, что больше на 11,3% потребностей 2022 года. При этом доля потребления МНН водорода пероксид больничными ПА по итогам 2023 года составила 59,5%. Вторую строку занимает МНН декстроза, потребность в которой по итогам 2023 года составила 33 488 кг, показав прирост на 9,2%. Третью строку занимает МНН вазелин, потребность в котором по итогам 2023 года составила 23 657 кг, показав прирост на 9,4%.
Распределение потребности в зависимости от массы ФС представлена в таблице 4. По итогам 2023 года, общая потребность ПА в ФС, необходимых в объеме менее 1 кг, определена для 35 МНН. Такие ФС в основном востребованы для изготовления ЛП, предназначенных для лечения сердечно-сосудистых заболеваний и заболеваний нервной системы (например, дигоксин, карведилол, азатиоприн).
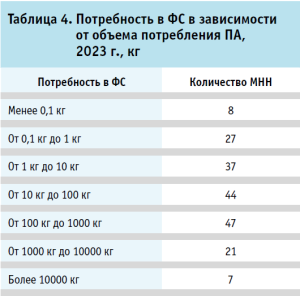
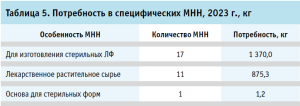
В таблице 5 представлена потребность за 2023 год в ФС, имеющих следующие особенности: 17 МНН используются для изготовления стерильных лекарственных форм, 11 МНН представлены в виде лекарственного растительного сырья и одно МНН используется в качестве основы для стерильных лекарственных форм (глазная мазь).
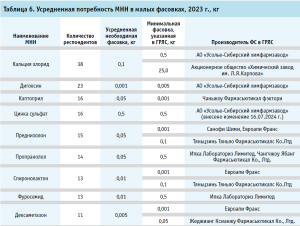
Неудовлетворенная потребность в малых фасовках ФС обозначена 107 респондентами в количестве 154 МНН. Потребность в фасовках ФС до 0,01 кг указана для 35 МНН, от 0,01 до 0,1 кг – 51 МНН, от 0,1 до 1 кг – 55 МНН, и более 1 кг – 13 МНН. В таблице 6 указаны средние значения малых фасовок для 24 МНН, которые отметили более пяти респондентов. Усредненную фасовку в натуральном выражении рассчитывали по медианному значению. Наиболее частое указание было по МНН кальция хлорид, дигоксин, каптоприл, необходимость наличия малых фасовок которых отметило 38, 23, 16 респондентов соответственно (табл. 6).
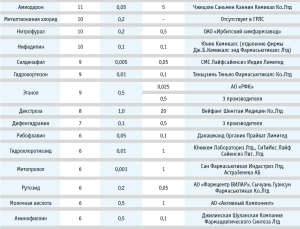
Следует отметить, что в соответствии с данными государственного реестра лекарственных средств (далее – ГРЛС) у подавляющей части производителей ФС заявлен широкий диапазон фасовок ФС, однако фактически данные фасовки отсутствуют на рынке как у непосредственных российских производителей, так и у поставщиков. Подтверждением этому служат сведения о наиболее частых ответах респондентов в отношении причин неудовлетворенного спроса, среди которых:
- отсутствие малых фасовок у производителей/поставщиков (100% респондентов);
- отсутствие включения в ГРЛС малых фасовок ФС для реализации (20,6% респондентов);
- наличие в реестре ГРЛС зарегистрированной ФС, не дающее гарантии на приобретение минимальной фасовки (15,9% респондентов).
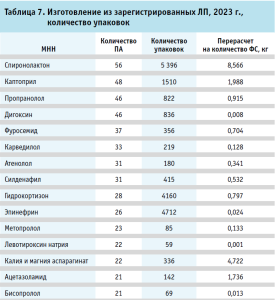
Изучение номенклатуры и объемов изготовления лекарственных препаратов из зарегистрированных лекарственных препаратов. 43 из 193 респондентов ответили, что при изготовлении не используют зарегистрированные ЛП. В таблице 7 представлены МНН, которые выделили более 10 респондентов. Из 24 МНН, представленных в таблице 6, 7 наименований не изготавливаются из зарегистрированных ЛП: цинка сульфат, метилтиониния хлорид, нитрофурал, декстроза, рибофлавин, рутозид и молочная кислота.
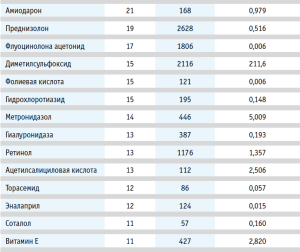
Таким образом, по вышеуказанным МНН существует дополнительная потребность в ФС, которую невозможно было официально представлять с 2010 года. Эта потребность стала объективна с момента вступления в силу положений, принятых Федеральным законом от 05.12.2022 № 502-ФЗ3.
Портреты общественной и госпитальной производственной аптеки.
В связи с множественным увеличением выборки респондентов в 2024 году, стало возможным наиболее точно составить портрет «среднестатистической» общественной и больничной ПА. Их основные характеристики представлены на рисунках 6 и 7 соответственно.
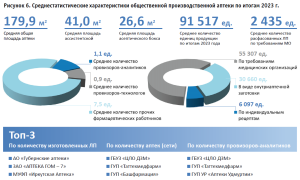
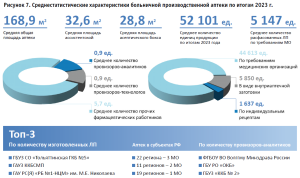
Необходимо отметить, что по средней общей площади больничные ПА меньше общественных ПА на 6,1%. Сравнение распределения структуры фармацевтических работников, занятых при изготовлении ЛП, также показало свое отличие – в структуре больничных ПА на 31,8% больше штатных единиц из категории «Прочие работники, в т.ч. сотрудники младшего обслуживающего персонала». В отношении распределения спроса на изготовление ЛП в больничных ПА средняя доля изготовленных ЛП по требованиям МО, в том числе для собственных нужд, ниже на 19,3% среднестатистической общественной аптеки, при этом средняя доля изготовленных ЛП по рецептам на ЛП ниже практически в пять раз.
Краткий обзор инициатив фармацевтических работников и лучших практик производственных аптек России
Республика Татарстан. В соответствии с данными Реестра РЗН, на территории Республики Татарстан правом на изготовление ЛП обладали пять юридических лиц, которые осуществляли свою деятельность по 21 адресам, из которых 17 относятся к ПА амбулаторного типа – оказывающим фармацевтическую помощь гражданам при обращении в аптечную организацию и отпуске товаров аптечного ассортимента, безрецептурных, рецептурных ЛП, включая изготовление и отпуск ЛП по рецептам. Результаты Мониторинга показывают, что по 17 адресам в Республике Татарстан сохранена фармацевтическая деятельность с правом изготовления ЛП в структуре ГУП «Медицинская техника и фармация Татарстана» (далее – ГУП «Таттехмедфарм»), которое получило статус единственного поставщика в 2018 году4. ГУП «Таттехмедфарм» осуществляет полномочия по обеспечению уполномоченного органа исполнительной власти Республики Татарстан в сфере охраны здоровья и подведомственных ему организаций в отношении ЛС. Инфраструктура изготовления ЛП на базе ГУП «Таттехмедфарм» вносит существенный вклад в доступность ЛП для сельского населения, в том числе экстемпоральных. В частности, на базе ГУП «Таттехмедфарм» модернизирована производственная аптека площадью 1120 м2. Аптека оснащена современным оборудованием, которое позволило повысить уровень качества, безопасности и эффективности изготавливаемых ЛП: «Система получения воды очищенной и воды для инъекций с двухступенчатым обратным осмосом, промежуточной и финишной стерилизующей апирогенной микрофильтрацией» отечественного производства с объемом дистилляции до 100 литров в час; «Линия розлива для стерильных лекарственных форм с системой фильтрования» отечественного производства с объемом розлива и укупорки до 1000 флаконов в час; «Cтерилизатор паровой прямоугольный, двухдверный с автоматическим управлением в комплекте с тележками и загрузочным контейнером» отечественного производства с рабочим объемом – 400 литров и возможностью настройки двух режимов стерилизации – 120 град и 132 град. В целях выполнения мероприятий по контролю и обеспечению качества аптека имеет спектрофотометр отечественного производства; титровальную автоматическую установку; автоматический цифровой рефрактометр.
Нижегородская область. В связи с отсутствием зарегистрированных ЛФ противотуберкулезных ЛП для детей, ПА играют ключевую роль. В условиях детского отделения ГБУЗ НО «Нижегородский областной клинический центр фтизиопульмонологии» больничная аптека ежедневно изготавливает индивидуальные дозировки по 12 МНН в форме порошков и свечей, что позволяет наиболее точно корригировать дозы с учетом массы тела пациента, обеспечивать безопасность и удобство применения у детей всех возрастов, включая пациентов с трудностями при проглатывании или непереносимостью пероральных лекарственных форм. Также в субъекте действует государственная (региональная) фармация – ГП НО «НОФ». В структуре предприятия функционирует 251 аптека, включая 4 ПА. За 2023 год предприятием было изготовлено 275 рецептур в объеме 178 264 единиц экстемпоральных ЛП, из них 39 981 было изготовлено по рецептам на ЛП и 138 285 по требованиям МО. ГП НО «НОФ» планирует не только нарастить количество изготавливаемых рецептур до 335 и довести объем изготовления ЛП до 240 000 единиц в год, но и ведет активную работу по модернизации существующей инфраструктуры. В ближайшее время планируется строительство современной ПА. Реализация проекта направлена как на повышение уровня и обеспечение физического доступа пациентов к необходимым дозировкам, лекарственным формам и объемам фасовки в рамках курсовых назначений ЛП, так и оказание прямого, положительного фармако-экономического эффекта на бюджеты всех уровней, в том числе при исполнении полномочий исполнительных органов субъекта РФ при обращении ЛС в части реализации региональных программ обеспечения населения ЛП за счет организации внутриаптечной фасовки зарегистрированных ЛП из «балк» форм в индивидуальную.
Краснодарский край. Производственная аптека ГБУЗ «Краевая клиническая больница № 2» Минздрава Краснодарского края реализует проект по оптимизации системы лекарственного обеспечения в рамках программы «Приоритет-2030» при участии АНО «Региональный центр компетенций» и Кубанского государственного медицинского университета. Внедрение риск-ориентированного подхода к формированию формулярных перечней позволило сократить затраты на обеспечение ЛП на 46%. Проект признан лучшей практикой региона. Примером значимости ПА стало изготовление суппозиториев с бензоатом натрия для новорожденного с редким наследственным заболеванием обмена веществ, когда зарегистрированные аналоги отсутствовали. Также в субъекте планируется открытие современной ПА площадью около 3 тыс. м2 в образовательном центре «Сириус», что по актуальным данным запланировано на март 2026 года. Ее работа будет сосредоточена на ЛП, предназначенных для лечения редких (орфанных) заболеваний. Объем инвестиций оценивается в 1 млрд рублей5.
Москва. Государственное бюджетное учреждение здравоохранения города Москвы «Центр лекарственного обеспечения Департамента здравоохранения города Москвы» (ГБУЗ «ЦЛО ДЗМ») имеет широчайший опыт в повышении качества функционирования системы лекарственного обеспечения посредством обеспечения доступности экстемпоральных ЛП. Особо значимым является опыт в обеспечении пациентов с редкими (орфанными) заболеваниями, а также обеспечении изготавливаемыми ЛП льготных категорий граждан – за 2023 год производственными аптеками ГБУЗ «ЦЛО ДЗМ» обеспечено экстемпоральных ЛП в рамках 569 рецептов.
Алтайский край. Для привлечения интереса подрастающего поколения к профессии провизора и фармацевта на базе аптеки МУП «Фармация» Заринского района, расположенной в г. Заринск Алтайского края создан Музей аптечного дела с площадкой для профориентации молодежи (школьники, студенты городского и сельского населения), где фармацевтические работники осуществляют просветительскую деятельность в сфере аптечного изготовления. Как и во многих ПА России, в МУП «Фармация» Заринского района за преемственность практических знаний и навыков отвечают фармацевтические работники с опытом работы более 40 лет. Аптека участвует в системе льготного отпуска ЛП системе льготного лекарственного обеспечения и отпуска ЛП.
Приморский край. На базе Тихоокеанского государственного медицинского университета во Владивостоке в рамках проекта «Приоритет-2030» создана учебно-производственная аптека, организованы самые современные условия для развития технологий – дополнительно созданы помещения под лабораторию разработки аптечных технологий, методик качества и проведения испытаний.
Conclusion.
В совокупности двух представленных частей исследования, полученные результаты Мониторинга свидетельствуют о максимально полном аудите действующих в России МО и АО, имеющих лицензию на фармацевтическую деятельность с правом изготовления ЛП. В составе ключевых и уникальных информационно-аналитических выводов Мониторинга:
- Основные количественные характеристики:
- впервые установлено точное количество действующих ПА – не менее 683, функционирующих в структуре 505 ЮЛ (по состоянию на октябрь 2024 года), при этом в Реестре РЗН содержится информация о количестве действующих лицензий с соответствующим правом для 1339 аптек – то есть каждая вторая аптека по факту не осуществляет деятельность по изготовлению ЛП;
- к основным причинам сокращения количества ПА в 2024 году на 2,8% относятся: низкий уровень технологической готовности инфраструктуры и устаревшее инженерное, технологическое, аналитическое оснащение;
- ПА действуют только в 82 субъектах (без учета новых регионов), 41,3% аптек располагаются в 10 субъектах России, в 27 субъектах страны действуют три и менее аптеки, в 11 субъектах только одна аптека;
- 275 из не менее 683 действующих ПА функционируют в составе организаций с государственными формами собственности – то есть 40,3%; в случае, если рассматривать только общественные ПА, то аналогичный показатель составит 64,7%;
- на ТОП-5 государственных (региональных) фармаций приходится 107 действующих ПА;
- установлен острый дефицит провизоров-аналитиков и провизоров-технологов: в 44,5% опрошенных аптек отмечен недостаток данных специалистов.
- Основные результаты анализа 353 полученных и обработанных анкет (полностью и частично заполненные в ходе мониторинга) установили, что по итогам 2023 года:
- текущие занимаемые площади составляют не менее 59 243 м2, из которых 12 409 м2 приходится на «ассистентские» и 8044 м2 на «асептические боксы», которые требуют модернизации (реконструкции);
- общее количество единиц изготовления составило не менее 23,7 млн, из них 3,0 млн ед. расфасованных ЛС, но отпускаемых в виде изготовленных ЛП (однокомпонентные по составу), в т.ч. зарегистрированных ЛП – это свидетельствует о том, что ПА являются основными субъектами персонификации лекарственной терапии;
- 66,3% ЛП аптечного изготовления отпущено по требованиям МО;
- 309 аптек представили сведения о востребованности 191 МНН и 44 наименований вспомогательных веществ;
- наибольшим и стабильным спросом как в количественном, так и в натуральном выражении возглавила группа (D) ЛП для лечения заболеваний кожи, ее доля составляет 46,5%;
- неудовлетворенная потребность в малых фасовках ФС наблюдается по 154 МНН, из них на фасовки менее 0,1 кг приходится по 86 МНН.
- Для ПА, прежде всего расположенных в сельской местности, требуется обеспечить доступ к действующим региональным мерам государственной поддержки социально значимых видов деятельности в части предоставления налоговых и прочих льгот – уже внесены изменения в коды ОКВЭД2, требуется продолжить работу по совершенствованию кодов ОКПД2 и в дальнейшем анализировать практику применения имеющихся и новых мер государственной поддержки.
- В распоряжении имеется информация о существенно устаревшем инженерном, технологическом, аналитическом оснащении ПА. В частности, средний «возраст» технологического оборудования ПА одного из субъектов РФ составляет от 15,7 лет. В ПА преобладает ручной труд, не внедрены и отсутствуют финансовые возможности для применения полуавтоматических методов, которые позволяли бы добиться существенной эффективности, в том числе с точки зрения валидиации и квалификации оборудования – менее 13% ПА оснащены соответствующими установками для дозированной подачи лекарственных форм, например, во флаконы. Практически отсутствуют ПА, оснащенные трубопроводом для подачи воды очищенной и воды стерильной к рабочим местам. Отсутствие современного оборудования отрицательно сказывается на возможностях повышения производительности труда, в связи с чем необходимо внедрить и расширить комплекс мер государственной поддержки, который включал бы финансовые и нефинансовые мероприятия, в том числе ориентированные на создание, модернизацию (реконструкцию) инфраструктуры здравоохранения, разработку и освоение новых технологий изготовления ЛП, методик контроля качества, включая экспресс-методы анализа, проведение испытаний стабильности для установления сроков годности, рекомендуемых требований к надлежащим условиям хранения, выбора необходимых указаний по маркировке, надлежащих упаковочных материалов, систем упаковки и (или) укупорки, а также обоснования использования необходимой концентрации антимикробных консервантов и других вспомогательных веществ.
- По результатам исследования сделан вывод о необходимости дальнейшего решения следующих задач по:
- разработке и внедрению регулярного (цифрового) механизма и инструментария для сбора, обработки, анализа и хранения отчетности аптек;
- качественному повышению уровня доступности и обеспеченности аптек исходным сырьем и ФС, в том числе в «малых» фасовках;
- усовершенствованию действующего законодательства, прежде всего, в части выравнивания уровней доступности экстемпоральных и зарегистрированных ЛП в структуре системы здравоохранения, в том числе в рамках программ льготного лекарственного обеспечения и программы государственных гарантий;
- уточнению параметров национального проекта «Продолжительная и активная жизнь» и (или) нацпроекта «Новые технологии сбережения здоровья», а также формированию специализированного федерального проекта или подпрограммы в составе, например, государственной программы «Развитие здравоохранения», направленной на создание, модернизацию и развитие соответствующей инфраструктуры здравоохранения в сфере изготовления ЛП, разработку и освоение новых технологий изготовления ЛП, поддержку фармацевтических работников, занятых при изготовлении ЛП.
Для решения задачи по регулярному мониторингу деятельности ПА одним из возможных путей реализации является внесение изменений в приказ Министерства здравоохранения Российской Федерации от 22.05.2023 № 249н6, определяющих точный состав показателей, которые имеют существенное значение для принятия управленческих и административных решений в сфере организации здравоохранения и фармацевтического дела.
- Существует высокая потребность в создании единого центра компетенций по регулированию и методической поддержке развития фармацевтической помощи и оказания фармацевтических услуг в части изготовления ЛП.
На текущий момент одной из перспективных моделей по созданию такого центра компетенций является принцип развития сети национальных исследовательских центров, в том числе в форме национального фармацевтического исследовательского центра (далее – НФИЦ). Функции НФИЦ могут включать в себя организационно-методическую поддержку краевых, республиканских, областных, окружных фармацевтических организаций сферы изготовления ЛП с дальнейшим формированием вертикально-интегрированной системы организационно-методического сопровождения при оказании фармацевтической помощи в субъектах РФ. В целом, в рамках действующего или нового федерального проекта есть возможность предусмотреть формирование сети НФИЦ и учреждений-лидеров по отдельным профилям оказания фармацевтической помощи. Специализированный НФИЦ для ПА может формировать и развивать соответствующую систему инспектората по внедрению, реализации надлежащей практики изготовления и отпуска ЛП.
Как известно, с момента проведения предыдущего мониторинга [2] и начала функционирования Рабочей группы были приняты правила изготовления и отпуска ЛП, а также ряд общих фармакопейных статей, посвященных аптечному изготовлению ЛП7. Ввиду сохранения ряда ограничений, которые влияют на показатели сокращения ПА, примером глубокого понимания особенностей организации процессов по изготовлению и контролю качества ЛП, специфики деятельности, а также текущих реалий данной сферы, рекомендуется с бо’льшим вниманием относиться к сбалансированным предложениям по совершенствованию регулирования в отношении основного документа, регулирующего Правила изготовления и отпуска ЛП. Примеры широко представлены профессиональным фармацевтическим сообществом, в том числе в рамках процедуры общественного обсуждения, и централизованы в исх. № ФАЗ-4/724 и № ФАЗ-4/726 от 30.05.2023 г. Важно подчеркнуть, что сегодня необходимо учитывать мировую практику – переход на правила надлежащей практики изготовления и отпуска ЛП, что заключается не просто в замене наименования нормативного документа, а представляет системную смену парадигмы и подходов при организации соответствующего вида фармацевтической деятельности. Такие практики уже действуют в странах БРИКС [4] и уполномоченные органы государственной власти с поддержкой научного и экспертного сообщества успешно внедряют современные подходы. В ранее проведенных исследованиях [5, 6] представлены результаты изучения мирового опыта по организации деятельности ПА, где, в частности, в заключениях отмечено, что текущий объем и положения нормативных правовых документов сохраняют устаревшие подходы в регулировании деятельности производственных аптек. Последнее также наиболее ярко прослеживается в развитии регулирования по отношению к так называемым «госпитальным исключениям» [7] – согласно ст. 13 Федерального закона от 12.04.2010 № 61-ФЗ «Об обращении лекарственных средств» (далее – ФЗ-61)8 не подлежат государственной регистрации радиофармацевтические и биотехнологические ЛП, изготовленные в МО в рамках лицензии на медицинскую деятельность. При введении в ст. 13 ФЗ-61 РФЛП изначальный подход заключался в отсылке к требованиям по их изготовлению, предусмотренных правилами изготовления и отпуска ЛП, т.е. регулятор планировал развивать персонифицированную медицину в рамках фармацевтической деятельности. Однако к текущему времени положения об изготовлении биотехнологических ЛП показывают планирование в разработке отдельных подзаконных нормативных правовых документов для каждого типа или вида ЛП, согласно внедрению отдельных и самостоятельных правил, утверждаемых Правительством РФ. С высокой степенью вероятности описанное будет распространено и на высокотехнологичные ЛП в 2026 году.
В области персонифицированной медицины вероятно появление существенного объема дегармонизированного права со значительным количеством разрозненных нормативных правовых документов и подчиненности субъектов обращения изготавливаемых ЛП к различным подведомственным органам государственной власти, выходящим за рамки фармацевтической деятельности, что не является оптимальной и сбалансированной практикой. Важно подчеркнуть, что фармацевтическая деятельность в фундаментальной своей основе не сосредотачивается на исключительно «орфанной», «радиофармацевтической», «биотехнологической» или других возможных подвидов аптек, а предполагает реализацию комплексной организации, управления и развития инфраструктуры, в том числе в рамках единых и гармонизированных регуляторных условий, предусматривая возможность изготавливать все типы лекарственных препаратов и виды лекарственных форм, в соответствии с теми особенностями, которые обеспечивают качество и безопасность за счет последовательных «уровневых» и процессных требований, исходя из критериев «токсичности» или «активности» действующих веществ.
Таким образом, необходима реализация согласованной государственной политики в сфере изготовления ЛП, в том числе в субъектах РФ, где дальнейшее продолжение работ над совершенствованием регулирования деятельности ПА должно отражаться в рациональных регуляторных подходах, а не в продолжении сохранения ограничений, которые не позволяют реализовать эффективные экономические и социальные модели развития данной деятельности для целей системы здравоохранения и социальных служб РФ, что может быть одной из задач разрабатываемой и планируемой к принятию Стратегии лекарственного обеспечения населения Российской Федерации на период до 2035 года.
Авторы выражают благодарность за участие, поддержку и доверие при выполнении настоящего исследования:
- Фармацевтическим работникам производственных аптек Российской Федерации, которые ежедневно содействуют повышению уровня лекарственного обеспечения, предоставляя доступ к персонализированным видам лекарственной терапии, прежде всего для детского населения, а также руководителям медицинских и аптечных организаций, сохраняющих и развивающих социально значимый вид фармацевтической деятельности;
- Федеральной службе по надзору в сфере здравоохранения (Росздравнадзору) за помощь в реализации методологии и содействие в повышении качества данных об осуществлении фармацевтической деятельности с правом изготовления лекарственных препаратов;
- Федеральному государственному бюджетному учреждению «Информационно-методический центр по экспертизе, учету и анализу обращения средств медицинского применения» Федеральной службы по надзору в сфере здравоохранения (ФГБУ «ИМЦЭУАОСМП» Росздравнадзора) за ценные рекомендации при рецензировании данной работы и содействие в публикации;
- Федеральному государственному бюджетному учреждению «Научный центр экспертизы средств медицинского применения» Министерства здравоохранения Российской Федерации (ФГБУ «НЦЭСМП» Минздрава России) за содействие и информационную поддержку при выполнении данного исследования;
- Региональным органам исполнительной власти, в частности, Комитету по здравоохранению Ленинградской области, Комитету по здравоохранению Санкт-Петербурга, Департаменту здравоохранения города Москвы, за содействие и информационную поддержку при выполнении данного исследования;
- Некоммерческим и саморегулируемым организациям: Ассоциации государственных аптечных сетей; Ассоциации независимых аптек; Ассоциации аптечных учреждений «Союзфарма»; Ассоциации содействия развитию аптечной отрасли «Аптечная гильдия»; Союзу «Национальная Фармацевтическая Палата» за содействие и информационную поддержку при выполнении данного исследования.
______________________________________________________________________
1 В структуру анализа включены данные из анкет, которые содержали значимую информацию по структурированным блокам, при этом исключены анкеты, которые не содержали сведения в связи с отнесением информации к «бизнес-процессам» и (или) «коммерческой тайне».
2 Единый реестр лицензий, в том числе лицензий, выданных органами государственной власти субъектов Российской Федерации в соответствии с переданным полномочием по лицензированию отдельных видов деятельности. URL: https://roszdravnadzor.gov.ru/services/licenses (дата обращения: 10.07.2024).
3 Федеральный закон от 05.12.2022 № 502-ФЗ «О внесении изменений в статью 56 Федерального закона «Об обращении лекарственных средств». Электронный ресурс. URL: https://docs.cntd.ru/document/1300131660 (дата обращения: 24.10.2024).
4 Закон Республики Татарстан от 22.11.2012 № 87-ЗРТ «О регулировании отдельных вопросов в сфере охраны здоровья граждан в Республике Татарстан». URL: https://docs.cntd.ru/document/422403341 (дата обращения: 24.10.2024).
5 Каверина А. Аптеку для создания редких лекарств запустят в Сириусе в 2025 году // Коммерсантъ. – URL: https://www.kommersant.ru/doc/7283342. Дата публикации: 06.11.2024.
6 Приказ Министерства здравоохранения Российской Федерации от 22.05.2023 № 249н «Об утверждении правил изготовления и отпуска лекарственных препаратов для медицинского применения аптечными организациями, имеющими лицензию на фармацевтическую деятельность». URL: https://docs.cntd.ru/document/1301699481 (дата обращения: 11.12.2024)
7 Лекарственные препараты аптечного изготовления. URL: https://pharmacopoeia.regmed.ru/pharmacopoeia/izdanie-15/1/1-7/ (дата обращения: 11.12.2024)
8 Федеральный закон от 12.04.2010 № 61-ФЗ «Об обращении лекарственных средств». URL: https://docs.cntd.ru/document/902209774 (дата обращения: 11.12.2024).
- Farrakhov A.Z., Leonov S.D., Bashankaev B.N., Ogul L.A., Solomatina T.V., Krupnova I.V., Yurochkin D.S., Erdni-Garyaev S.E., Mamedov D.D., Golant Z.M., Chagin D.A., Narkevich I.A. Monitoring of compounding pharmacies in the Russian Federation or 2023–2024 (part 1) // Vestnik Roszdravnadzora. – 2025. – Vol 3. – P. 6–28. (In Russian).
- Fisenko V.S., Farrakhov A.Z., Solomatina T.V., Alekhin A.V., Yurochkin D.S., Erdni-Garyaev S.E., Mamedov D.D., Golant Z.M. Monitoring of compounding pharmacies in the Russian Federation // Vestnik Roszdravnadzora. – 2023. – Vol. 3. – P. 22–33. – EDN XZJIJT. (in Russian).
- Fisenko V.S., Farrakhov A.Z., Mamedov D.D., Yurochkin D.S., Golant Z.M., Narkevich I.A. Review of judicial practice in relation to public procurement of extemporal drugs for 2012–2022 // Vestnik Roszdravnadzora. – 2023. – Vol. 5. – P. 19–30. – EDN XCIZZY. (In Russian).
- Yurochkin D.S., Mamedov D.D., Erdni-Garyaev S.E., Yarutkin A.V., Bagirova V.L., Guryanov P.S., Loudiyi O., Li W. Review of BRICS regulatory practices in the field of drugs compounding. Pharmacy & Pharmacology. 2024; 12(2): 172–194. DOI: https://doi.org/10.19163/2307-9266-2024-12-2-172-194. (In Russian).
- Erdni-Garyaev S.E., Mamedov D.D., Yurochkin D.S., Zelikova D.D., Golant Z.M., Fisenko V.S., Narkevich I.A. Pharmacy Compounding Regulation in the German Pharmaceutical Market. Part 2. Organisational Features (Review). Regulatory Research and Medicine Evaluation. 2025; 15(1): 63–81. DOI: https://doi.org/10.30895/1991-2919-2024-590.
- Mamedov D.D., Yurochkin D.S., Golant Z.M., Fisenko V.S., Alekhin A.V., Narkevich I.A. Past, current and future of legal regulation of drugs compounding in the Russian Federation. Pharmacy & Pharmacology. 2023; 11(3): 176–192. DOI: https://doi.org/10.19163/2307-9266-2023-11-3-176-192. – EDN QXJFKF. (In Russian).
- Mamedov D.D. Hospital exceptions in the manufacture of drugs / D.D. Mamedov // Pavlovsk readings 2023: Proceedings of the IX International scientific and practical conference dedicated to the 130th anniversary of the birth of Professor N.K. Vereshchagin, Kursk, October 13, 2023. - Kursk: Kursk State Medical University, 2023. - P. 64–69. – EDN CZYHJO. (In Russian).
