LABORATORY CONTROL
Microbiological studies: estimation of measurement uncertainty of quantitative microbiological quantities
1 — Federal state budgetary institution «Information center for expertise, accounting and analysis of circulation of medical products» of Federal Service for Surveillance in Healthcare, Kursk branch, 122 letter «Б», 50 years of October st., Kursk, 305040, Russian Federation.
ОRCID: https://оrcid.оrg/0000-0002-7212-338X
2 — Federal state budgetary institution «Information center for expertise, accounting and analysis of circulation of medical products» of Federal Service for Surveillance in Healthcare, Kursk branch, 122 letter «Б», 50 years of October st., Kursk, 305040, Russian Federation.
ORCID: https://orcid.org/0000-0001-6197-1351
The article presents the basic concepts and principles of uncertainty in the measurement of microbiological quantities on the example of intralaboratory control in a microbiological laboratory.
Keywords: measurement uncertainty, standard deviation, total standard uncertainty, intermediate precision, technical component, matrix component, Poisson distribution
Background.
Согласно широко известному определению, «качество лекарственного средства – это соответствие лекарственного средства требованиям фармакопейной статьи либо, в случае ее отсутствия, нормативной документации или нормативного документа» [12]. Таким образом, заключение о качестве конкретного образца лекарственного средства выносится на основании ряда испытаний, оцениваемых исключительно как положительное или отрицательное решения.
Бактериологические исследования лекарственных средств являются частью фармацевтической микробиологии, цель которой – определение качества лекарственных средств в соответствии с требованиями и методами Государственной Фармакопеи. Продукцию, выпускаемую на мировой рынок фармацевтической промышленностью, по уровню микробиологической чистоты можно условно разделить на две части. Около 20% препаратов должны быть стерильными, а в остальных случаях допускается присутствие ограниченного количества микроорганизмов, исключая определенные виды бактерий, грибов, представляющих опасность для здоровья человека.
В настоящее время международными руководствами установлено, что для достоверности, сопоставимости и взаимного признания результатов измерений следует оценивать неопределенность измерений, интервал которых вокруг результата не должен выходить за пределы (или предел) поля допуска [1]. В случае микробиологических испытаний, проводимая в соответствии с требованиями фармакопеи Евразийского экономического союза и Государственной фармакопеи Российской Федерации (XIV издание) оценка стандартного отклонения воспроизводимости или стандартного отклонения прецизионности в промежуточных условиях осуществляется для каждого вида целевого микроорганизма, каждой матрицы, а также для каждого метода испытаний, используемого лабораторией. Обработка данных проводится в логарифмической шкале, важно использование естественно контаминированных образцов [6, 11].
Главным критерием валидации количественных величин в методиках проведения различных испытаний является неопределенность измерений и метрологическая прослеживаемость. Классический набор аналитических характеристик, рассматриваемых при валидации, таких как сходимость/воспроизводимость, правильность, предел обнаружения и т.д., предложено заменить на одну «функцию неопределенности», выражающую зависимость неопределенности измерений от концентрации определяемого компонента. Это означает, что точность методики анализа приобретает «метрологический характер» [5].
Определение неопределенности
Неопределенность измерений (measurement uncertainty) – это параметр, связанный с результатом измерений, который характеризует разброс значений, которые могли бы быть обоснованно приписаны измеряемой величине [2]. Параметром может быть, например, стандартное отклонение, называемое стандартной неопределенностью измерений (или кратное ему число), или половина ширины интервала с установленной вероятностью охвата. В целом, при данном объеме информации подразумевается, что неопределенность измерений связывают с определенным значением, приписываемым измеряемой величине. Изменение этого значения приводит к изменению связываемой с ним неопределенности.
Источники неопределенности
Неопределенность результата измерения может возникать вследствие влияния различных факторов, включая неполное определение измеряемой величины, отбора проб, эффекты матрицы и мешающие влияния, условия окружающей среды, погрешности средств измерений массы и объема, неопределенности значений эталонов, приближения и допущения, являющиеся частью метода и процедуры измерений, а также случайные колебания [3].
Составляющие неопределенности
- Техническая составляющая – это изменчивость результатов, вызванная реализацией этапов метода испытаний: взятие, перемешивание и растворение порции для испытаний, подготовка первичной суспензии и последовательных разбавлений, инкубация и питательная среда. В нашем исследовании техническая составляющая неопределенности (Utech) представлена стандартным отклонением промежуточной прецизионности (1) (внутрилабораторной воспроизводимости) [2]:
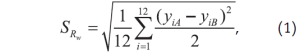
где i – индекс измерения, i = [1; n], (n ≥ 10); yiA и yiB – данные, преобразованные в логарифмическую шкалу, от условий A и B соответственно, [log10(колониеобразующая единица на грамм, КОЕ/г)].
- Матричная составляющая характеризует степень репрезентативности порции для испытаний (Umatrix). Может определяться:
- как фиксированное значение (для достаточно однородных проб может приниматься равной 0,1 log10 (КОЕ/г или КОЕ/см3);
- как стандартное отклонение повторяемости (испытания нескольких порций для испытаний из одной лабораторной пробы в условиях повторяемости) [3].
- Составляющая распределения представляет собой внутреннюю изменчивость, связанную с распределением микроорганизмов в образце (UPoisson). В данном анализе использовалось распределение Пуассона (метод подсчета колоний):
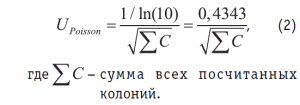
При оценке суммарной неопределенности может оказаться необходимым рассмотрение каждого источника неопределенности по отдельности, чтобы установить вклад именно этого источника. Каждый из отдельных вкладов рассматривается как составляющая неопределенности. Если составляющая неопределенности выражена в виде стандартного отклонения, она определяется как стандартная неопределенность. Оценка суммарного эффекта нескольких составляющих уменьшает объем работы, и даже тогда, когда составляющие, вклад которых оценивается совместно, действительно коррелируют, можно обойтись без учета этой корреляции [3].
Суммарная неопределенность – это сумма отдельно оцененных технической, матричной неопределенностей и составляющей распределения (3). При таком суммировании используют закон распространения неопределенностей [8]:
![]()
Этапы оценивания неопределенности
- Описание измеряемой величины, включая соотношение между измеряемой величиной и параметрами от которых она зависит.
- Выявление источников неопределенности. Включает источники, вносящие вклад в неопределенность параметров в том самом соотношении, которое было установлено на этапе 1.
- Количественное описание составляющих неопределенности. Определение значений неопределенности, присущей каждому выявленному потенциальному источнику. Возможно определение единого вклада в неопределенность, связанного с несколькими источниками.
- Вычисление суммарной неопределенности. Результаты, полученные на предыдущем этапе, состоят из количественно описанных вкладов в общую неопределенность, связанных либо с отдельными источниками, либо с суммарными эффектами нескольких источников. Эти вклады следует выразить в виде стандартных отклонений и просуммировать для получения суммарной стандартной неопределенности в соответствии с имеющимися правилами [5, 7].
- Расчет расширенной неопределенности. Применяется для расширения уровня доверия, связанного с суммарной стандартной неопределенностью, вычисляется по формуле (4) с доверительным уровнем 95% [3, 4]:
![]()
Оценка количественных микробиологических величин в микробиологической лаборатории Курского филиала ФГБУ ИМЦЭУАОСМП Росздравнадзора
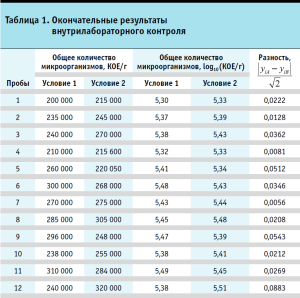
В ходе проведения внутрилабораторного контроля по микробиологической чистоте образца категории 4А ОФС.1.2.4.0002.18 по показателю «общее количество аэробов» глубинным методом, были получены результаты, представленные в таблице 1. Образец был разделен на 12 проб по 10 г. Контроль проводился двумя исследователями в разные дни с интервалом в 3-е суток. Посевы просматривались ежедневно. Подсчет колоний производился через 48 часов (предварительный результат) и через 5 суток (окончательный результат) [9, 10].
На основе данных таблицы 1 была проведена оценка неопределенности исследования, результаты которой представлены в таблице 2.
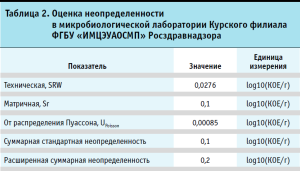
Conclusion.
Исследование на микробиологическую чистоту было проведено по разработанному стандарту организации – стандартизованной операционной процедуре (СОП) «Внутрилабораторный контроль качества и достоверности результатов испытаний». Согласно ГОСТ ISO/IEC 17025-2019 лаборатории должны определять вклад(ы) в неопределенность измерений. При оценке неопределенности все существенные вклады, в том числе связанные с отбором образцов, должны учитываться с применением соответствующих методов анализа (п. 7.6) [9].
Результаты полученных данных оценки неопределенности позволяют говорить о достоверности, сопоставимости результатов, не выходящих за пределы поля допуска заявленной расширенной неопределенности измерений. Оценка производилась в соответствии с ISO 19036 и основана на стандартном отклонении, умноженном на коэффициент охвата 2, что обеспечивает уровень доверия приблизительно 95%. Суммарная стандартная неопределенность принята равной стандартному отклонению промежуточной прецизионности.
Категория 4а ОФС.1.2.4.0002.18 «Микробиологическая чистота» является неоднородной в отношении количества аэробных бактерий, микробная загрязненность данного образца составила 2,6 105 КОЕ/г или 5,4 0,2 [log10 (КОЕ/г)], от среднего значения общего количества микроорганизмов условия 1 и 2, что не противоречит заявленным нормам Государственной фармакопеи Российской Федерации.
- EURACHEM/CITAC. Guide Quantifying Uncertainty in Analytical Measurement.
- JCGM 200:2008 International vocabulary of metrology – Basic and general concepts and associated terms (VIM3).
- ISO 19036:2019 Microbiology of the food chain – Estimation of measurement uncertainty for quantitative determinations.
- ISO/ IEC GUIDE 98-6:2021 Uncertainty of measurement – Part 6: Developing and using measurement models.
- GOST ISO/IEC Guide 98-3 Uncertainty of measurement. Part 3. Guide to the expression of uncertainty in measurement. (in Russian).
- GOST ISO/IEC Guide 98-1 Uncertainty of measurement. Part 1. Introduction to guides on the expression of uncertainty in measurement. (in Russian).
- GOST ISO/lEC Guide 98-3/Suppl 1:2008 Uncertainty of measurement. Part 3. Guide to the expression of uncertainty in measurement. Supplement 1. Propagation of distributions using a Monte-Carlo method.
- GOST ISO/IEC Guide 98-3/Suppl 2:2011 Uncertainty of measurement. Part 3. Guide to the expression of uncertainty in measurement. Supplement 2. Extension to any number of output quantities. (in Russian).
- GOST ISO/IEC 17025-2019 General requirements for the competence of testing and calibration laboratories. (in Russian).
- State Pharmacopoeia of the Russian Federation. OFS.1.2.4.0002.18 “Microbiological purity”. (in Russian).
- Pharmacopoeia of the Eurasian Economic Union. (in Russian).
- Federal Law No. 61-FZ of April 12, 2010 “On the Circulation of Medicines”. (in Russian).
