INNOVATIVE MEDICAL TECHNOLOGY
Topical hemostatic adhesives based on chitosan and polymer compositions
1 — Federal State Budgetary Institution “Russian Scientific Center of Radiology and Surgical Technologies named after Akad. A.M. Granova” of the Ministry of Health of the Russian Federation, 70, Leningradskaya str., Pesochny, St. Petersburg, 197758, Russian Federation.
ORCID: https://orcid.org/0009-0002-6098-4737
2 — Federal State Budgetary Institution “Russian Scientific Center of Radiology and Surgical Technologies named after Akad. A.M. Granova” of the Ministry of Health of the Russian Federation, 70, Leningradskaya str., Pesochny, St. Petersburg, 197758, Russian Federation.
ORCID: https://orcid.org/0000-0002-1577-4178
3 — Federal State Budgetary Institution “Russian Scientific Center of Radiology and Surgical Technologies named after Akad. A.M. Granova” of the Ministry of Health of the Russian Federation, 70, Leningradskaya str., Pesochny, St. Petersburg, 197758, Russian Federation.
ORCID: https: //orcid.org/0000-0001-8174-7461
4 — Federal State Budgetary Institution “Russian Scientific Center of Radiology and Surgical Technologies named after Akad. A.M. Granova” of the Ministry of Health of the Russian Federation, 70, Leningradskaya str., Pesochny, St. Petersburg, 197758, Russian Federation.
ORCID: https://orcid.org/0000-0003-0501-7007
5 — Federal State Budgetary Institution “Russian Scientific Center of Radiology and Surgical Technologies named after Akad. A.M. Granova” of the Ministry of Health of the Russian Federation, 70, Leningradskaya str., Pesochny, St. Petersburg, 197758, Russian Federation.
ORCID: https://orcid.org/0000-0001-8077-9832
6 — Federal State Budgetary Institution “Russian Scientific Center of Radiology and Surgical Technologies named after Akad. A.M. Granova” of the Ministry of Health of the Russian Federation, 70, Leningradskaya str., Pesochny, St. Petersburg, 197758, Russian Federation.
ORCID: https://orcid.org/0000-0002-1630-0564
7 — Federal State Budgetary Institution “Russian Scientific Center of Radiology and Surgical Technologies named after Akad. A.M. Granova” of the Ministry of Health of the Russian Federation, 70, Leningradskaya str., Pesochny, St. Petersburg, 197758, Russian Federation.
ORCID: https://orcid.org/0000-0003-3882-1720
8 — Federal State Budgetary Institution “Russian Scientific Center of Radiology and Surgical Technologies named after Akad. A.M. Granova” of the Ministry of Health of the Russian Federation, 70, Leningradskaya str., Pesochny, St. Petersburg, 197758, Russian Federation.
ORCID: https://orcid.org/0000-0001-8980-5240
The article presents the results of the development of new local hemostatic agents based on chitosan and adhesive polymers. By combining chitosan with ingredients bearing guanidine and polyhydrofenol groups, an effective topical hemostatic agent with increased adhesion (including to a wet wound surface) was obtained, which does not require additional materials to fix it.
In addition, a prototype of an agent for local hemostasis based on a polymer composition in the form of a film (xerogel), which, due to its hydrophilicity, has strong adhesion to wet surfaces, has been created.
Both films obtained by the drying method are biodegradable, have good hemostatic properties, and strong adhesion to the wound surface and elasticity. The developed local hemostatic agents are universal and suitable for both external wounds and intrasurgical use when working with parenchymal organs and vessels.
Keywords: local hemostatic agents with increased adhesion, hemostatic agents based on chitosan and polymer compositions, chitosan, tannin, arginine, polyvinyl pyrrolidone, polyethylene glycol, hemostasis
Background.
Все более актуальной в современной медицине становится проблема разработки новых местных гемостатических средств. Эти изделия широко применяются на догоспитальном этапе, а также при оказании стационарной помощи во время проведения оперативных вмешательств. Особенно часто местные гемостатические средства применяются в хирургии паренхиматозных органов – они позволяют достичь гемостаза, не травмируя при этом ткани, как это происходит при использовании физических (коагуляция) или механических (прошивание, перевязывание источника кровотечения) методов окончательного гемостаза.
На сегодняшний день существует большой выбор местных гемостатических средств, созданных на основе коллагена, целлюлозы, факторов свертывания крови человека или животных, хитозана и альгината. Все эти продукты имеют свои положительные и отрицательные стороны [1,2]. При этом относительно недорогие местные гемостатические средства обычно обладают сравнительно меньшей эффективностью, в то время как более эффективные местные кровоостанавливающие средства (такие как Тахокомб) являются значительно более дорогими [3,4].
В связи с этим до сих пор остается актуальной проблема синтеза недорого и эффективного средства для локального гемостаза. Одним из наиболее очевидных веществ-кандидатов остается хитозан, который входит в состав многих предложенных на сегодняшний день средств для местного гемостаза [5]. Другим перспективным направлением является использование биосовместимых адгезивных полимеров.
Цель работы
Описание метода разработки нового местного гемостатического средства на основе модифицированного хитозана и биосовместимых полимерных композиций.
Материалы и методы
Авторами создано два прототипа композитных гемостатических пленок, первый из которых выполнен на основе хитозана, второй – на основе биосовместимых полимеров. Была выбрана форма сухой пленки, поскольку влажный гидрогель не обладает достаточной адгезией, так как в этом случае нет плотного контакта положительно заряженных групп с поверхностями клеток. Использование сухой пленки приводит к тому, что в месте ее взаимодействия с тканью происходит локальная дегидратация поверхности ткани, обеспечивающая плотный контакт между функциональными группами компонентов пленки и клеточной мембраной.
Создан прототип (пленка А) медицинского изделия на основе хитозана, выполненный в виде двухслойной пленки, которая содержит несущий слой и слой для контакта с раной из соли хитозана. Несущий слой содержит соль хитозана (ацетат), глицерин и воду, а слой для контакта с раной содержит ацетат хитозана, таннин, воду и аргинин в следующем соотношении компонентов, масс. %: соль хитозана 2-4, глицерин 1, таннин 1, аргинин 1, 96–98% – вода.
Механизм действия гемостатического средства основан на том, что положительный заряд –NH2 группы хитозана электростатически взаимодействует с анионами на поверхности эритроцитов, что приводит к интенсивной агрегации эритроцитов вокруг ранения с образованием тромбов, которые быстро останавливают кровотечение [6]. Хитозан способствует активации тромбоцитов и усилению их адгезии. Кроме того, in vivo хитозан приводит к контактной активации факторов свертывания крови, укрепляя сгусток. Он биологически инертен и расщепляется лизоцимом крови [7].
В основе адгезивного слоя, контактирующего с раной, применяется органическая соль хитозана, для создания которой могут быть использованы органические и одноосновные неорганические кислоты, например: ацетат, лактат, сукцинат, малат, цитрат и им подобные. Дополнительно адгезивный слой пленки содержит аргинин – аминокислоту, имеющую в своем составе сильно положительно заряженную гуанидиновую группу, благодаря которой потенцируются адгезивные и гемостатические свойства хитозана [8]. Пленка хитозан/аргинин продемонстрировала подавление роста колоний E. Coli и S. Aureus. Более того, раствор хитозана и аргинина не проявлял цитотоксичности и способствовал клеточной пролиферации [9].
Адгезивные свойства пленки и устойчивость к размоканию во влажной среде усилены за счет введения в состав композиции таннина – растительного полифенольного дубильного вещества. Хорошая адгезивность таннина обусловлена его взаимодействием с нуклеофильными группами, такими как –NH2 или –SH на поверхности ткани. Включение таннина в композицию обеспечило значительную силу адгезии к влажной поверхности [10]. Биологические адгезивы на основе таннина обладают антиоксидантными, противовоспалительными и антибактериальными свойствами, он может связывать свободные радикалы, а также способствовать пролиферации клеток млекопитающих. Противовоспалительные свойства таннина обусловлены его способностью вызывать снижение экспрессии интерлейкина 1В и фактора некроза опухоли альфа [11]. Таннин не обладает токсичностью, что было продемонстрировано при применении повязок, содержащих таннин, у больных с обширными ожогами [12].
Несущий слой также, как и активный, содержит соль хитозана в качестве основы, что делает пленку биологически инертной и позволяет оставлять ее на ране после завершения операции на паренхиматозных органах и сосудах.
При изготовлении пленки на ровную поверхность наносится раствор хитозана с глицерином и высушивается в течение 48 часов при комнатной температуре в вытяжном шкафу. Затем на высушенную подложку заливается смесь хитозана, аргинина и таннина. Слой также высушивается при комнатной температуре в течение 48 часов. После высыхания композитная пленка готова к использованию (рис. 1).

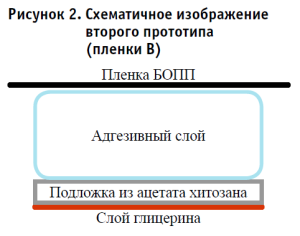
В качестве второго прототипа (пленка В) (рис. 2) создано местное гемостатическое средство на основе адгезивных полимеров, которые, благодаря своей гидрофильности, способны создавать прочные адгезионные соединения с кровоточащей поверхностью поврежденного органа. Основными компонентами для создания нового местного гемостатического средства явились поливинилпирролидон (ПВП) и полиэтиленгликоль (ПЭГ), которые способны к образованию водородных связей [13]. Карбонильные группы в составе ПВП являются донорами электронов, как и атомы кислорода оксиэтиленовых мономерных звеньев ПЭГ [14]. Эти химические свойства позволяют данным соединениям создавать прочные адгезионные взаимодействия. ПВП и ПЭГ не обладают токсическим действием на организм, что было доказано в клинической практике [15].
Недостатками полимерной композиции являются: растворимость в течение двух часов при длительном контакте с кровью и отсутствие собственных гемостатических свойств. Для преодоления быстрой растворимости в воде при сохранении адгезивных свойств использованы такие соединения, как бутили метилпарабен. Они позволяют пленке оставаться нерастворимой до трех суток, при этом не происходит потери адгезивных свойств. Для потенцирования адгезивных свойств в пленку добавлен также аргинин. Собственные адгезивные свойства пленке придает хитозан, введенный в данную композицию.
Для того, чтобы повысить манипуляционные характеристики пленки, которая по причине высокой адгезии липнет к рукам хирурга, использована подложка, состоящая из ацетата хитозана и покрытая глицерином после высыхания, которая позволяет произвести аппликацию пленки к раневой поверхности без технических трудностей.
Пленка В также имеет форму композитной пластины, несущий слой которой состоит из ацетата хитозана (хитозан 2% мас., уксусная кислота 1% мас., остальное – вода). Несущий слой получают методом полива на подложку из пленки БОПП (биаксиально ориентированная полипропиленовая пленка). Адгезивный слой состоит из полимерной композиции, в состав которой входят: ПВП 68% мас., ПЭГ 30% мас., бутилпарабен/метилпарабен 1%, аргинин 1%, а в качестве растворителя использован 98% спирт. Адгезивный слой наносится методом полива на пленку БОПП, затем высушивается при комнатной температуре в течение суток. Далее производится аппликация несущего слоя на адгезивный, поверх наносится тонкий слой 99,8% глицерина, затем адгезивная поверхность отделяется от подложки.
Представленные местные гемостатические средства, по мнению авторов, могли бы объединить в себе такие полезные свойства, как высокая адгезия, хороший гемостатический эффект и биосовместимость.
Сравнительно быстрая растворимость пленки позволяет предотвратить развитие гнойно-септических осложнений, вызванных инородным телом, оставленным в брюшной полости после операции.
Результаты и обсуждение
Полученные прототипы кровоостанавливающих средств обладают хорошей адгезией и гемостатическими свойствами, что было доказано в экспериментах.
Экспериментальное исследование разработанного нами гемостатического средства проводили на свиньях породы русская белая, самцах, вес свиней 80–100 кг, а также на кроликах породы советская шиншилла весом 8,0–10,0 кг. Исследования проведены после одобрения комитета по этике ФГБУ «Российский научный центр радиологии и хирургических технологий имени академика А.М. Гранова» Минздрава России.
Испытания на животных композитной полимерной пленки А. В условиях операционной под наркозом выполнена лапаротомия. Правая доля печени выведена в рану на салфетках. Скальпелем иссечен участок правой доли размерами 2 2 0,5 см. Дефект осушен салфеткой (рис. 3). Накрыт опытным образцом пленки диаметром 5 см, прижат салфеткой. Экспозиция 20 секунд. Через 20 секунд отмечено плотное прилегание к ткани печени с хорошей адгезией по всей поверхности. Кровотечения не наблюдается. Наблюдение в течение 3 минут 30 секунд для контроля гемостаза. На четвертой минуте адгезия к ткани по-прежнему хорошая. Печень накрыта влажной салфеткой. Переход к испытаниям на аорте.

Брюшная аорта выделена на протяжении 6 см. На сосудистых зажимах пережата выше и ниже зоны доступа. Скальпелем произведена продольная аортотомия, длина разреза – 1 см. Рана осушена салфеткой (рис. 4). Дефект накрыт образцом пленки и прижат салфеткой. Зажимы сняты. Через 30 с отмечено плотное приклеивание образца к аорте и парааортальным тканям. Наблюдается устойчивый гемостаз. Контроль систолического давления – 110 мм.рт.ст.

Перенос внимания на образец пленки на печени. Суммарно через 15 минут после аппликации наблюдается частичное размягчение образца, адгезия сохраняется. Кровотечения из дефекта печени не отмечено.
Селезенка выведена в рану, отграничена салфетками. Скальпелем в средней трети органа иссечен дефект размерами 2 1,5 0,5 см (рис. 5). Наблюдается обильное кровотечение. Дефект осушен салфеткой, после чего сразу же накрыт образцом пленки диаметром около 5 см и прижат салфеткой. Через 30 с наблюдается плотная адгезия по всей площади образца.
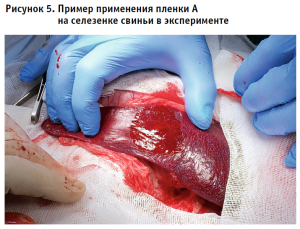
Наблюдение в течение 20 минут. Кровотечение не продолжается. Адгезия сохраняется, подтекания крови не определяется.
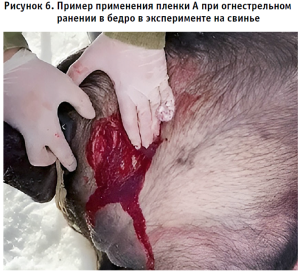
При моделировании наружных ранений выполнен эксперимент в условиях полигона: под наркозом свинье нанесено огнестрельное ранение в область бедра по траектории снаружи внутрь. В области внутренней поверхности бедра выходное отверстие от пули (рис. 6). Из области раны наблюдается обильное кровотечение. Рана осушена марлевой салфеткой, накрыта опытным образцом пленки диаметром 10 см, прижата салфеткой. Экспозиция 30 с. Через 30 с хорошая адгезия пленки к ране и поверхности кожи. Кровотечения не наблюдается. Наблюдение в течение 10 минут для контроля гемостаза. На одиннадцатой минуте адгезия сохраняется без дополнительной фиксации пленки.
Испытания на животных композитной полимерной пленки В. Исследование эффективности гемостатической пленки В при ранениях паренхиматозных органов у кроликов.
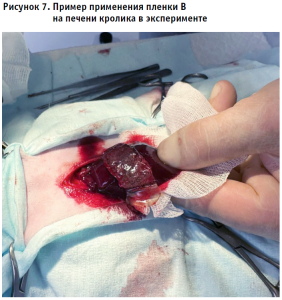
В условиях операционной под наркозом произведена лапаротомия, кролику нанесено ранение печени, размерами 2,0 2,0 см. После того, как рану промокнули салфеткой, произведена аппликация образца гемостатической пленки, размерами 4,0 3,0 см, образец прижат салфеткой. Экспозиция 20 секунд. Через 20 секунд отмечено плотное прилегание к ткани печени с хорошей адгезией по всей поверхности. Гемостаз достигнут. В течение 15 минут гемостаз надежный (рис. 7). Эксперимент проведен на 10 кроликах одного пола и примерно равного веса. Интраоперационный гемостаз достигнут во всех 10 случаях.
На следующий день кроликам выполнена релапаротомия. При осмотре ранения печени: рецидива паренхиматозного кровотечения не отмечено ни в одном из 10 случаев (рис. 8).

Исследование эффективности гемостатической пленки при наружных ранениях. Под наркозом свинье нанесено проникающее колото-резаное ранение передней поверхности груди слева, размерами 5,0 7,0 см. Из области раны отмечено смешанное артериально-венозное кровотечение. Произведена аппликация опытного образца пленки В диаметром 6 см. Плотное прижатие в течение 20 секунд. Достигнут гемостаз (рис. 9).
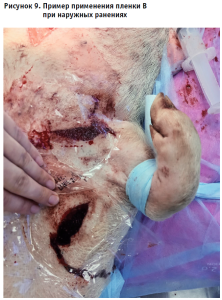
Наблюдение в течение 20 минут за нанесенным ранением: признаков продолжающегося кровотечения нет.
Таким образом, оба разработанных прототипа местного гемостатического средства доказали свои адгезивные и гемостатические свойства на животных моделях при проведении первичных экспериментов.
Conclusion.
Разработанные местные гемостатические средства в экспериментах продемонстрировали свою эффективность. Необходимо продолжить исследования по направлению разработки средств для локального гемостаза на основе полимерных композиций и хитозана. Созданные композиции для местного гемостаза обладают следующими достоинствами:
- универсальность использования: эффективны как раневые повязки и как средства для интраоперационного гемостаза при работе с паренхиматозными органами;
- могут использоваться интраоперационно при ранениях печени, почек, селезенки и крупных сосудов как средство временного или окончательного гемостаза;
- применимы в качестве раневого гемостатического адгезива при наружных ранах;
- при необходимости отделяются от раневой поверхности без дополнительной травматизации ткани.
Внесение аргинина и таннина в композитные пленки позволяет улучшить их благоприятные свойства, не увеличивая при этом количество побочных эффектов, а наличие подложки увеличивает прочность пленок и устойчивость к размоканию во влажной среде.
Работа выполнена в рамках прикладного научного исследования в интересах медицины и здравоохранения «Разработка медицинского изделия – новое локальное гемостатическое средство с повышенной адгезией для внутриполостного использования – биодеградируемая поликомпонентная пленка» (YBZU-2023-0009).
- Lipatov V.A. Local hemostatics in surgery of the XXI CENTURY (literature review) / V.A. Lipatov, D.A. Severinov, A.R. Saakyan // Innova. – 2019. – No. 1(14). – S. 16–22.
- Local hemostatic agents and ways to improve them / E.V. Budko, D.A. Chernikova, L.M.Yampolsky, V.Ya. Pavlova. – 2019. – T. 27, No. 2. – S. 274–285.
- Costa F.W., Rodrigues R.R., Sousa L.H., Carvalho F.S., Chaves F.N., Fernandes C.P., Perei-ra K.M., Soares E.C. Local hemostatic measures in anticoagulated patients undergoing oral surgery: a systematized literature review. Acta Cir Bras. 2013 Jan; 28(1): 78–83.
- Petlakh V.I. Results of the use of local hemostatic agents in disaster medicine // Disaster Medicine. 2014. No. 4 (88). pp. 21–24.
- Grishin A.A., Zorina N.V., Lutskiy V.I. Chitin and chitosan: Chemistry, biological activity, application // Izvestiya vuzov. Applied chemistry and biotechnology. 2014. No. 1 (6).
- Wang W., Meng Q., Li Q., Liu J., Zhou M., Jin Z., Zhao K. Chitosan Derivatives and Their Application in Biomedicine. Int J Mol Sci. 2020 Jan 12.
- Ovsyannikov V.G., Toropkina Yu.E., Kraskevich V.V., Alekseev V.V., Boychenko A.E., Alekseeva N.S., Kraskevich D.A. Lysozyme – the brink of the possible // Modern problems of science and education. – 2020. – No. 3.
- Song J., Feng H., Wu M., Chen L., Xia W., Zhang W. Preparation and characterization of arginine-modified chitosan/hydroxypropyl methylcellose antibacterial film. Int J Biol Macromol. 2020 Feb 15, P. 750–758.
- Di Martino A. Sittinger M., Risbud M.V. hitosan: a versatile biopolymer for ortho-paedic tissue-engineering // Biomaterials. –2005. – Vol. 26, № 30. – P. 5983–5990.
- Da Sacco L., Masotti A. Chitin and chitosan as multipurpose natural polymers for groundwater arsenic removal and AS2O3 delivery in tumor therapy // Mar. Drugs. – 2010. – Vol. 8, № 5. – P. 1518–1525.
- Guo J., Sun W., Kim J.P., Lu X., Li Q., Lin M., Mrowczynski O., Rizk E.B., Cheng J., Qian G., Yang J. Development of tannininspired antimicrobial bioadhesives. Acta Biomater. 2018 May, P. 35–44.
- Chokotho L., van Hasselt E. The use of tannins in the local treatment of burn wounds – a pilot study. Malawi Med J. 2005 Jun; 17(1) P. 19–20.
- Feldshtein M. M. The contribution of relaxation processes to the strength of adhesive compounds of viscoelastic polymers // High-molecular compounds. Series A. – 2009. – V. 51, No. 11. – S. 2085–2100.
- Pressure-sensitive adhesives with adjustable stickiness / K.A. Bovaldinova, N.E. Sherstneva, M.M. Feldshtein [et al.] // High Molecular Compounds. Series B. – 2019. – V. 61, No. 4. – S. 289–302.
- Makhayeva D.N., Irmukhametova G.S., Khutoryanskiy V.V. Polymeric Iodophors: Preparation, Properties, and Biomedical Applications. Ref. J. Chem. 10, 40–57 (2020).
