PHARMACOTHERAPY
Tools for assessing the rationale of antimicrobial therapy in children. Could AWaRe for clinical recommendations be customized?
1 — Federal State Budgetary Educational Institution of Additional Professional Education “Russian Medical Academy of Continuing Professional Education” of the Ministry of Health of the Russian Federation (RMANPO), 2/1, building 1, Barrikadnaya st., Moscow, 125993, Russian Federation.$; State Budgetary Healthcare Institution of the City of Moscow “Morozovskaya Children's City Clinical Hospital of the Department of Healthcare of the City of Moscow”, 1/9, 4th Dobryninsky Lane, Moscow, 119049, Russian Federation.; Federal State Autonomous Educational Institution of Higher Education “N.I. Pirogov Russian National Research Medical University” of the Ministry of Health of the Russian Federation, 1, Ostrovityanova St., Moscow 117997, Russian Federation.; State Budgetary Institution of the City of Moscow “Scientific Research Institute of Healthcare Organization and Medical Management of the Department of Healthcare of the City of Moscow”, 9, Sharikopodshipnikovskaya st., Moscow, 115088, Russian Federation.
ORCID: https://orcid.org/0000-0001-5272-2070
2 — Federal State Budgetary Educational Institution of Additional Professional Education “Russian Medical Academy of Continuing Professional Education” of the Ministry of Health of the Russian Federation (RMANPO), 2/1, building 1, Barrikadnaya st., Moscow, 125993, Russian Federation.
ORCID: https://orcid.org/0000-0002-4496-3680
3 — State Budgetary Healthcare Institution of the City of Moscow “Morozovskaya Children's City Clinical Hospital of the Department of Healthcare of the City of Moscow”, 1/9, 4th Dobryninsky Lane, Moscow, 119049, Russian Federation.; Federal State Autonomous Educational Institution of Higher Education “N.I. Pirogov Russian National Research Medical University” of the Ministry of Health of the Russian Federation, 1, Ostrovityanova St., Moscow 117997, Russian Federation.
ORCID: https://orcid.org/0000-0002-4382-462Х
4 — Federal State Autonomous Educational Institution of Higher Education “N.I. Pirogov Russian National Research Medical University” of the Ministry of Health of the Russian Federation, 1, Ostrovityanova St., Moscow, 117997, Russian Federation.
ORCID: https://orcid.org/0000-0002-3523-5411
5 — State Budgetary Healthcare Institution of the City of Moscow “Morozovskaya Children's City Clinical Hospital of the Department of Healthcare of the City of Moscow”, 1/9, 4th Dobryninsky Lane, Moscow, 119049, Russian Federation.; Federal State Autonomous Educational Institution of Higher Education “N.I. Pirogov Russian National Research Medical University” of the Ministry of Health of the Russian Federation, 1, Ostrovityanova St., Moscow 117997, Russian Federation.
ORCID: http://orcid.org/0000-0002-2302-1205
6 — Federal State Autonomous Educational Institution of Higher Education “N.I. Pirogov Russian National Research Medical University” of the Ministry of Health of the Russian Federation, 1, Ostrovityanova St., Moscow, 117997, Russian Federation.
ORCID: https://orcid 0000-0002-5371-4264
7 — Federal State Autonomous Educational Institution of Higher Education “N.I. Pirogov Russian National Research Medical University” of the Ministry of Health of the Russian Federation, 1, Ostrovityanova St., Moscow, 117997, Russian Federation.
ORCID https://orcid.org/0000-0001-5787-3900
8 — State Budgetary Healthcare Institution of the City of Moscow “Morozovskaya Children's City Clinical Hospital of the Department of Healthcare of the City of Moscow”, 1/9, 4th Dobryninsky Lane, Moscow, 119049, Russian Federation.
ORCID: https://orcid.org/0000-0001-8272-3648
The article discusses issues that indicate the feasibility of a comprehensive assessment of antimicrobial therapy as a medical technology in multidisciplinary children's hospitals in Russia, the adaptation of WHO tools for assessing adherence to domestic medical recommendations and the implementation of antibiotic therapy management programs in multidisciplinary hospitals for children in clinical practice are proposed.
This study shows the difference between the categorization of antibiotics AWaRe in the reference version of WHO2019 and according to the version based on domestic clinical recommendations for 2019–2021, using the example of children's anchor hospitals in 7 constituent entities of Russia, the importance of including analysis data in the complex-integral assessment of antimicrobial therapy as a medical technology primary medical record according to the WHO Toolkit questionnaire. According to the data obtained, with the same nosologically diagnoses in the pediatrics profile, hospitalized children used different approaches to pharmacotherapy in the infectious and somatic departments, clinical practice in the infectious diseases departments was distinguished by a more aggressive approach.
Keywords: rational antimicrobial therapy, pediatrics, antibiotics, prescribing antibiotics in the hospital, AWaRe, categorization of antibiotics AWaRe, evaluation of antimicrobial therapy
Background.
Современные рекомендации ВОЗ продвигают внедрение программ надзора за реальной клинической практикой назначения и применения антимикробных препаратов (АМП) у детей в стационарах методом AWaRe по определенным категориям, предложенным ВОЗ в 2017 г. для взрослых и адаптированным в 2019 г. для детей [3,5]. Внедрение метода AWaRe в соответствии с рекомендациями ВОЗ следует подкреплять результатами исследования точечной распространенности использования АМП у госпитализированных детей [1]. Однако в России практический опыт получения информации по оценке антимикробной терапии, как медицинской технологии в стационаре, не представлен. Адаптация существующих клинико-фармакологических инструментов для оценки реальной клинической практики назначения и применения антибиотиков в детских многопрофильных стационарах России на основе отечественных клинических рекомендаций является перспективным направлением развития для улучшения назначения и применения АМП в стационарах для детей.
Материалы и методы
Наблюдательное многоцентровое исследование сложившейся клинической практики антимикробной терапии в многопрофильных педиатрических стационарах III уровня выполнено в девяти субъектах РФ: Дальневосточном, Приволжском, Сибирском и Центральном федеральных округах.
Частота потребления антимикробных препаратов оценивалась по показателю «число дней терапии на 100 пациенто-дней» для каждого МНН в лекарственных формах для парентерального и перорального применения. Препараты были разделены на следующие категории:
- группа «Доступа» («Access»);
- группа «Контроля» («Watch»);
- группа «Резерва» («Reserve»).
Указанный показатель оценивался методом AWaRe, предложенным ВОЗ. Результаты представлены в виде диаграмм, в процентном соотношении. Количественная оценка показателей выполнена методом DDD-анализа по показателю «число дней терапии на 100 пациенто-дней» (ЧДТ на 100 пд) по каждой АТХ антимикробного препарата.
Организационно-методическое сопровождение проекта состояло из двух частей: первая часть – документарная оценка потребления АМП методом AWaRe в сравнении категоризации на основе клинических рекомендаций 2019–2021 гг. с эталонной версией WHO2019 группой врачей-клинических фармакологов; вторая часть – оценка клинической практики врачами-педиатрами методом Global-PPS в многопрофильном педиатрическом стационаре по вопроснику инструментария ВОЗ для детских стационаров стран-участников ВОЗ.
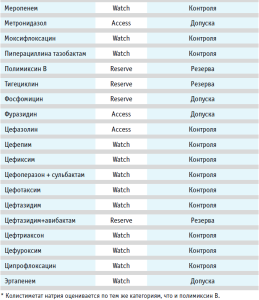
Нами предложена адаптация категоризации АМП для метода AWaRe на основе российских клинических рекомендаций 2019–2021 гг.: «Острый бронхит», «Инфекция мочевых путей у детей», «Острый тонзиллит и фарингит (Острый тонзиллофарингит)», «Острый средний отит», «Острый синусит», «Пневмония (внебольничная)». Проведен сравнительный анализ результатов предложенной категоризации метода AWaRe с эталонной версией WHO2019, варианты категоризации АМП выполнены для метода AWaRe и представлены в таблице по двум версиям [9].
Оценка клинической практики непосредственно «на месте» при визите в детский стационар выполнялась с применением инструмента-вопросника для точечного обследования распространенности использования антибиотиков у госпитализированных детей (Global-PPS) в многопрофильных стационарах семи субъектов РФ в 2020–2021 гг. по вопроснику Инструментария ВОЗ [3,5,9].
Анализ первичной документации проводился по 3139 медицинским картам стационарных больных с обезличиванием персональных данных на момент визита в стационар по чек-листу, содержащему критерии оценки фармакотерапии инструментария ВОЗ в соответствии с установленным диагнозом [6]. Оценка рациональности назначения антимикробной терапии основывалась на отечественных клинических рекомендациях.
Показатель количественной характеристики потребления АМП для построения графического изображения категорий метода AWaRe измерялся методом DDD-анализа, для стационаров III уровня каждого субъекта соответственно на основе данных ATS DDD показателей ВОЗ WHO Collaborating Centre for Drug Statistics Methodology Norwegian Institute of Public Health. Основной показатель для расчета процентного соотношения по МНН для АМП в структуре удельного веса каждой из категорий АМП – «Доступа» (зеленый), «Контроля» (желтый) и «Резерва» (красный) рассчитывался методом DDD-анализа по показателю «число дней терапии по каждому МНН АМП из АТХ J01 Антибактериальные препараты для системного использования» в пересчете на 100 пациенто-дней (далее – ЧДТ по МНН на 100 п/д) по профилю «педиатрия».
Сравнительная оценка проводилась по эталонной версии категоризации антибиотиков WHO2019 и категоризации по предложенной нами версии на основе отечественных клинических рекомендаций 2019–2021 гг.: «Острый бронхит», «Инфекция мочевых путей у детей», «Острый тонзиллит и фарингит (Острый тонзиллофарингит)», «Острый средний отит», «Острый синусит», «Пневмония (внебольничная)».
Эталонная версия категоризации ВОЗ включает перечень основных лекарственных средств (EML) и стратификацию антибиотиков в EML для детей (eMLC) на три группы: «Access» – антибиотики «Доступа» (зеленый), «Watch» – антибиотики «Контроля» (желтый) и «Reserve» – резервные антибиотики (красный). В эталонной версии ВОЗ группа антибиотиков «Доступа» содержит, как правило, антибиотики узкого спектра действия, рекомендуемые в качестве препарата первого и второго выбора при наиболее распространенных клинических инфекционных синдромах, преимущественно имеющие пероральные лекарственные формы. Группа антибиотиков «Контроля» содержит, как правило, классы антибиотиков более широкого спектра действия, в том числе цефалоспорины, имеющие исключительно парентеральные формы введения для терапии пациентов с серьезными инфекциями [3,9]. Группу «Резерва» составляют антибиотики, назначаемые в критических состояниях при инфекциях, вызванных полирезистентными микроорганизмами [9].
Антибиотики, не включенные ни в одну из эталонных версий категоризации из групп «Access», «Watch» и «Reserve», были определены как неклассифицированные, включая все антибиотики, не перечисленные в eMLC, такие как цефалоспорины второго поколения (код ATC: J01DC) и комбинации противомикробных препаратов для системного применения (код ATC: J01RA) [6,8,9].
В настоящем исследовании нами предложена версия категоризации антибиотиков на основе отечественных клинических рекомендаций 2019–2021 гг.: «Острый бронхит», «Инфекция мочевых путей у детей», «Острый тонзиллит и фарингит (Острый тонзиллофарингит)», «Острый средний отит», «Острый синусит», «Пневмония (внебольничная)». В предложенной нами версии категоризации в перечень антибиотиков «Доступа» включены антибиотики 1-2 линии, в перечень антибиотиков «Контроля» включены препараты 3 линии и в перечень антибиотиков «Резерва» включены резервные препараты на основе отечественных клинических рекомендаций 2019–2021 гг.
Нами впервые сформулированы принципы категоризации метода AWaRe WHO на основе новых российских клинических рекомендаций 2019–2021 гг.: «Острый бронхит», «Инфекция мочевых путей у детей», «Острый тонзиллит и фарингит (Острый тонзиллофарингит)», «Острый средний отит», «Острый синусит», «Пневмония (внебольничная)».
Как представлено в таблице, основным отличием между категоризацией антибиотиков в эталонной версии WHO2019 и на основе отечественных клинических рекомендаций 2019–2021 гг. явилось исключение амикацина из категории «Доступа», включение линезолида в категорию «Контроля». В категории антибиотиков «Резерва» изменения коснулись включения амикацина и исключения линезолида.

Цель работы
Показать возможности улучшения комплексно-интегральной оценки антимикробной терапии как медицинской технологии в многопрофильных детских стационарах России, адаптировав предложенные ВОЗ инструменты в целях получения оценки приверженности к отечественным клиническим рекомендациям и внедрения в реальную клиническую практику программ управления антибиотикотерапией у детей.
Результаты исследования
Качественные показатели структуры потребления АМП в якорных стационарах субъектов РФ в 2021 г. по результатам DDDанализа методом AWaRe в традиционной категоризации по версии WHO2019 представлены на рисунке 1.
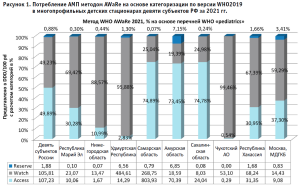
В среднем по России, на основе данных из девяти субъектов РФ, препараты категории «Доступа» («Access») составляли 49,89%, препараты категории «Контроля» («Watch») – 49,23%, препараты «Резерва» («Reserve») – 0,88%.
Качественные показатели структуры потребления АМП, полученные в якорных стационарах девяти субъектов РФ в 2021 г., отличались от данных, полученных при традиционной категоризации по версии WHO2019.
Как представлено на рисунке 2, в среднем по России, на основе данных из девяти субъектов РФ, препараты категории «Доступа» («Access») составляли 44,24% (для сравнения – на рисунке 1 «Access» составляли 49,89%), препараты категории «Контроля» («Watch») – 49,09% (для сравнения – на рисунке 1 «Watch» – 49,23%), препараты «Резерва» «Reserve» – 6,67% (для сравнения – на рисунке 1 «Reserve» – 0,88%).
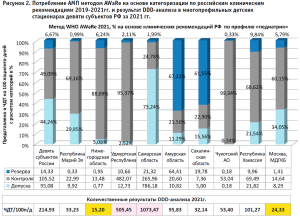
При изменении категоризации по предложенной нами версии на основе отечественных клинических рекомендаций для метода AWaRe, удельный вес препаратов категории «Доступа» («Access», зеленый) в стационарах III уровня составил (в порядке убывания):
- Самарская область – 73,24%;
- г. Москва, ГБУЗ «Морозовская ДГКБ ДЗМ» – 34,05%;
- Республика Марий Эл – 29,85%;
- Республика Хакассия – 21,54%;
- Сахалинская область – 15,26%;
- Амурская область – 11,29%;
- Нижегородская область – 5,08%;
- Удмуртская Республика – 2,52%;
- Чукотский АО – 0,34%.
Удельный вес категории «Контроля» («Watch», желтый) в стационарах III уровня составил (в порядке убывания):
- Чукотский АО – 99,34%;
- Удмуртская Республика – 95,37%;
- Нижегородская область – 88,69%;
- Республика Марий Эл – 69,16%;
- Республика Хакассия – 68,62%;
- г. Москва, ГБУЗ «Морозовская ДГКБ ДЗМ» – 60,15%;
- Самарская область – 24,78%;
- Сахалинская область – 22,09%;
- Амурская область – 21,5%.
Удельный вес категории «Резерв» («Reserve», красный) в стационарах III уровня составил (в порядке убывания):
- Амурская область – 67,21%;
- Сахалинская область – 61,55%;
- Республика Хакассия – 9,84%;
- Нижегородская область – 6,24%;
- г. Москва, ГБУЗ «Морозовская ДГКБ ДЗМ» – 5,79%;
- Самарская область – 1,99%;
- Удмуртская Республика – 2,11%;
- Республика Марий Эл – 0,99%;
- Чукотский АО – 0,33%.
Наибольший удельный вес категории «Резерв» («Reserve», красный) был выявлен в Амурской области (70,5%), и Сахалинской области (58,5%) за счет избыточной практики применения аминогликозидов в качестве негативного паттерна.
В многопрофильных детских стационарах Амурской и Сахалинской области по профилю «педиатрия» в 2021 г. удельный вес категории «Резерв» был самым высоким и составил 67,21% и 61,55% соответственно, при этом количественный показатель потребления в Амурской области для аминогликозидов был выше, чем в других субъектах РФ и составил 61,33 ЧДТ на 100 п/д (98,32%) от всей категории «Резерв», составившей в абсолютных значениях 64,41 ЧДТ на 100 п/д. Количественный показатель потребления в Сахалинской области составил для аминогликозидов 19,5 ЧДТ (98,58%) от всей категории «Резерв», составившей в абсолютных значениях 19,78 на 100 п/д соответственно.
Полученные данные показывают, что из госпитализированных детей по профилю «педиатрия» каждый второй ребенок в Амурской области и каждый пятый в Сахалинской области получал аминогликозиды, при этом аминогликозиды были самыми часто назначаемыми антибиотиками по профилю «педиатрия», что нерационально и не соответствует клиническим рекомендациям 2019–2021 гг.
Проведена сравнительная количественная оценка потребления АМП в исследуемой группе якорных стационаров субъектов РФ по профилю «педиатрия». Суммарный показатель числа дней терапии АМП по группе АТХ «J01 Антибактериальные препараты для системного использования» на 100 пациенто-дней по профилю «педиатрия» в среднем по России в стационарах III уровня в субъектах составил 214,93 на 100 пациенто-дней. Как представлено на рисунке 2, самые высокие показатели потребления АМП для детских стационаров были выявлены в Самарской области (1073,43 ЧДТ на 100 пациенто-дней) и в Удмуртии (ЧДТ 505,45 на 100 пациенто-дней).
Наименьшие показатели потребления АМП были зарегистрированы в Нижнем Новгороде (число дней терапии составило 15,2 на 100 пациенто-дней) и в г. Москве (число дней терапии составило 24,33 на 100 пациенто-дней в ГБУЗ «Морозовская ДГКБ ДЗМ»).
В якорных стационарах субъектов РФ в настоящем исследовании проведен анализ клинической практики по вопроснику инструментария ВОЗ за 2020–2021 гг., исследование проводилось в тех же многопрофильных стационарах, которые предоставляли данные по потреблению АМП. Результаты представлены для наиболее информативных показателей:
- «Причинение необоснованной боли (избыточные манипуляции, анализы, способ введения лекарственных препаратов)»;
- «Полипрагмазия (два и более лекарственных препарата без доказательной базы их применения при данном заболевании)»;
- «Несоответствие лечения диагнозу (по основному)»;
- «Нерациональная антибиотикотерапия (выбор АМП, способ введения, длительность курса, нецелесообразность применения)»;
- «Неадекватная инфузионная терапия»;
- ключевой показатель «Агрессивное лечение (необоснованная госпитализация + полипрагмазия + причинение необоснованной боли)».
Как представлено на рисунке 3, в якорных стационарах субъектов РФ в 2020–2021 гг. показатель «Причинение необоснованной боли (избыточные манипуляции, анализы, способ введения лекарственных препаратов)» для Самарской области составил 47%, Республики Марий-Эл – 46%, показатель «Полипрагмазия (два и более лекарственных препарата без доказательной базы их применения при данном заболевании)» более часто выявлялся в Амурской области 57,5% и в Самарской области – 52,9%, «Несоответствие лечения диагнозу (по основному)» наиболее часто отмечалось в Самарской области – 46,6% и в Амурской области 46,5%.
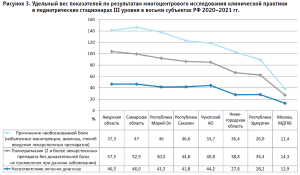
В ГБУЗ «Морозовская ДГКБ ДЗМ» в 2020– 2021 гг. все показатели были ниже по сравнению с данными, полученными из всех представленных данных по стационарам иных субъектов РФ, показатель «Причинение необоснованной боли» составил 11,4%, «Полипрагмазия» – 14,3% и «Несоответствие лечения диагнозу» – 12,9%.
Как представлено на рисунке 4, в якорных стационарах субъектов РФ эксперты-аналитики НМИЦ в 2020–2021 гг. отметили наиболее частое выявление показателя «Неадекватное использование глюкокортикостероидов» в Самарской области – 21,5% и в Республике Марий Эл – 15,3%, «Нерациональная антибиотикотерапия (выбор АМП, способ введения, длительность курса, нецелесообразность применения)» в Самарской области – 49,8% и Республики Марий-Эл – 49,5%, «Неадекватная инфузионная терапия» в для Самарской области – 38,7% и в Амурской области – 37,1%. В ГБУЗ «Морозовская ДГКБ ДЗМ» в 2020– 2021 гг. аналогичные показатели были самыми низкими: «Неадекватное использование глюкокортикостероидов» отмечено в 1,2%, «Нерациональная антибиотикотерапия» – 11,6% и «Неадекватная инфузионная терапия» – 3,8%.
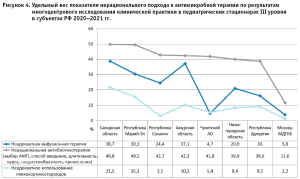
Как показал анализ клинической практики, наибольший удельный вес составил показатель «Нерациональная антибиотикотерапия (выбор АМП, способа введения, длительность курса, нецелесообразность применения). В стационарах субъектов данный показатель составил в порядке убывания: 49,8% для Самарской области, 49,5% в Республике Марий-Эл, на Сахалине 42,7%, в Амурской области 42,3%, в Нижегородской области 39,9%, в Удмуртии 38,6% и 11,6% в ГБУЗ «Морозовская ДГКБ ДЗМ».
Проведен анализ клинической практики фармакотерапии в разрезе отделений стационаров инфекционных (n = 829) и соматических (n = 548) по каждому раздельно. Как представлено на рисунке 5, показатель «Причинение необоснованной боли (избыточные манипуляции, анализы, способ введения лекарственных препаратов)» за 2020–2021 гг. по результатам оценки чек-листов в инфекционных отделениях составил 56,17%, в соматических – 24,96%. Частота выявления показателя «Полипрагмазия (два и более лекарственных препаратов без доказательной базы их применения при данном заболевании)» в инфекционных отделениях – 69%, в соматических – 29,33%. Удельный вес показателя «Несоответствие лечения диагнозу (по основному)» составил в инфекционных отделениях 58,18%, в соматических – 28,12%.
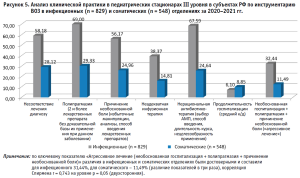
Удельный вес наиболее значимого показателя «Нерациональная антибиотикотерапия (выбор АМП, способ введения, длительность курса, нецелесообразность применения)» был в 2,5 раза выше в инфекционных отделениях и составил 67,59%, по сравнению с аналогичным показателем в соматических отделениях – 24,64%. Удельный вес показателя «Неадекватная инфузионная терапия» в инфекционных отделениях был выше в 2,5 раза и составил 38,37%, в соматических – 14,81%. Удельный вес показателя «Продолжительность госпитализации (средний к/д)» в инфекционных отделениях был короче и составил 6,1 койко-день, в соматических – 8,85 койко-дней.
Получены достоверные различия по ключевому показателю: «Агрессивное лечение (необоснованная госпитализация + полипрагмазия + причинение необоснованной боли)»: в инфекционных отделениях показатель был в три раза выше и составил 31,44% медицинских карт пациентов по сравнению с соматическими отделениями – 11,49% (корреляция Спирмена r = 0,743 на уровне p = 0,05 двухсторонняя).
По данным оценки первичной документации, ключевой показатель «Необоснованная госпитализация + полипрагмазия + причинение необоснованной боли («агрессивное лечение»)» за 2020–2021 гг. в стационаре ГБУЗ «Морозовская ДГКБ» г. Москва составил «0».
Обсуждение результатов
Ранее нами было показано, что существующая категоризация по версии WHO2019 метода AWaRe имеет ограничения при оценке рациональности потребления АМП в многопрофильных детских стационарах субъектов РФ. Так, в категорию «Доступа» входят аминогликозиды и парентеральные цефалоспорины первого поколения, в категорию «Контроля» включены антисинегнойные цефалоспорины, что не соответствует клинической практике назначения АМП первой и второй линии на основе отечественных клинических рекомендаций в России 2019–2021 гг.: «Острый бронхит», «Инфекция мочевых путей у детей», «Острый тонзиллит и фарингит (Острый тонзиллофарингит)», «Острый средний отит», «Острый синусит», «Пневмония (внебольничная)». Выявленные ограничения категоризации по версии WHO2019, которые объясняются особенностями структуры детского многопрофильного стационара для детей в странах-участниках ВОЗ, где профиль «неонатология» обязательно включается в оценку. По версии WHO2019 категоризации метода AWaRe аминогликозиды и цефалоспорины, имеющие исключительно парентеральные лекарственные формы, решением экспертов ВОЗ, были включены в категорию «Доступа» («Access», зеленый), что является приемлемым для профиля «неонатология», однако не может считаться рациональным при применении категоризации по профилю «педиатрия»3,6,8,11 [3,6,8,11]. Выявленное ограничение категоризации WHO2019 метода AWaRe не вполне подходит для оценки рациональности потребления АМП у детей по профилю «педиатрия» в России, что создает основания для оптимизации категоризации метода AWaRe по версии на основе отечественных клинических рекомендаций.
Изменение соотношения категорий потребляемых АМП при переходе от категоризации по версии WHO2019 к версии на основе отечественных клинических рекомендаций 2019–2021 гг. позволяет улучшить точность характеристики рациональности клинической практики использования АМП в многопрофильных стационарах для детей в соответствии с надлежащей клинической практикой на основе клинических рекомендаций по профилю «педиатрия» в России.
На примере увеличения удельного веса категории «Резерва» с 0,88% до 6,67% при переходе от категоризации по версии WHO2019 к версии на основе отечественных клинических рекомендаций 2019– 2021 гг., по данным потребления АМП во флагманских стационарах из девяти субъектов РФ, были выявлены значительные различия в клинической практике потребления антибиотиков по профилю «педиатрия» для одинаковых нозологий. В двух из девяти субъектов, согласно полученным данным, для госпитализированных детей по профилю «педиатрия» аминогликозиды были самыми часто потребляемыми антибиотиками в 2021 г.: каждый второй ребенок в Амурской области и каждый пятый в Сахалинской области получал аминогликозиды, что нерационально и не соответствует клиническим рекомендациям 2019–2021 гг. Данные об избыточной практике применения аминогликозидов в Амурской и Сахалинской области были подтверждены при оценке клинической практики по вопроснику инструментария ВОЗ «на месте» при оценке первичной медицинской документации.
По данным оценки на основе первичной медицинской документации «на местах», выявлены значительные различия в клинической практике в зависимости от того, в какое профильное отделение госпитализировали детей в многопрофильном детском стационаре. Так, в инфекционных отделениях, по сравнению с соматическими отделениями, в 2,5 раза выше удельный вес показателей «Нерациональная антибиотикотерапия (выбор АМП, способ введения, длительность курса, нецелесообразность применения)» и «Неадекватная инфузионная терапия». Ключевой показатель «Агрессивное лечение (необоснованная госпитализация + полипрагмазия + причинение необоснованной боли)» в инфекционных отделениях выявлялся в три раза чаще, чем в соматических отделениях и составил для инфекционного 31,44%, для соматического – 11,49% (корреляция Спирмена r = 0,743, p = 0,05, двухсторонняя).
Выводы
Впервые получен опыт внедрения нового клинико-фармакологического инструмента – метода AWaRe, предложенного ВОЗ в 2017 г. для взрослых и адаптированного в 2019 г. для детей. К сожалению, по результатам оценки потребления АМП в некоторых субъектах России в настоящем исследовании в 2021 г. основной показатель оценочной категории «Доступа» («Access», зеленый) для антибиотиков, предписанный ВОЗ, не достиг целевых 60% ни в одном из педиатрических стационаров, что указывает на необходимость дальнейших мероприятий по внедрению надлежащих принципов управления антимикробной терапией и динамической оценки в педиатрических стационарах России. Сравнительный анализ возможностей двух принципов категоризации метода AWaRe – традиционной категоризации по версии WHO2019 и предложенной нами версии категоризации метода AWaRe на основе отечественных клинических рекомендаций 2019–2021 гг. (табл.) показал успешный опыт адаптации метода AWaRe для оценки рациональности применения АМП в многопрофильных детских стационарах у детей при применении категоризации на основе отечественных клинических рекомендаций 2019–2021 гг. В настоящем наблюдательном исследовании были выявлены значительные различия в клинической практике на основе оценки рациональности потребления АМП и по данным первичной медицинской документации. В настоящем наблюдательном протоколе представлены данные о рациональности потребления антибиотиков в педиатрических стационарах РФ на основе отечественных клинических рекомендаций, которые можно было бы использовать для организации локальных и национальных профилактических мероприятий, направленных на создание системы управления антимикробной терапией в педиатрии.
Международный опыт внедрения оценки рациональности клинической практики применения АМП по потреблению в 2019 г. в сопоставлении с оценкой точечной распространенности использования антибиотиков для детских стационаров в версии WHO2019 методом AWaRе из 56 стран представлен у 18 305 детей (77,7%) в Европе и Азии. Результаты показали, что потребление антибиотиков категории «Допуска» («Access», зеленый) у детей варьировало от 8% (Китай) до 61% (Словения) всех назначений антибиотиков в стационаре. Использование антибиотиков категории «Контроля» («Watch», желтый) у детей было самым высоким в Иране (77%) и самым низким в Финляндии (10%). Показатель потребления антибиотиков категории «Резерва» («Reserve», красный) было низким во всех странах, лидером в практике применения резервных антибиотиков у детей оказалась Мексика (до 20%) [8,9,11,12]. На основании полученных данных целевые нормативные показатели по ВОЗ определены для категории «Доступа» («Access», зеленый) – 60%, обсуждается соотношение для препаратов категории «Контроля» («Watch», желтый) в интервале до 40% (35–40%) и группы «Резерв» («Reserve», красный) в интервале не более 5% АМП, однако четких нормативных показателей для последних двух категорий в настоящее время ВОЗ не определено [2,5,6].
Сочетание методов оценки потребления АМП и метода точечных обследований распространенности использования антибиотиков у госпитализированных детей «на местах» помогает охарактеризовать клиническую практику, подкрепляя результат данными первичной медицинской документации во время визита в детский стационар, что способствует получению всесторонней информации о том, насколько сложившийся в данной медицинской организации подход к применению АМП на уровне пациента соответствует политике и установочным принципам использования АМП (национальным клиническим руководствам, рекомендациям, протоколам), способствует ли достижению клинически значимых результатов, включая оценку клинической эффективности и длительности пребывания в стационаре [12,13]. Дальнейшая работа должна быть сосредоточена на оптимизации и корректировке критериев для метода AWaRе и направлена на оптимизацию перечней АМП в соответствии с конкретными условиями целевой выборки, включая нозологию и возраст детей.
При анализе первичной документации «на местах» нами был выявлен более агрессивный подход к выбору тактики фармакотерапии и более частая практика нерационального применения АМП в инфекционных отделениях многопрофильных детских стационаров, по сравнению с соматическими отделениями у детей, госпитализированных в 2020–2021 гг. по профилю «педиатрия» по поводу одинаковых нозологических форм заболеваний в семи субъектах РФ.
_______________________________________________________________________
Выражение признательности
Авторы выражают слова признательности коллективам сотрудников, предоставившим данные в рамках проекта и участвовавшим в проведении выездных мероприятий: ГАУЗ АО «Амурская областная детская клиническая больница» (главный врач – Белоус Руслан Алексеевич), АОГБУЗ «Чукотская окружная больница» (главный врач – Острась Марина Алексеевна), ГБУЗ «Областная детская больница» (г. Южно-Сахалинск) (главный врач – Фатеева Лариса Юрьевна), ГБУЗ НО «Нижегородская областная детская клиническая больница» (главный врач – Кондратьева Инна Юрьевна), БУЗ УР «Республиканская детская клиническая больница МЗ УР» (главный врач – Пупков Павел Витальевич), ГБУ Республики Марий Эл «Детская республиканская клиническая больница» (главный врач – Груздев Дмитрий Владимирович), ГБУЗ РХ «Республиканская детская клиническая больница» (главный врач – Кузнецова Татьяна Алексеевна).
- Pakyz A.L., Gurgle H.E., Ibrahim O.M., Oinonen M.J. & Polk R.E. Trends in antibacterial use in hospitalized pediatric patients in United States academic health centers. Infect Control Hosp Epidemiol. 2009 Jun; 30(6): 600-3. doi: 10.1086/597545.
- D’Amore C. [et al.] Use of multiple metrics to assess antibiotic use in Italian children’s hospitals. Sci Rep. 2021 Feb 11; 11(1): 3543. doi: 10.1038/s41598-021-83026-1.
- Sharland M. [et al.] Classifying antibiotics in the WHO Essential Medicines List for optimal use-be AWaRe. Lancet Infect Dis. 2018 Jan; 18(1): 18–20. doi: 10.1016/S1473-3099(17)30724-7.
- Gharbi M. [et al.] Using a simple point-prevalence survey to define appropriate antibiotic prescribing in hospitalised children across the UK. BMJ Open. 2016 Nov 3;6(11):e012675. doi: 10.1136/bmjopen-2016-012675.
- Bergman U. [et al.] Drug utilization 90% – a simple method for assessing the quality of drug prescribing. Eur J Clin Pharmacol. 1998 Apr; 54(2): 113-8. doi: 10.1007/s002280050431.
- Review of antibiotics in national medicines selection listsin eastern Europe and central Asia / World Health Organization: European Region. – URL: https://apps.who.int/iris/bitstream/handle/10665/365989/9789289058582-eng.pdf.
- World Health Organization. Global action plan on antimicrobial resistance. (2015).
- World Health Organization. The 2019 WHO AWaRe classification of antibiotics for evaluation and monitoring of use. in The 2019 WHO AWaRe classification of antibiotics for evaluation and monitoring of use (2019).
- Bakaki P.M. [et al.] Defining pediatric polypharmacy: a scoping review. PLoS One. 2018 Nov 29;13(11):e0208047. doi: 10.1371/journal.pone.0208047. eCollection 2018.
- Berrington A. Antimicrobial prescribing in hospitals: be careful what you measure. J Antimicrob Chemother. 2010 Jan; 65(1): 163-8. doi: 10.1093/jac/dkp399.
- Polk R., Letcavage J., Mahoney A. & MacDougall C. Measurement of adult antibacterial drug use in 130 US hospitals: comparison of defined daily dose and days of therapy. Clin Infect Dis. 2007 Mar 1; 44(5): 664-70. doi: 10.1086/511640.
- World Health Organization. WHO Advisory Group on Integrated Surveillance of Antimicrobial Resistance (AGISAR): report of the 7th meeting, 17-20 October 2016, Raleigh, United States of America. (2018).
- Versporten A. [et al.] The Worldwide Antibiotic Resistance and Prescribing in European Children (ARPEC) point prevalence survey: developing hospital-quality indicators of antibiotic prescribing for children. J Antimicrob Chemother. 2016 Apr; 71(4): 1106-17. doi: 10.1093/jac/dkv418.
