MEDICAL DEVICES
Features of the supply of medical devices within the framework of Federal Law No. 44-FZ. Problematic situations in the execution of the contract and ways to solve them
1 — FSBI «Russian Scientific and Research Institute for Medical Engineering» of Roszdravnadzor, 24, bld. 16, Kashirskoye highway, Moscow, 115478, Russian Federation.
2 — FSBI «Russian Scientific and Research Institute for Medical Engineering» of Roszdravnadzor, 24, bld. 16, Kashirskoye highway, Moscow, 115478, Russian Federation.
The article provides a legal analysis of the features of the supply of medical devices to medical organizations. The main regulatory legal acts that the customer is obliged to follow when purchasing medical devices are specified. Some problematic situations that arise during the execution of a contract for the supply of medical devices are considered, as well as recommendations for solving and preventing problematic situations during the execution of the contract are proposed.
Keywords: delivery of medical devices, customer, supplier, standard contract, purchase documentation, technical requirements
Background.
Поставка медицинских изделий является достаточно сложным процессом как для заказчика, так и для поставщика. Заказчик обязан правильно оформить документацию о закупке, организовать проведение закупочной процедуры, надлежащим образом принять и совместно с поставщиком ввести в эксплуатацию поставленное медицинское изделие. Как показывает правоприменительная практика в отношении поставок медицинских изделий, которая также не является однородной, не все участники процесса успешно справляются с поставленной задачей.
Так как полноценный правовой анализ процедуры поставки медицинских изделий в объеме небольшой публикации провести невозможно, в этой работе будут рассмотрены только основные аспекты поставки медицинских изделий в медицинские организации, а также несколько проблемных моментов, с которыми сталкиваются заказчики при исполнении контрактов, и предложены пути их решения.
Возникновение и стремительное распространение новой коронавирусной инфекции COVID-19 поставило перед специалистами здравоохранения задачи, связанные с быстрой диагностикой вируса и оказанием медицинской помощи пострадавшим от инфекции пациентам. В настоящее время продолжается интенсивное изучение клинических и эпидемиологических особенностей заболевания, разработка новых средств его профилактики и лечения. Вместе с тем с российского здравоохранения не снималась важнейшая задача по оказанию медицинских услуг пациентам по неотложным и плановым показаниям в связи с другими заболеваниями. Поэтому в настоящее время в разы выросла потребность в обеспечении отечественного здравоохранения качественными, эффективными и безопасными медицинскими изделиями в минимальные сроки.
Инструментом для реализации этой важной государственной задачи являются поставки медицинских изделий, реализуемые в рамках процедур, установленных Федеральным законом от 05.04.2013 № 44-ФЗ «О контрактной системе в сфере закупок товаров, работ, услуг для обеспечения государственных и муниципальных нужд»1 (далее – Закон о контрактной системе).
Основные нормативные правовые акты Российской Федерации, регулирующие правила поставки медицинских изделий
В соответствии с частью 11 статьи 34 Закона о контрактной системе и Правилами разработки типовых контрактов, типовых условий контрактов, утвержденными Постановлением Правительства Российской Федерации от 02.07.2014 № 606 «О порядке разработки типовых контрактов, типовых условий контрактов, а также о случаях и условиях их применения»2, Министерством здравоохранения Российской Федерации издан приказ от 15.10.2015 № 724н (ред. от 19.08.2020) «Об утверждении типового контракта на поставку медицинских изделий, ввод в эксплуатацию медицинских изделий, обучение правилам эксплуатации специалистов, эксплуатирующих медицинские изделия, и специалистов, осуществляющих техническое обслуживание медицинских изделий», (далее – Типовой контракт).
Типовой контракт состоит непосредственно из самого Типового контракта, а также следующих приложений к нему:
- приложение 1. Спецификация;
- приложение 2. Технические требования;
- приложение 3. Отгрузочная разнарядка (План распределения);
- приложение 4. Акт приема-передачи Оборудования;
- приложение 5. Акт ввода Оборудования в эксплуатацию, оказанию Услуг по обучению и инструктажу специалистов;
- приложение 6. Сводный реестр товарных накладных на поставку Оборудования;
- приложение 7. Акт сверки расчетов;
- приложение 8. Акт об исполнении обязательств по Контракту.
При этом следует обратить внимание, что приложения 3, 6 и 8 включаются в Типовой контракт в случае, если поставка осуществляется в пользу третьих лиц при централизованной закупке или по нескольким местам доставки.
Также в связи с необходимостью закупок медицинских изделий у общества с ограниченной ответственностью «Стентекс», Минздравом России издан Приказ от 21.12.2016 № 982н «Об утверждении типового контракта на поставку стентов для коронарных артерий металлических непокрытых, стентов для коронарных артерий, выделяющих лекарственное средство (с нерассасывающимся полимерным покрытием), катетеров баллонных стандартных для коронарной ангиопластики, катетеров аспирационных для эмболоэктомии (тромбэктомии), заключаемого единственным поставщиком – обществом с ограниченной ответственностью «Стентекс» и федеральными государственными бюджетными учреждениями и государственными бюджетными учреждениями субъектов Российской Федерации, и информационной карты указанного типового контракта». Определение медицинского изделия содержится в статье 38 Федерального закона от 21.11.2011 № 323-ФЗ (ред. от 30.04.2021) «Об основах охраны здоровья граждан в Российской Федерации». Обязательным требованием предложения того или иного медицинского изделия к поставке является условие, что на территории Российской Федерации разрешается обращение медицинских изделий, зарегистрированных в порядке, установленном Правительством Российской Федерации, уполномоченным им федеральным органом исполнительной власти. Регистрация медицинских изделий осуществляется в соответствии с Постановлением Правительства РФ от 27.12.2012 № 1416 (ред. от 24.11.2020) «Об утверждении Правил государственной регистрации медицинских изделий». Зарегистрированные медицинские изделия должны быть включены в реестр медицинских изделий3.
Заказчику при формировании лотов на поставку медицинских изделий необходимо учитывать требования и ограничения, установленные:
- Федеральным законом от 26.07.2006 № 135-ФЗ (ред. от 17.02.2021) «О защите конкуренции»;
- Постановлением Правительства РФ от 15.04.2014 № 341 (ред. от 27.07.2019) «О предоставлении преимуществ организациям инвалидов при определении поставщика (подрядчика, исполнителя) в отношении предлагаемых ими цены контракта, суммы цен единиц товара, работы, услуги» (вместе с «Правилами предоставления преимуществ организациям инвалидов при определении поставщика (подрядчика, исполнителя) в отношении предлагаемых ими цены контракта, суммы цен единиц товара, работы, услуги») (далее – Постановление № 341);
- Постановлением Правительства РФ от 05.02.2015 № 102 (ред. от 06.03.2021) «Об ограничениях и условиях допуска отдельных видов медицинских изделий, происходящих из иностранных государств, для целей осуществления закупок для обеспечения государственных и муниципальных нужд» (далее – Постановление № 102);
- Приказом Минфина России от 04.06.2018 № 126н (ред. от 10.07.2020) «Об условиях допуска товаров, происходящих из иностранного государства или группы иностранных государств, для целей осуществления закупок товаров для обеспечения государственных и муниципальных нужд» (зарегистрировано в Минюсте России 24.10.2018 № 52516) (с изм. и доп., вступ. в силу с 01.10.2020) (далее – приказ № 126н).
Правила формирования лота и описания медицинских изделий в документации на закупку
Все медицинские изделия при формировании лотов на закупку условно можно разделить на несколько групп (каждую группу необходимо закупать отдельно):
1) медицинские изделия, не указанные в перечнях Постановлений № 341, № 102 и № 126н;
2) медицинские изделия, указанные в Постановлении № 341;
3) медицинские изделия, указанные в Перечне № 1 Постановления № 102 (для обеспечения государственных и муниципальных нужд);
4) медицинские изделия, указанные в Перечне № 2 Постановления № 102 (для обеспечения государственных и муниципальных нужд);
5) медицинские изделия, указанные в двух перечнях Постановления № 102 (для обеспечения государственных и муниципальных нужд): например, устройства для переливания крови, кровезаменителей и инфузионных растворов, контейнеры для заготовки, хранения и транспортировки крови и ее компонентов.
6) медицинские изделия, указанные в Постановлении № 341 и в Перечне № 2 Постановления № 102 (для обеспечения государственных и муниципальных нужд): например, расходные материалы для аппаратов искусственного кровообращения, расходные материалы для ИВЛ.
7) медицинские изделия, указанные в Приказе № 126н.
ПРИМЕР нарушения заказчиком требований о разделении лотов на поставку медицинских изделий
Решение УФАС по г. Москва от 21.11.2018 по делу № 2-57-14399/77-18 (0373200583118000126)
«Комиссией Управления установлено, что наряду с поставкой медицинский изделий, относящихся к коду ОКПД2 32.50.12.000: «Стерилизаторы хирургические или лабораторные», включенных в приложение к Приказу Минфина России № 126н, Заказчику необходимы также к поставке товары с кодами ОКПД2 20.59.52.199: «Реагенты сложные диагностические или лабораторные прочие, не включенные в другие группировки»; 20.59.52.192 «Индикаторы», которые не включены в приложении к Приказу Минфина России №126н. Таким образом, Комиссия Управления приходит к выводу об обоснованности данных доводов жалобы и нарушении Заказчиком п. 1 ч. 1 ст. 33 Закона о контрактной системе».
Описание объекта закупки должно отвечать следующим требованиям:
1) основываться на правилах нормирования (если требования установлены);
2) соответствовать каталогу товаров, работ, услуг (ТРУ);
3) учитывать требования антимонопольного законодательства;
4) соответствовать Закону о контрактной системе;
5) учитывать требования законодательства о техническом регулировании;
6) учитывать требования законодательства об энергосбережении и о повышении энергетической эффективности;
7) учитывать пожелания Заказчика4.
Заказчик обязан соблюдать все правила описания объекта закупки.
Также заказчику необходимо определить необходимость применения при описании медицинских изделий требований технических регламентов, принятых в соответствии с законодательством Российской Федерации о техническом регулировании, документов, разрабатываемых и применяемых в национальной системе стандартизации, принятых в соответствии с законодательством Российской Федерации о стандартизации.
Перечисление в документации о закупке большого количества ГОСТов, а также фраза «объект закупки должен соответствовать действующим ГОСТ, СанПин и пр.» не является надлежащим описанием, что подтверждается Определением Верховного суда Российской Федерации от 01.02.2016 №№ 301-КГ15-18555, А17-394/ 2015:
«…пункт 3.2.2 устанавливает требования к объекту закупки путем приложения к документации нормативных (технических) документов (ГОСТов), что возлагает на участников аукциона функции по самостоятельному выбору необходимых характеристик и показателей объекта закупки, соответствующих данным нормативным документам. При этом достаточных доказательств необходимости таких требований не представлено. Учитывая, что аукционная документация не основана на объективных потребностях заказчика, суд признал ее не соответствующей требованиям».
Заказчику следует неукоснительно следовать следующему правилу: конкретно указывать в документации о закупке именно те ГОСТы, которые непосредственно относятся к объекту закупки и использовать при описании объекта закупки только действующие технические регламенты и ГОСТы.
В целях соблюдения требований ст. 33 Закона о контрактной системе, заказчики, осуществляющие закупку по правилам данного закона, при описании объекта закупки обязаны таким образом определить требования к закупаемым товарам, работам, услугам, чтобы, с одной стороны, повысить шансы на приобретение товара именно с теми характеристиками, которые соответствуют их потребностям, а с другой – необоснованно не ограничить количество участников закупки. Таким образом, в целях соблюдения антимонопольного законодательства, технические характеристики поставляемых медицинских изделий, указанные заказчиком, должны соответствовать как минимум 2–3 производителям медицинских изделий. При этом заказчику необходимо учитывать, что он не вправе устанавливать требования к химическому составу и (или) компонентам товара, и (или) к показателям технологии производства, к испытанию товара, и (или) к показателям, значения которых становятся известными при испытании определенной партии продукции после его производства.
Данное утверждение подтверждается Решением Верховного суда РФ от 09.02.2017 № АКПИ16-1287 «Об отказе в удовлетворении заявления о признании недействующим пункта 3 письма Федеральной антимонопольной службы от 1 июля 2016 г. № ИА/44536/16 “Об установлении заказчиком требований к составу, инструкции по заполнению заявки на участие в закупке”»:
«При установлении заказчиком в документации, извещении о закупке требований к описанию участниками закупки товаров следует учесть, что Закон о контрактной системе не обязывает участника закупки иметь в наличии товар в момент подачи заявки, в связи с чем требования заказчика подробно описать в заявке (путем предоставления показателей и (или) их значений, как в виде одного значения, диапазона значений, так и сохранения неизменного значения) химический состав и (или) компоненты товара, и (или) показатели технологии производства, испытания товара, и (или) показатели, значения которых становятся известными при испытании определенной партии товара после его производства, имеют признаки ограничения доступа к участию в закупке».
Исполнение контракта по поставке медицинских изделий
В целях успешного исполнения заключенного контракта, заказчику целесообразно включить в пункт 3 контракта «Взаимодействие сторон» подпункт о контактных лицах, как со стороны заказчика, так и со стороны поставщика. Включение данного подпункта в контракт на поставку медицинских изделий позволит сторонам организовать эффективное взаимодействие и оперативно решать возникающие в ходе исполнения контракта вопросы. На практике срок поставки медицинских изделий часто указывается в календарных днях с момента заключения контракта. Если поставка выполняется в соответствии с планом распределения, и (или) контрактом предусмотрены этапы, то возможна ситуация, когда стороны могут допустить ошибку в определении даты поставки медицинских изделий. В целях неукоснительного соблюдения сроков поставки медицинских изделий по контракту заказчику после заключения контракта с поставщиком целесообразно самостоятельно произвести расчет с определением конкретной даты поставки по контракту и направить соответствующее уведомление поставщику.
Также заказчику в ходе исполнения контракта необходимо следовать алгоритму, представленному в таблице 1.

Техническая и (или) эксплуатационная документация поставщика (производителя) при поставке медицинских изделий по контракту
В соответствии с подпунктом «б» пункта 5.3 Типового контракта, поставщик предоставляет заказчику «техническую и (или) эксплуатационную документацию производителя (изготовителя) Оборудования на русском языке». Вместе с тем, отсутствие в Типовом контракте и приложении № 2 к Типовому контракту «Технические требования» конкретного перечня документации к медицинскому изделию дает возможность поставщику самостоятельно определять перечень предоставляемой документации, что, по нашему мнению, не является правильным. Заказчику после приемки медицинского изделия и постановки его на баланс предстоит эксплуатировать поставленное медицинское изделие, от правильной эксплуатации которого будет зависеть не только здоровье, но и жизнь пациентов. Представленная в полном объеме техническая и (или) эксплуатационная документация на медицинское изделие в вопросе безопасной и эффективной эксплуатации имеет очень важное значение. Однако совершенно резонно возникает вопрос, почему в Типовом контракте используется такая формулировка: «техническая и (или) эксплуатационная документация»? В законодательстве Российской Федерации используется термин «техническая документация». Данное понятие содержится в статье 743 Гражданского кодекса Российской Федерации (ГК РФ): «Техническая документация и смета» и используется исключительно по отношению к договору строительного подряда. В соответствии с пунктом 1 статьи 743 ГК РФ «Подрядчик обязан осуществлять строительство и связанные с ним работы в соответствии с технической документацией, определяющей объем, содержание работ и другие предъявляемые к ним требования, и со сметой, определяющей цену работ». Так как поставка медицинского изделия по Типовому контракту совершенно очевидно не имеет никакого отношения к договору строительного подряда, то и понятие «техническая документация» в контексте статьи 743 ГК РФ не может быть применимо к Типовому контракту. Обоснованно возникает вопрос – тогда какое отношение имеет «техническая документация» к медицинским изделиям? Попробуем разобраться в этом вопросе. Техническое оснащение современных медицинских организаций в наше время характеризуется большим разнообразием: от самых простых изделий до сложнейших инженерных комплексов (например, медицинские кислородные станции, баллоны и другие системы, работающие под давлением). В соответствии с приложением 8 к Федеральным нормам и правилам в области промышленной безопасности «Правила промышленной безопасности опасных производственных объектов, на которых используется оборудование, работающее под избыточным давлением», утвержденным Приказом Ростехнадзора от 25.03.2014 № 116 (далее – ФНП № 116), установлен перечень «эксплуатационной документации».
Рассмотрим другой документ, также устанавливающий требования к безопасности аналогичного оборудования. В соответствии с Техническим регламентом Таможенного союза «О безопасности оборудования, работающего под избыточным давлением» (далее – ТР ТС 032/2013) при изготовлении (производстве) оборудования и устройств безопасности изготовителем обеспечивается их соответствие параметрам и характеристикам, установленным проектной документацией, и требованиям настоящего технического регламента. Изготовитель проводит испытания оборудования, предусмотренные проектной документацией. Отклонения от проектной документации при изготовлении (производстве) оборудования согласовываются с разработчиком (проектировщиком). Оборудование должно быть безопасным в течение всего срока службы при выполнении потребителем мер по обеспечению его безопасности, установленных в «технической документации». Техническая документация, прилагаемая к оборудованию, включает:
а) паспорт оборудования;
б) копию обоснования безопасности;
в) чертеж общего вида;
г) паспорта предохранительных устройств (при их наличии в соответствии с проектной документацией);
д) расчет пропускной способности предохранительных устройств (при их наличии в соответствии с проектной документацией);
е) расчет на прочность оборудования;
ж) руководство(инструкцию) поэксплуатации;
з) чертежи, схемы, расчеты и другую документацию в соответствии с договором поставки (контракта).
Паспорт оборудования является основным документом для идентификации оборудования. Наличие паспорта оборудования обязательно для обращения оборудования на таможенной территории Таможенного союза на всех стадиях жизненного цикла. Паспорт оборудования оформляется изготовителем, который проставляет на паспорте печать и указывает дату его оформления. Обоснование безопасности оборудования готовится на этапе разработки (проектирования) оборудования.
В обосновании безопасности приводятся анализ рисков для оборудования, а также минимально необходимые меры по обеспечению безопасности. Оригинал обоснования безопасности оборудования хранится у разработчика (проектировщика), а копия – у изготовителя оборудования и организации, эксплуатирующей оборудование. Таким образом, мы имеем два действующих документа на территории Российской Федерации, которые имеют одинаковую сферу правового регулирования, но используют разную терминологию. В первом документе – эксплуатационная документация, а во втором – техническая документация.
Но не будем забывать, что оборудование, работающее под давлением, это всего лишь одна из многих номенклатур, поставляемых в медицинские организации. Поэтому при поставке медицинских изделий, за исключением оборудования, работающего под давлением, заказчику и поставщику необходимо руководствоваться ГОСТ Р 2.601-2019 «Единая система конструкторской документации (ЕСКД). Эксплуатационные документы».
В соответствии с пунктом 3.1.1 ГОСТ Р 2.601-2019, эксплуатационный документ – это конструкторский документ, который в отдельности или в совокупности с другими документами определяет правила эксплуатации продукции и (или) отражает сведения, удостоверяющие гарантированные изготовителем значения основных параметров и характеристик (свойств) продукции, а также гарантии и сведения по ее эксплуатации в течение установленного срока службы.
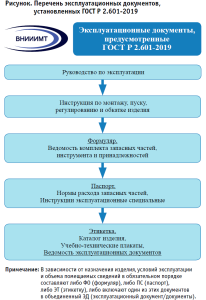
Перечень эксплуатационных документов, установленных ГОСТ Р 2.601-2019, приведен ниже (см. рисунок). При этом ГОСТ Р 2.601-2019 содержит перечень обязательных эксплуатационных документов (формуляр, паспорт, этикетка, ведомость эксплуатационных документов), а также документов, необходимость разработки которых устанавливает производитель (разработчик) медицинского изделия. На основании изложенного, в целях исключения разного толкования у сторон контракта (какой перечень технической или эксплуатационной документации необходимо представить поставщику), заказчику целесообразно указать в контракте нормативный акт: соответствующий ГОСТ или Технический регламент, которым будет обязан руководствоваться поставщик при представлении документации заказчику. В идеальном варианте заказчик имеет право указать (например, в приложении 2 к контракту «Технические требования») перечень необходимых ему технических или эксплуатационных документов на поставляемое медицинское изделие.
Также анализ практики исполнения контрактов показывает, что у заказчика и поставщика возникают разногласия в отношении формы представляемых технических или эксплуатационных документов. В Типовом контракте отсутствуют требования о том, что документы должны предоставляться именно на бумажных носителях. Заказчик, получая документы от поставщика на электронных носителях, не знает, как аргументировать законность своих требований о предоставлении поставщиком документов на бумажных носителях. В соответствии с пунктом 11.1 статьи 2 Федерального закона от 27.07.2006 № 149-ФЗ «Об информации, информационных технологиях и о защите информации» под электронным документом понимается документированная информация, представленная в электронной форме, то есть в виде, пригодном для восприятия человеком с использованием электронных вычислительных машин, а также для передачи по информационно-телекоммуникационным сетям или обработки в информационных системах.
В пункте 1 постановления Пленума Верховного Суда РФ от 26.12.2017 № 57 «О некоторых вопросах применения законодательства, регулирующего использование документов в электронном виде в деятельности судов общей юрисдикции и арбитражных судов» дается следующее определение данного понятия: «электронный документ – документ, созданный в электронной форме без предварительного документирования на бумажном носителе, подписанный электронной подписью в порядке, установленном законодательством РФ».
Согласно пункту 1.6.1 Регламента удостоверяющего центра Евразийской экономической комиссии5 под электронным документом понимается документ в электронном виде, заверенный электронной цифровой подписью и отвечающий требованиям общей инфраструктуры документирования информации в электронном виде.
Следовательно, можно выделить следующие основные признаки электронного документа:
- электронная форма;
- соблюдение требований документирования информации;
- заверение информации электронной цифровой подписью.
Таким образом, у заказчика есть совершенно законные основания в отказе принятия технической или эксплуатационной документации, исполненной поставщиком в электронной форме, но без соблюдения требований документирования информации и/или без заверения информации электронной цифровой подписью. Наилучший вариант, который исключает двойственное толкование заказчиком и поставщиком формы исполнения данного обязательства, это указание в контракте, в какой форме необходимо поставщику предоставить техническую или эксплуатационную документацию – бумажной или электронной.
Условия включения участника закупки в Реестр недобросовестных поставщиков
Еще одним проблемным аспектом исполнения контракта для многих заказчиков является ситуация, когда поставщик допускает существенные нарушения условий контракта, но заказчик, в силу незнания процедуры, не может выполнить необходимые действия для внесения поставщика в реестр недобросовестных поставщиков (далее – РНП). Непринятие должных мер к недобросовестным поставщикам, в том числе и невключение их в РНП, приводит к тому, что на рынке поставок медицинских изделий продолжают работать недобросовестные поставщики, а данное обстоятельство, безусловно, может отрицательно влиять на качество и безопасность поставляемых медицинских изделий.
Вместе с тем положениями части 8, 9 статьи 95 Закона о контрактной системе установлено право заказчика на расторжение контракта в одностороннем порядке по основаниям, предусмотренным ГК РФ. При этом принятие решения допускается исключительно в связи с существенным нарушением условий контракта. То есть по основаниям, предусмотренным ГК РФ для одностороннего отказа от исполнения отдельных видов обязательств, при условии, если это было предусмотрено контрактом:
- существенное нарушение поставщиком требований к качеству товара, а именно обнаружение заказчиком неустранимых недостатков, недостатков, которые не могут быть устранены без несоразмерных расходов или затрат времени, или выявляются неоднократно, либо проявляются вновь после их устранения, и других подобных недостатков (пункт 2 статьи 475 ГК РФ);
- невыполнение поставщиком в разумный срок требования заказчика о доукомплектовании товара (пункт 1 статьи 480 ГК РФ);
- неоднократное нарушение поставщиком сроков поставки товаров (пункт 2 статьи 523 ГК РФ).
Документами, подтверждающими обоснование причин одностороннего отказа заказчика от исполнения контракта, являются, например, заключения экспертизы, акты приемки, составленные с участием поставщика (подрядчика, исполнителя), товаросопроводительные документы, решения/предписания контролирующих органов власти, претензионная переписка и другие документы, фиксирующие факты неисполнения/ненадлежащего исполнения обязательств по контракту.
При рассмотрении вопроса о включении (невключении) сведений о поставщике (подрядчике, исполнителе) в РНП в связи с принятием заказчиком решения об одностороннем отказе от исполнения контракта, такие лица также вправе представлять документы, свидетельствующие о надлежащем исполнении своих обязательств по контракту.
Также необходимо отметить, что при отсутствии основания для расторжения контракта (неисполнение/ненадлежащее исполнение обязательств по контракту) сведения о поставщике (подрядчике, исполнителе) не подлежат включению в РНП, а действия заказчика, принявшего решение об одностороннем отказе от исполнения контракта в нарушение положений части 8, 9 статьи 95 Закона о контрактной системе, содержат признаки состава административного правонарушения, предусмотренного частью 6 статьи 7.32 КоАП РФ. Типовые ситуации, когда заказчик имеет все законные основания инициировать процедуру включения поставщика в РНП, указаны в схеме, являющейся приложением к письму ФАС России от 12.03.2019 № ИА/18794/19 (табл. 2)

Заключение и выводы
В заключении необходимо отметить, что любой раздел контракта может содержать и иные положения, не указанные в Типовом контракте, зависящие от характера обязательств по контракту. Данные положения не должны противоречить законодательству Российской Федерации и иным положениям контракта и учитывать специфику закупки. Таким образом, в качестве рекомендации можно предложить заказчикам вдумчиво и нешаблонно подходить к процедуре поставки медицинских изделий, а на стадии формирования документации о закупке профессионально отнестись к разработке технических требований, предъявляемых к планируемым к поставке медицинским изделиям.
_______________________________________________________________________
1 Собрание законодательства Российской Федерации, 2013, № 14, ст. 1652; 2014, № 23, ст. 2925; № 49, ст. 6925; № 52, ст. 6961; 2015; № 1, ст. 51, ст. 72; № 10, ст. 1418; № 14, ст. 2022; № 27, ст. 4001; № 29, ст. 4342, 4346, 4352, 4353, 4375.
2 Собрание законодательства Российской Федерации, 2014, № 28, ст. 4053; 2015, № 1, ст. 279.
3 URL: http://www. roszdravnadzor. ru/services/misearch.
4 См. Определение Верховного суда РФ от 21.06.2017 №310-КГ-1939: «Заказчику предоставлены полномочия по самостоятельному определению параметров и характеристик товара, удовлетворяющих его потребностям, которые отражают специфику его деятельности и обеспечивают эффективное расходование бюджетных средств».
5 Приложение к Положению об удостоверяющем центре Евразийской экономической комиссии, утв. решением Коллегии Евразийской экономической комиссии от 09.07.2018 № 110.
