АКТУАЛЬНЫЙ АСПЕКТ
Трансформация рынка медицинских изделий: тренды, решения и перспективы развития
1 — Федеральная служба по надзору в сфере здравоохранения, 109074, Российская Федерация, г. Москва, Славянская площадь, д. 4, стр. 1.; ФГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования» Министерства здравоохранения Российской Федерации, 125993, Российская Федерация, г. Москва, ул. Баррикадная, д. 2/1, стр. 1.
ORCID: https://orcid.org/0000–0002–9142–8808
В последние десятилетия рынок медицинских изделий претерпевает значительные структурные и функциональные изменения, обусловленные технологическими достижениями и изменениями в регуляторной среде. Внедрение инновационных решений и повышение требований к качеству и безопасности продукции являются ключевыми факторами, определяющими перспективы развития данного сегмента.
Ключевые слова: медицинские изделия, доступность и качество медицинских услуг, высокотехнологичная медицинская помощь, технологический суверенитет, индикаторы риска нарушений обязательных требований, Государственный реестр медицинских изделий, маркировка медицинских изделий
Введение
В рамках государственной политики Российской Федерации приоритетными направлениями в социальной сфере являются обеспечение и повышение уровня здоровья населения, а также оптимизация доступности и качества медицинских услуг. Эти задачи требуют комплексного подхода, включающего разработку и реализацию эффективных стратегий в области здравоохранения, направленных на улучшение показателей общественного здоровья, повышение уровня медицинской грамотности населения и обеспечение доступности высокотехнологичной медицинской помощи для всех категорий граждан.
Для решения этих задач требуется скоординированное взаимодействие всех субъектов системы здравоохранения, включая представителей рынка медицинских изделий. В современных реалиях, когда обеспечение высококачественной медицинской помощи, соответствующей высоким стандартам современности и технологического прогресса, является приоритетной задачей, невозможно переоценить роль медицинских изделий в этом процессе.
В последние годы система здравоохранения подверглась значительной трансформации, перейдя к новой парадигме функционирования – «пациентоцентричности» («пациентоориентированности»). Этот концептуальный сдвиг подкрепляется интенсивной интеграцией передовых технологий, направленных на повышение доступности, качества и безопасности медицинской помощи для населения. В рамках данной парадигмы акцент смещается с традиционных моделей, ориентированных на институциональные процессы, на индивидуализированные подходы, учитывающие уникальные потребности и предпочтения каждого пациента.
Стимулирование инновационного развития медицинской отрасли
В соответствии с поручением Президента Российской Федерации В.В. Путина, к 2030 году ожидается увеличение средней продолжительности жизни в стране до 78 лет, а к 2036 году – до 81 года. Достижение этой амбициозной цели предполагает реализацию комплекса инновационных мероприятий в рамках национальных проектов, включая стратегическую инициативу «Новые технологии сбережения здоровья». Данный проект направлен на стимулирование инновационного развития медицинской отрасли, обеспечение технологического суверенитета государства, а также на расширение спектра отечественных разработок в области инновационных медицинских изделий и лекарственных препаратов. Ключевым элементом проекта является создание цифровой платформы для управления здоровьем, что позволит интегрировать передовые технологии в систему здравоохранения и оптимизировать процессы мониторинга и лечения пациентов.
Правительство Российской Федерации и Министерство здравоохранения Российской Федерации активно способствуют модернизации отечественной системы здравоохранения посредством внедрения инновационных и высокотехнологичных медицинских устройств. В рамках этой стратегии за последний год было зарегистрировано значительное количество медицинского оборудования, разработанного российскими производителями, что составляет приблизительно 47% от общего объема зарегистрированных изделий. Данный показатель свидетельствует о существенном прогрессе в области отечественного медицинского приборостроения и подтверждает эффективность государственной политики, направленной на развитие научно-технического потенциала в сфере здравоохранения.
Механизмы стимулирования и поддержки отечественных производителей медицинских изделий
В рамках государственной политики активно внедряются комплексные механизмы стимулирования и поддержки отечественных производителей медицинских изделий. Данные инициативы способствуют устойчивому увеличению доли рынка, занимаемой продукцией отечественного происхождения.
Росздравнадзор совместно с Министерством промышленности и торговли Российской Федерации разработали стратегическую дорожную карту, направленную на удовлетворение потребностей отечественного здравоохранения в критически значимых медицинских изделиях и масштабирование их производства на территории Российской Федерации. Данная дорожная карта охватывает 368 видов медицинских изделий, которые в настоящее время не имеют отечественных аналогов.
Реализация данной инициативы предполагает комплексное решение задач, связанных с импортозамещением и развитием отечественного производства высокотехнологичной медицинской продукции. В рамках проекта планируется не только обеспечить текущие потребности здравоохранения, но и создать условия для устойчивого развития отрасли, включая разработку и внедрение инновационных технологий, а также повышение конкурентоспособности российских медицинских изделий на международном рынке.
Особое внимание в рамках данной инициативы уделяется координации усилий различных ведомств и организаций, задействованных в процессе разработки, производства и внедрения медицинских изделий. Это позволит обеспечить синергетический эффект и повысить эффективность реализации поставленных задач.
В рамках реализации государственной политики поддержки и стимулирования отечественного производства медицинских изделий активно применяется национальный режим в процессе проведения закупочных процедур. Согласно действующим нормативно-правовым актам, в целях обеспечения приоритетного развития внутреннего рынка и повышения конкурентоспособности национальной продукции, установлены запреты и ограничения на допуск иностранных товаров. Данный механизм направлен на создание благоприятных условий для локализации производства, повышения качества медицинских изделий и укрепления экономической независимости в данной сфере.
На сегодняшний день в рамках ограничений находится 3352 вида медицинских изделий. В то же время, работа по расширению применения национального режима при осуществлении государственных закупок медицинских изделий осуществляется непрерывно. В ближайшее время планируется дополнительно распространить действие данного режима на 212 новых видов медицинских изделий. Помимо этого, активно внедряются механизмы совместных закупок и заключения долгосрочных контрактов, что способствует оптимизации затрат и успешной реализации национальных проектов.
Совместные закупки медицинских изделий представляют собой высокоэффективный инструмент управления бюджетными средствами, позволяющий оптимизировать логистические процессы и снизить совокупные затраты. Данная практика также способствует достижению стратегических целей национальных проектов, направленных на улучшение качества медицинской помощи и повышение уровня доступности медицинских услуг для населения.
Таким образом, комплекс мер, включающий расширение применения национального режима, развитие механизмов совместных закупок и заключение долгосрочных контрактов, демонстрирует высокую эффективность в контексте управления государственными закупками медицинских изделий и реализации приоритетных национальных программ в области здравоохранения.
Совместные закупки, осуществляемые с применением унифицированных технических спецификаций, представляют собой стратегически важный инструмент, позволяющий оптимизировать финансовые ресурсы и повысить эффективность закупочной деятельности. Данный подход способствует достижению ряда значимых результатов, включая:
- Снижение затрат на приобретение медицинских изделий, что является ключевым фактором в условиях ограниченности бюджетных средств.
- В некоторых случаях возможность приобретения продукции с улучшенными эксплуатационными характеристиками, что может привести к повышению качества медицинских услуг и продлению гарантийного срока эксплуатации оборудования.
- Минимизацию рисков, связанных с неисполнением контрактных обязательств, благодаря консолидации объемов закупок и усилению переговорной позиции.
Практика совместных закупок активно внедряется как на федеральном уровне, так и в субъектах Российской Федерации, что свидетельствует о признании их эффективности и целесообразности в рамках системы государственного регулирования. Данный механизм позволяет оптимизировать логистические процессы, повысить прозрачность закупочных процедур и обеспечить более высокий уровень контроля за качеством приобретаемой продукции.
В рамках реализации совместных закупок тяжелого медицинского оборудования субъектами Российской Федерации уже проведено 19 комплексных процедур. Эти мероприятия позволили не только достичь рекордных показателей снижения стоимости медицинских изделий, но и значительно улучшить их технические характеристики. Комплексный подход к закупкам, включающий детальный анализ рынка, конкурентное ценообразование и тщательный контроль качества, способствовал достижению данных результатов. Таким образом, субъекты Российской Федерации продемонстрировали высокий уровень профессионализма и эффективности в управлении государственными закупками медицинского оборудования.
В рамках реализации национального проекта «Семья» и федерального проекта «Охрана материнства и детства» было инициировано проведение серии электронных аукционов по закупке пяти категорий медицинских изделий среди субъектов Российской Федерации. Общая сумма заключенных контрактов составила более одного миллиарда рублей. В результате проведения этих аукционов удалось достичь существенного снижения закупочных цен на медицинские изделия, что подтверждается экономией в размере 342,6 миллиона рублей, что составляет 33,4% от первоначальной стоимости лотов (рис. 1).

В контексте реализации федерального проекта «Борьба с онкологическими заболеваниями», инициированного в рамках национальной стратегии здравоохранения, были организованы электронные аукционы для государственных медицинских учреждений. Целью данных мероприятий являлась оптимизация закупочных процедур и повышение экономической эффективности приобретения медицинских изделий.
В результате проведения аукционов были заключены контракты на поставку трех категорий медицинских изделий на общую сумму свыше 8,173 миллиардов рублей. Следует отметить, что достигнутая экономия бюджетных средств составила 3,89 миллиарда рублей, что эквивалентно 47,7% от общей суммы закупок (рис. 2).

Таким образом, реализация данного этапа федерального проекта продемонстрировала высокую степень эффективности применения современных методов управления закупками в сфере здравоохранения, что, в свою очередь, способствовало улучшению качества медицинского обслуживания и повышению уровня медицинской помощи населению.
В рамках реализации федерального проекта «Развитие федеральных медицинских организаций, включая создание и развитие сети национальных медицинских исследовательских центров с целью их оснащения современным медицинским оборудованием» на текущий момент проведено одиннадцать совместных аукционов. Общая сумма заключенных контрактов составила 3,64 млрд рублей. Благодаря оптимизации закупочных процедур и эффективному управлению тендерными процессами достигнута значительная экономия бюджетных средств, составившая 1,37 млрд рублей, что представляет собой процентное соотношение в размере 37,7% (рис. 3). Эти результаты свидетельствуют о высокой эффективности проведенных мероприятий и могут служить основой для дальнейшего совершенствования механизмов государственного заказа в сфере здравоохранения.
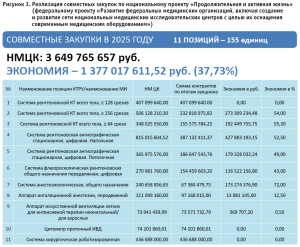
В рамках стратегии повышения операционной эффективности и оптимизации бюджетных расходов было принято стратегически обоснованное решение о консолидации закупочных процессов по 29 категориям медицинских изделий, используемых в рамках реализации федерального проекта «Модернизация первичного звена здравоохранения». Данный подход направлен на снижение совокупных затрат за счет оптимизации логистических цепей.
Планируемые консолидированные закупки предусматривают приобретение более 16 тысяч единиц медицинских изделий для обеспечения потребностей свыше 500 медицинских организаций, расположенных в более чем 50 субъектах Российской Федерации. Это позволит не только обеспечить единообразие материально-технической базы, но и повысить качество медицинского обслуживания за счет стандартизации и унификации используемых изделий.
Согласно государственной стратегии регулирования обращения медицинских изделий, Росздравнадзор осуществляет систематическое совершенствование методологических подходов к данной области, учитывая специфические особенности и динамику жизненного цикла различных медицинских устройств. На текущий момент в реестре зарегистрировано свыше 39 тысяч медицинских изделий, из которых более 15 тысяч являются продукцией отечественного производства, а около 24 тысяч – импортными изделиями. Следует отметить, что в разработке у отечественных производителей находится более 380 наименований инновационных медицинских изделий, включая высокотехнологичное оборудование, функционирующее на основе алгоритмов искусственного интеллекта для анализа больших объемов медицинских данных.
В последние годы в Российской Федерации наблюдается значительное усиление акцента на стратегию импортозамещения и развитие отечественного производства медицинского оборудования. Эта инициатива направлена на достижение технологического суверенитета и обеспечение национальной безопасности в сфере здравоохранения. Доля отечественных медицинских изделий на внутреннем рынке уже достигла существенного уровня, а оснащенность новых поликлиник российским оборудованием составляет порядка 90%.
Для поддержания и дальнейшего расширения существующего парка медицинского оборудования, а также для стимулирования инновационных разработок, в Российской Федерации внедрены и успешно функционируют механизмы ускоренной и упрощенной регистрации медицинских изделий. Эти механизмы включают процедуры внесения изменений в регистрационные досье в случаях выявления дефектов или рисков их возникновения, обусловленных экономическими санкциями.
Правительственные меры, направленные на поддержку отечественных производителей, привели к значительному росту их активности в различных сегментах медицинского производства. Данная положительная тенденция способствует стабилизации рынка медицинских изделий и укреплению системы здравоохранения в целом. В результате, негативное воздействие санкций на отрасль минимизируется, что обеспечивает устойчивое развитие и функционирование сектора медицинских технологий.
Таким образом, комплексный подход к развитию отечественного производства медицинского оборудования, включающий ускоренные процедуры регистрации и государственную поддержку, позволяет Российской Федерации не только достигать технологического суверенитета, но и создавать условия для инновационного роста и повышения конкурентоспособности на международном уровне.
Внедрение инновационных технологий
Для современной системы здравоохранения характерно активное внедрение инновационных технологий, направленных на оптимизацию процессов принятия клинических решений. Одним из таких перспективных направлений является использование искусственного интеллекта (ИИ) в медицинских приложениях. Эти технологии включают в себя широкий спектр решений, таких как системы анализа медицинских изображений, цифровые диагностические платформы, системы мониторинга неотложных состояний и хронических заболеваний, а также алгоритмы прогнозирования осложнений.
Применение ИИ в здравоохранении позволяет существенно повысить качество медицинской помощи, особенно в отдаленных регионах. Системы анализа медицинских изображений обеспечивают высокоточную интерпретацию рентгенографических, магнитно-резонансных и других визуализационных данных, что способствует своевременной постановке диагнозов экспертного уровня и выбору оптимальных схем лечения. Цифровые диагностические платформы, интегрирующие данные из различных источников, позволяют создавать комплексные профили пациентов и выявлять скрытые патологии на ранних стадиях.
Системы мониторинга неотложных состояний с использованием алгоритмов машинного обучения обеспечивают непрерывный контроль за жизненно важными показателями пациентов, что позволяет оперативно реагировать на критические изменения и минимизировать риск развития осложнений. Аналогичные технологии применяются для ведения мониторинга хронических заболеваний, что способствует улучшению качества жизни пациентов и снижению затрат на медицинское обслуживание.
Таким образом, внедрение ИИ в систему здравоохранения представляет собой значительный шаг вперед в развитии медицинской науки и практики. Эти технологии не только повышают эффективность диагностики и лечения, но и способствуют улучшению общего состояния здоровья населения, особенно в удаленных и труднодоступных регионах.
Следует подчеркнуть, что на текущий момент в базе данных Росздравнадзора зарегистрировано 48 различных медицинских изделий, интегрирующих технологии искусственного интеллекта. Среди них 43 продукта разработаны отечественными производителями, что свидетельствует о высоком уровне технологической компетенции российских специалистов в данной области.
Эволюция инновационных технологий неразрывно связана с динамичным развитием сектора медицинской науки, который, в свою очередь, выступает в качестве фундаментального драйвера научно-технического прогресса. Интеграция молодежи в научно-исследовательскую деятельность и стимулирование научной элиты к решению приоритетных задач национального развития представляют собой стратегически значимые направления государственной политики. Министерство промышленности и торговли Российской Федерации активно осуществляет информационную поддержку, предоставляя доступ к современным инструментам и механизмам финансирования проектов в области медицинской промышленности, а также обеспечивая эффективное взаимодействие с поставщиками необходимых компонентов и сырья.
Контроль качества, безопасности и эффективности выводимых на рынок медицинских изделий
Контроль качества, безопасности и эффективности медицинских изделий, предназначенных для введения в обращение на российском рынке, осуществляемый Федеральной службой по надзору в сфере здравоохранения, является ключевым элементом комплексной системы обеспечения безопасности пациентов, гарантирующим соответствие медицинских изделий установленным стандартам и нормативным требованиям.
Российская система регистрации медицинских изделий демонстрирует ряд преимуществ по сравнению с зарубежными аналогами, в частности, в аспекте временных рамок, особенно при наличии квалифицированного сопровождения регуляторных процессов. Это обусловлено комплексным подходом к обеспечению качества и конкурентоспособности отечественной продукции в медицинской сфере.
С 1 марта 2025 года вступили в силу обновленные Правила государственной регистрации медицинских изделий, которые существенно модифицируют ранее действующий порядок. Ключевым элементом нововведений является опция выбора одной из альтернативных процедур государственной регистрации для медицинских изделий отечественного производства. Эта услуга впервые предполагает формирование реестровой записи о медицинском изделии с одновременным полным переводом процедуры в электронный формат. Кроме того, новые правила регламентируют особый порядок регулирования определенных аспектов обращения программного обеспечения, основанного на технологиях искусственного интеллекта.
Комплексную научно-техническую и организационно-методическую поддержку в области разработки нормативной документации, планирования и проведения всех видов технических испытаний, токсикологических исследований и клинико-лабораторных анализов осуществляет подведомственный институт ФГБУ «ВНИИИМТ» Росздравнадзора. В частности, он обеспечивает сопровождение клинических испытаний, включая те, что проводятся с участием человека. Комплексная услуга консультирования заявителей по принципу «одного окна» позволяет существенно сократить сроки регистрации медицинских изделий и минимизировать финансовые затраты производителей. Эта услуга интегрирует различные этапы процесса регистрации, обеспечивая их координацию и оптимизацию, что способствует повышению эффективности и снижению административных барьеров.
Оптимизация технического обслуживания медицинской техники
Одним из основополагающих факторов, обеспечивающих безопасность медицинской помощи, является систематическое и высококачественное техническое обслуживание медицинского оборудования. В гарантийный и постгарантийный периоды данный аспект приобретает критическую значимость, поскольку он не только обеспечивает безопасную эксплуатацию и оптимальное функционирование аппаратуры, но и способствует рациональному использованию бюджетных средств. Надлежащее техническое обслуживание, включая своевременную диагностику, профилактику и ремонт, является ключевым элементом в цепочке мероприятий, направленных на поддержание высокого уровня медицинской помощи и снижение рисков, связанных с использованием неисправного оборудования. Таким образом, данное направление деятельности требует комплексного подхода и высокого уровня профессионализма специалистов, что, в свою очередь, способствует повышению эффективности системы здравоохранения в целом.
Существенную угрозу для работоспособности медицинского оборудования спровоцировал уход западных производителей, включая их сервисные и логистические подразделения, с российского рынка, в сочетании с принудительным нарушением цепочек поставок запасных частей и комплектующих. Более того, многие производители медицинской продукции не предоставляют сторонним сервисным организациям необходимую документацию, ключи и пароли для доступа к техническим системам. Является значимой проблемой и тот факт, что децентрализованная модель технического обслуживания и ремонта медицинских изделий распространена в большинстве регионов Российской Федерации, что вынуждает руководителей медицинских учреждений самостоятельно решать широкий спектр вопросов, связанных с обеспечением бесперебойной работы медицинской техники.
Учитывая все вышеперечисленные проблемы, а также в контексте модернизации и повышения эффективности системы здравоохранения, Росздравнадзор инициировал создание Центра технического обслуживания и ремонта медицинской техники на базе ФГБУ «ВНИИИМТ». Данный центр, являясь ключевым элементом инфраструктуры для обеспечения надежности и долговечности медицинского оборудования, активно расширяет свою деятельность в различных регионах страны.
В 2024 году был успешно открыт межрегиональный филиал в Донецке, что позволило значительно улучшить доступность сервисных услуг для медицинских учреждений в этом регионе. Кроме того, были организованы представительства в Луганске и Мелитополе, что способствовало расширению географического охвата и повышению уровня технической поддержки. С момента открытия центра проведена комплексная диагностика 55 тысяч единиц медицинской техники, из которых 8 тысяч были обслужены и отремонтированы. Эти показатели свидетельствуют о высокой востребованности услуг центра и его способности оперативно реагировать на потребности медицинских учреждений. В 2025 году был открыт филиал
в Санкт-Петербурге, на базе которого был создан центр компетенций в области эндоскопического оборудования. Это решение позволило сосредоточить усилия на развитии специализированных услуг, связанных с ремонтом и обслуживанием сложной медицинской техники.
Особое внимание уделяется направлениям, связанным с ремонтом рентгеновских излучателей для компьютерных томографов и восстановлением систем криохлаждения магнитно-резонансных томографов. Эти технологии являются критически важными для современной медицины, и их надежность напрямую влияет на качество диагностики и лечения пациентов.
Таким образом, деятельность Центра технического обслуживания и ремонта медицинской техники, созданного Росздравнадзором, является важным вкладом в развитие системы здравоохранения и повышение ее эффективности.
В ответ на международные санкции и уход зарубежных производителей с отечественного рынка, ФГБУ «ВНИИИМТ» инициировало комплексную программу испытаний и экспертной оценки неоригинальных компонентов для их последующего применения в техническом обслуживании медицинских изделий. Эта программа реализуется в соответствии с постановлением Правительства Российской Федерации от 01.04.2022 № 5521 и приказом Федеральной службы по надзору в сфере здравоохранения от 16.05.2023 № 29832. На сегодняшний день завершены успешные испытания, подтверждающие безопасность использования 10 моделей российских рентгеновских излучателей. Это достижение имеет стратегическое значение для удовлетворения спроса на ключевые компоненты для наиболее востребованных моделей компьютерных томографов, включая продукцию таких ведущих мировых брендов, как Canon, Toshiba, GE и Siemens. Результаты данных исследований не только способствуют стабилизации рынка медицинских изделий в условиях санкционного давления, но и закладывают основу для дальнейшего развития отечественной индустрии медицинского оборудования, повышая ее независимость и конкурентоспособность на глобальном уровне.
Согласно проведенным расчетам, замещение импортных рентгеновских излучателей отечественными аналогами приведет к значительной экономии финансовых ресурсов медицинских учреждений в размере от 3 до 9 млн рублей. Это обусловлено снижением стоимости приобретения и эксплуатации оборудования, а также оптимизацией логистических процессов. Кроме того, внедрение отечественных технологий позволит существенно сократить сроки проведения ремонтных работ и время поставки оборудования, что в совокупности составит приблизительно два месяца.
Мониторинг безопасности медицинских изделий
Федеральная служба по надзору в сфере здравоохранения (Росздравнадзор) осуществляет непрерывный мониторинг безопасности медицинских изделий, применяя современные автоматизированные информационные технологии. Данная система позволяет фиксировать данные о неблагоприятных инцидентах, возникающих при использовании медицинских изделий, а также о результатах пострегистрационного клинического мониторинга, особенно в отношении изделий высокого класса риска. Этот процесс включает комплексный анализ и оценку потенциальных рисков, что способствует повышению уровня безопасности и эффективности медицинских технологий.
О значительном повышении уровня информированности среди участников системы, особенно среди медицинского персонала, свидетельствует анализ данных, интегрированных в автоматизированную информационную систему здравоохранения. К сентябрю 2025 года количество сообщений о нежелательных явлениях, связанных с использованием медицинских изделий, достигло уровня, зафиксированного по итогам предыдущего года (рис. 4). Важно отметить, что наблюдается существенный рост числа сообщений о неблагоприятных событиях, связанных с применением медицинских изделий высокого класса риска (рис. 5). Однако данная тенденция обусловлена интенсификацией мониторинга и отчетности в этой области среди субъектов обращения медицинских изделий, а не снижением их качества.
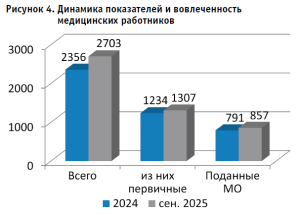
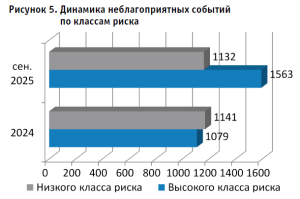
Следует также подчеркнуть, что объем поступивших отчетов о пострегистрационном клиническом мониторинге медицинских изделий значительно увеличился по сравнению с предыдущим годом, что свидетельствует о растущем интересе и усилении контроля в данной области.
С сентября 2025 года Федеральная служба по надзору в сфере здравоохранения внедрила систему интеграции данных о проведенных клинических испытаниях, включая информацию о выдаваемых актах оценки их результатов, в автоматизированную информационную систему. Эта система предназначена для медицинских организаций, обладающих соответствующими полномочиями для проведения клинических испытаний медицинских изделий. В настоящий момент реестр клинических испытаний активно пополняется результатами проведенных исследований, что способствует повышению прозрачности и надежности процесса регистрации медицинских изделий.
В рамках реализации комплексной стратегии противодействия фальсификации медицинских изделий, Федеральная служба по надзору в сфере здравоохранения активно внедряет систему маркировки продукции. В настоящее время данная инициатива реализуется в экспериментальном формате, охватывая ограниченный перечень медицинских изделий. Однако в перспективе планируется ее повсеместное распространение, что позволит существенно повысить уровень контроля за качеством медицинской продукции на рынке.
Система маркировки медицинских изделий представляет собой инновационный инструмент, основанный на использовании цифровых идентификаторов, наносимых на упаковку продукции. Это решение позволяет осуществлять мониторинг движения медицинских изделий от производителя до конечного потребителя, обеспечивая высокий уровень прозрачности и надежности.
Внедрение маркировки медицинских изделий открывает широкие перспективы для разработки превентивных мер, направленных на прогнозирование и предотвращение возможных дефицитов определенных видов продукции на рынке. Это, в свою очередь, способствует оптимизации логистических процессов и повышению эффективности управления запасами в системе здравоохранения.
Интеграция системы маркировки медицинских изделий в систему государственного контроля является стратегически важным шагом на пути к обеспечению безопасности и качества медицинской помощи, оказываемой населению.
В настоящее время в государственной информационной системе мониторинга товаров (ГИС МТ) зарегистрировано свыше 36,5 тысяч участников, а также нанесено более 188 миллионов кодов маркировки на медицинские изделия. Эксперимент по внедрению маркировки девяти видов медицинских изделий продлен до 28 февраля 2026 года, что свидетельствует о его значимости и эффективности. Кроме того, в настоящее время инициирован новый эксперимент, охватывающий семь дополнительных видов медицинских изделий, что расширяет спектр применения данной системы и повышает уровень контроля за оборотом продукции.
Внедрение обязательной маркировки медицинских изделий представляет собой инновационный подход к обеспечению прозрачности и эффективности цепочки поставок. Данная система позволяет осуществлять мониторинг полного цикла движения медицинских товаров от производителя или импортера до конечного потребителя, что существенно снижает уровень нелегального оборота продукции. Более того, интеграция маркировки в процесс управления медицинскими изделиями открывает новые возможности для оптимизации логистических операций, планирования закупок и производственных мощностей. Это, в свою очередь, способствует повышению качества медицинской помощи и рациональному использованию ресурсов здравоохранения.
Росздравнадзор активно развивает интеграционные процессы с маркетплейсами, направленные на обеспечение доступа к Государственному реестру медицинских изделий и организаций, осуществляющих их производство и изготовление (рис.6). Особое внимание уделяется разработке и внедрению алгоритмов для оперативного взаимодействия, что позволяет эффективно блокировать предложения о реализации продукции, обладающей признаками медицинских изделий, в случаях выявления нарушений.

Следует отметить, что процесс интеграции маркетплейсов с Реестром медицинских изделий находится в стадии завершения и будет окончательно реализован после 1 октября 2025 года. Этот шаг является важным этапом в обеспечении прозрачности и безопасности рынка медицинских изделий, а также в укреплении государственного контроля за их оборотом.
В контексте федерального государственного контроля (надзора) за обращением медицинских изделий индикаторы риска несоответствия обязательным требованиям представляют собой важный инструмент, интегрированный в систему мониторинга и оценки рисков. Этот механизм, обладающий высокой степенью адаптивности, функционирует на основе анализа текущей ситуации, что позволяет оперативно реагировать на изменения в сфере обращения медицинских изделий.
В рамках анализа эффективности ключевых показателей в 2024 году был проведен ряд исследований, по результатам которых было принято решение об исключении из мониторинга в 2025 году трех индикаторов риска, продемонстрировавших недостаточную результативность. К таким индикаторам относятся: «сотрудники на час», «помещение на час» и «рост клинических испытаний». Основанием для данного решения послужил анализ данных, свидетельствующий о том, что показатели эффективности этих индикаторов не достигли порогового значения в 75% по итогам прошедшего года. Таким образом, исключение указанных индикаторов из системы мониторинга является стратегически обоснованным шагом, направленным на оптимизацию аналитического процесса и повышение его точности и релевантности.
Первый индикатор риска «Повторное внесение изменений в регистрационное досье (ВИРД)» вступил в силу 5 мая 2025 года: непоступление от разработчика или производителя (изготовителя) медицинского изделия, или уполномоченного представителя производителя (изготовителя) медицинского изделия, или лица, осуществляющего ввоз медицинского изделия в Российскую Федерацию в целях его государственной регистрации, повторного заявления о внесении изменений в документы, содержащиеся в регистрационном досье на медицинское изделие, в течение 180 календарных дней с даты принятия Федеральной службой по надзору в сфере здравоохранения, в соответствии с международными договорами и актами, составляющими право Евразийского экономического союза или актами Правительства Российской Федерации, изданными во исполнение частей 4 и 51 статьи 38 Федерального закона от 21 ноября 2011 г. № 323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации», соответствующего решения об отказе во внесении изменений в регистрационное досье или о возврате заявления о внесении изменений и документов, или о прекращении дальнейшего рассмотрения заявления о внесении изменений в документы, содержащиеся в регистрационном досье, при условии наличия предложения к реализации такого медицинского изделия, в том числе дистанционным способом.
В настоящее время функционируют два индикатора риска, которые играют ключевую роль в оценке и мониторинге потенциальных угроз:
- «Аренда на час»;
- «Повторное ВИРД».
Также в настоящее время в Министерстве здравоохранения Российской Федерации активно обсуждаются проекты пяти индикаторов риска, направленных на обеспечение безопасности и качества медицинских изделий. Эти индикаторы разработаны с учетом современных требований к регуляторным процессам и направлены на выявление потенциальных угроз в сфере обращения медицинских изделий.

Первый индикатор предполагает выявление Федеральной службой по надзору в сфере здравоохранения информации, включая данные анализа Единой информационной системы в сфере закупок, о медицинских изделиях, стоимость которых существенно ниже отпускной цены производителя (в два и более раза). При этом важным условием является соответствие срока годности (или срока службы) таких изделий не менее половины от общего установленного срока. Данный индикатор позволяет оперативно идентифицировать потенциально недобросовестные практики в ценообразовании на медицинские изделия, что способствует повышению уровня доверия к рынку и защите интересов потребителей.
Второй индикатор направлен на выявление Росздравнадзором медицинских изделий (техники), удовлетворяющих следующим критериям:
1) отсутствие изменений в регистрационном досье в течение десяти и более лет с момента государственной регистрации;
2) высокая степень риска, относящаяся к классам потенциального риска применения 2б и более;
3) наличие предложений о реализации.
Данный индикатор позволяет своевременно выявлять медицинские изделия, которые могут представлять угрозу для здоровья пациентов из-за устаревших технических характеристик или недостаточного уровня безопасности.
Третий индикатор фокусируется на отсутствии в автоматизированной информационной системе Росздравнадзора сведений о направлении медицинскими организациями сообщений о неблагоприятных событиях, связанных с использованием медицинских изделий, отнесенных к различным категориям риска:
- чрезвычайно высокого риска – в течение года и более;
- высокого риска – в течение полутора лет и более;
- значительного риска – в течение двух и более лет;
- среднего, умеренного и низкого риска – в течение трех и более лет.
Отсутствие таких сведений может свидетельствовать о недостаточной прозрачности и контроле в сфере обращения медицинских изделий, что требует принятия соответствующих мер для повышения уровня безопасности пациентов.
Четвертый индикатор направлен на выявление несоответствий в сведениях автоматизированной информационной системе АИС Росздравнадзора, представленных производителем или импортером медицинских изделий, с данными, размещенными в Единой информационной системе в сфере закупок. Это включает сопоставление информации о вариантах исполнения, моделях, составе и комплектации медицинских изделий. Выявление таких несоответствий позволяет своевременно выявлять фальсифицированные или некачественные медицинские изделия, что способствует защите здоровья населения и повышению уровня доверия к медицинской продукции.
Пятый индикатор направлен на проверку наличия на маркировке медицинских изделий, находящихся в обращении, сведений об адресе производителя или месте производства, которые фактически отсутствуют в регистрационном удостоверении. Данный индикатор позволяет выявлять случаи несоответствия информации на упаковке и в официальных документах, что может свидетельствовать о нарушениях в процессе регистрации и обращения медицинских изделий.
Ответственность за корректное использование медицинских изделий лежит на медицинском персонале, который играет ключевую роль в обеспечении их эффективного применения в условиях медицинской организации. Надлежащая реализация процедур метрологического контроля, технического обслуживания и ремонта медицинского оборудования является критически важным фактором, обеспечивающим безопасность как пациентов, так и медицинских работников при использовании медицинских изделий в медицинской практике.
Совершенствование регуляторных механизмов
В контексте углубленной интеграции и гармонизации правовой базы Евразийского экономического союза (ЕАЭС) продолжается активная работа по совершенствованию регуляторных механизмов, направленных на унификацию подходов к оценке медицинских изделий в государствах-членах союза. В этом контексте следует отметить принятие в 2025 году Концепции развития общего рынка медицинских изделий ЕАЭС, представляющей собой стратегический документ, который определяет основные направления эволюции нормативно-правовой базы в данной области.
Важным шагом в этом направлении стало создание на базе ФГБУ «Всероссийский научно-исследовательский и испытательный институт медицинской техники» (ФГБУ «ВНИИИМТ») Росздравнадзора экспертного сообщества по обращению медицинских изделий. Данное сообщество функционирует как специализированная площадка для оперативного взаимодействия экспертов государств-членов ЕАЭС, что способствует более эффективной координации усилий в сфере регулирования медицинских технологий.
Предпринятые меры направлены на формирование единой регуляторной среды, обеспечивающей безопасность и качество медицинских изделий на территории ЕАЭС, а также на создание условий для устойчивого развития общего рынка медицинских технологий в рамках союза.
Заключение
В условиях современной трансформации мировой экономики и развития высоких технологий рынок медицинских изделий претерпевает значительные изменения. Это проявляется в смене ключевых участников рынка, а также в появлении новых, сложных и передовых медицинских изделий, функционирующих на основе искусственного интеллекта (ИИ). Данная тенденция свидетельствует о стремительном развитии сферы обращения медицинских изделий, что, в свою очередь, требует адекватной правовой регламентации.
В Российской Федерации активно совершенствуется нормативно-правовая база, регулирующая обращение медицинских изделий, как на национальном уровне, так и в рамках Евразийского экономического союза (ЕАЭС). Это создает необходимые условия для устойчивого развития отечественного рынка медицинских изделий и повышения его конкурентоспособности на международной арене.
Особое внимание уделяется внедрению системы контроля за движением медицинской продукции, что позволяет обеспечить ее безопасность, качество и клиническую эффективность. Однако достижение этих целей возможно только при условии консолидации усилий регулятора, медицинских и экспертных организаций. Таким образом, комплексная работа всех заинтересованных сторон является ключевым фактором успешного развития рынка медицинских изделий и реализации стратегических задач, поставленных Президентом Российской Федерации В.В. Путиным.
__________________________________________________________________
1 Постановление Правительства Российской Федерации от 01.04.2022 № 552 «Об утверждении особенностей обращения, включая особенности государственной регистрации, медицинских изделий в случае их дефектуры или риска возникновения дефектуры в связи с введением в отношении Российской Федерации ограничительных мер экономического характера». URL: https://base.garant.ru/403820386/?ysclid=mgjnprwnpz306075641.
2 Приказ Федеральной службы по надзору в сфере здравоохранения от 16.05.2023 № 2983 «Об утверждении перечня представляемых документов и требований к их содержанию, формы заключения о возможности (невозможности) использования комплектующих или принадлежностей медицинского изделия, не предусмотренных в их технической и (или) эксплуатационной документации производителя (изготовителя), перечня сведений о комплектующих или принадлежностях медицинского изделия, не предусмотренных в их технической и (или) эксплуатационной документации производителя (изготовителя), публикуемых на официальном сайте федерального государственного бюджетного учреждения “Всероссийский научно-исследовательский и испытательный институт медицинской техники” Федеральной службы по надзору в сфере здравоохранения в информационно-телекоммуникационной сети “Интернет”». URL: http://publication.pravo.gov.ru/document/0001202306020041?ysclid=mgjno7rcb5872941689.
