ФАРМАКОНАДЗОР
Оценка состояния системы фармаконадзора на уровне аптечных организаций (на примере Северо-Западного и Приволжского федеральных округов)
1 — Федеральное государственное бюджетное образовательное учреждение высшего образования «Санкт-Петербургский государственный химико-фармацевтический университет» Министерства здравоохранения Российской Федерации, 197376, Российская Федерация, г. Санкт-Петербург, ул. Профессора Попова, д. 14, лит. А.
2 — Федеральное государственное бюджетное образовательное учреждение высшего образования «Санкт-Петербургский государственный химико-фармацевтический университет» Министерства здравоохранения Российской Федерации, 197376, Российская Федерация, г. Санкт-Петербург, ул. Профессора Попова, д. 14, лит. А.
3 — Федеральное государственное бюджетное образовательное учреждение высшего образования «Санкт-Петербургский государственный химико-фармацевтический университет» Министерства здравоохранения Российской Федерации, 197376, Российская Федерация, г. Санкт-Петербург, ул. Профессора Попова, д. 14, лит. А.
4 — Федеральное государственное бюджетное образовательное учреждение высшего образования «Санкт-Петербургский государственный химико-фармацевтический университет» Министерства здравоохранения Российской Федерации, 197376, Российская Федерация, г. Санкт-Петербург, ул. Профессора Попова, д. 14, лит. А.
В статье рассмотрен порядок осуществления фармаконадзора в аптечных организациях Северо-Западного и Приволжского федеральных округов, проведена оценка удовлетворенности потребителей лекарственных препаратов информационно-консультативными услугами специалистов аптечных организаций по вопросам фармаконадзора. Проведенное исследование показало, что не все участвовавшие в исследовании аптечные организации соответствуют установленным требованиям (не везде назначено ответственное по фармаконадзору должностное лицо, только 30% фармацевтических работников верно указали нормативные правовые акты, регламентирующие проведение фармаконадзора, несущественная часть проанкетированных специалистов готовы использовать современные информационные системы для направления извещений в Росздравнадзор и пр.). Выявлены существенные недостатки документации системы менеджмента качества (в том числе, в стандартных операционных процедурах). С учетом полученных результатов сформулированы практические рекомендации по совершенствованию работы аптечных организаций в системе фармаконадзора.
Ключевые слова: фармаконадзор, нежелательные реакции, аптечные организации, фармацевтические работники, система менеджмента качества, стандартная операционная процедура
Введение
В соответствии с действующим законодательством Российской Федерации субъекты обращения лекарственных средств (ЛС), включая фармацевтические организации, обязаны предоставлять в Росздравнадзор информацию о нежелательных реакциях (НР) лекарственных препаратов (ЛП) и иную информацию по безопасности и эффективности, выявленную на всех этапах обращения ЛП. Соответствующие требования также закреплены в приказе Росздравнадзора от 15.02.2017 № 1071 «Об утверждении Порядка осуществления фармаконадзора» [4], а также как лицензионные – при осуществлении фармацевтической деятельности: аптечные организации (АО) обязаны разрабатывать, внедрять и развивать систему менеджмента качества (СМК). При этом базовыми требованиями СМК являются удовлетворенность потребителей и обратная связь, а также работа с несоответствующей продукцией [3]. В обязанность специалистов аптечных организаций, согласно профессиональным стандартам, входит регистрация обращений потребителей о возникновении побочных действий, НР, серьезных НР, непредвиденных НР при применении ЛП, об индивидуальной непереносимости и отсутствии терапевтической эффективности (ТЭ) ЛП [5, 6, 7, 8].
По итогам проведенных Росздравнадзором мероприятий за 2021 год, рассмотрено 60 372 сообщений о НР и терапевтической неэффективности при применении ЛП (рис. 1) [1, 2].
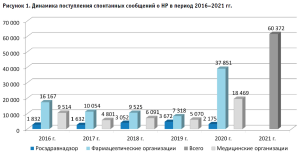
Очевидно, что фармацевтические организации с 2020 года начали принимать более активное участие в сборе данных о НР ЛП, что, безусловно, является положительным показателем, позволяющим в полной мере фиксировать возникающие у пациентов НР. Эффективность проводимой работы по фармаконадзору (ФНЗ) зависит так же и от вовлеченности потребителей ЛП, являющихся источником спонтанных сообщений о безопасности и эффективности ЛП.
В этой связи, целью настоящего исследования стало изучение порядка осуществления ФНЗ в АО, а также оценка удовлетворенности потребителей ЛП информационно-консультативной помощью специалистов АО по вопросам ФНЗ.
Материалы и методы
Методологическую основу работы составили нормативные правовые акты, регулирующие ФНЗ в РФ. Информационной базой исследования служили объекты инфраструктуры и документация СМК исследуемых АО (44 АО Северо-Западного и Приволжского федеральных округов государственной и частной формы собственности различных юридических лиц), обращения граждан, результаты анкетирования фармацевтических работников и посетителей АО. Сбор и обработка данных проводилась с использованием инструментов MS Excel 2016, онлайн-анкетирования через сервисы Google. Репрезентативная выборка была рассчитана по приведенной ниже формуле и составила 384:
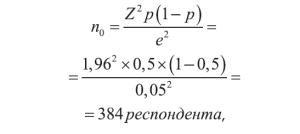
где n0 – объем выборки;
Z – значение стандартизованной нормально распределенной случайной величины, соответствующее интегральной вероятности (при доверительном уровне, равном 95%, Z = 1,96);
p – доля объектов с заданным признаком (для исключения недооценки выборки принято значение 0,5, при котором произведение p(1 – p) максимально;
e – допустимая ошибка выборки (принят ±5%).
Дальнейший расчет объема выборки с учетом генеральной совокупности не производился, так как объем генеральной совокупности значительно больше объема выборки (в сотни и более раз). Статистическая обработка результатов анкетирования проводилась с учетом критерия согласия Пирсона, а с помощью программы SPSS Statistics V.26.0 было получено совместное распределение переменных и найдены статистически значимые закономерности (p<0,05).
Результаты и обсуждение
Федеральным законом от 12.04.2010 №61-ФЗ установлена обязанность субъектов обращения ЛС сообщать в Росздравнадзор о побочных действиях, НР, серьезных НР, непредвиденных НР, об индивидуальной непереносимости, отсутствии ТЭ ЛП, а также об иных фактах и обстоятельствах, представляющих угрозу жизни или здоровью человека. Законом также предусмотрена ответственность за несообщение или сокрытие сведений о выявленном НР ЛП для лиц, которым они стали известны по роду их профессиональной деятельности. Нормативные документы Росздравнадзора регламентируют назначение ответственных по ФНЗ должностных лиц, порядок и сроки передачи регулятору выявленной информации [4]. Кроме того, согласно Правилам надлежащей аптечной практики (НАП) руководитель субъекта розничной торговли обязан обеспечить проведение инструктажа работников по вопросам обработки данных, полученных от покупателей и доведения данной информации до заинтересованных лиц [3]. Таким образом, обязанность сообщать о НР на ЛП юридически закреплена для всех участников обращения ЛС, в том числе и для фармацевтических работников. При этом в АО мероприятия, проводимые с целью ФНЗ, являются еще и частью общей СМК.
Контент-анализ профессиональных стандартов позволяет утверждать, что специалисты АО являются одним из важных звеньев системы ФНЗ в части оказания информационно-консультационной помощи при возникновении побочных реакций, НР на ЛП. Кроме того, фармацевтические работники обязаны оформлять извещения о НР на ЛП, отсутствии ТЭ ЛП, о побочных действиях, о жалобах потребителей. Соответствующие требования к трудовым функциям работников представлены в таблице 1 [5, 6, 7, 8].
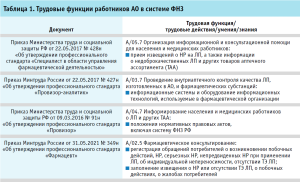
Из данных таблицы 1 следует, что профессиональные стандарты:
- устанавливают вовлечение в систему ФНЗ всех специалистов АО, от руководящего персонала до работников «первого стола»;
- объединяют и формируют обобщенную компетенцию по фармацевтическому консультированию, информированию, регистрации и репортированию о НР, которая является важной составляющей фармацевтической деятельности.
С целью изучения порядка осуществления ФНЗ в АО проведено анкетирование фармацевтических работников. В нем приняли участие специалисты как со средним (84%), так и высшим (23%) фармацевтическим образованием со стажем работы от 3 до 10 лет (41%). Анкета включала 20 вопросов и была структурирована по блокам:
1) осведомленность работников АО о ФНЗ;
2) работа АО с выявленными НР или отсутствием ТЭ ЛП;
3) соответствие АО нормативным документам, в т.ч. оценка СМК субъекта розничной торговли ЛС.
Анализ осведомленности специалистов по вопросам ФНЗ показал, что 100% респондентов знают о создании и функционировании в РФ системы непрерывного мониторинга безопасности ЛП. Однако только 30% фармацевтических работников верно указали нормативные правовые акты, регламентирующие проведение ФНЗ в АО. При этом крайне незначительное количество фармацевтических работников ответили, что сообщение о НР или терапевтической неэффективности ЛП относится к их прямым должностным обязанностям (14%). В результате обработки ответов, связанных с деятельностью АО при выявлении НР или отсутствия ТЭ ЛП, установлено, что существенную долю (39%) составляют АО, в которых не назначен специалист, ответственный по ФНЗ, что является прямым нарушением требований нормативных документов. Большинство АО (64%) имеет персонализированный доступ в АИС Росздравнадзора, однако анкетирование показало незначительную практику использования АИС для направления извещений в Росздравнадзор (только 25% АО используют данный ресурс). В условиях современного тренда на цифровизацию системы здравоохранения, выявленные показатели представляются неприемлемо низкими, что сигнализирует о необходимости усиления работы руководителей АО в этом направлении.
Несмотря на высокую долю обнаружения НР в исследуемых АО (55%), информируют руководителя о выявлении таких фактов 34% опрошенных, непосредственно сообщают регулятору полученные сведения около 13% работников, а 9% – вообще не предпринимают никаких действий (рис. 2). Следует отметить, что полученные 44% «совет об отмене ЛП» не являются достаточным действием специалиста и требуют выполнения дальнейших мероприятий по ФНЗ.
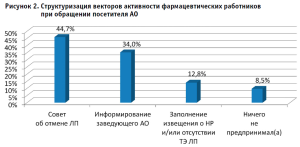
При отпуске ЛП только 11% сотрудников исследуемых АО регулярно информируют посетителей о рисках, связанных с возможным появлением НР или терапевтической неэффективности ЛП и необходимости передачи такой информации лечащему врачу, работнику аптеки или самостоятельно в Росздравнадзор. Подавляющее же количество респондентов проводят данную информационно-консультативную помощь только в случае, если посетитель аптеки сам проявляет интерес (86%).
Полученные данные свидетельствуют о необходимости обучения специалистов именно «первого стола», что также подтверждается результатами статистической обработкой анкет. Были установлены статистически значимые закономерности уровня образования и осведомленности: заведующие АО и их заместители более компетентны и информированы об организации системы ФНЗ, однако они не в полной мере проводят работу по информированию и обсуждению данных вопросов с рядовыми специалистами.
Выявлены ведущие факторы, препятствующие вовлеченности фармацевтических работников в мероприятия ФНЗ (рис. 3).
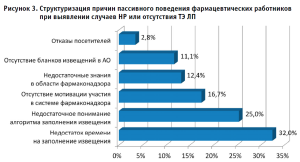
К числу наиболее значимых, по мнению опрошенных, относятся:
- недостаток времени на заполнение извещения (32%);
- непонимание алгоритма заполнения извещения (25%);
- отсутствие мотивации и недостаточные знания в области ФНЗ (около 30%).
Таким образом, проведенные исследования показали, что фармацевтические работники, являясь потенциально значимыми идентификаторами фактов НР или отсутствия ТЭ ЛП, не всегда и не в полной мере выполняют требования действующего законодательства о регистрации и передаче таких спонтанных сообщений по предусмотренным информационным каналам (в том числе электронным).
Повышение качества предоставляемых фармацевтических услуг является одной из основных целей АО. Указанная цель достигается, в том числе, путем внедрения СМК в деятельность АО. Нами была проведена оценка СМК субъектов розничной торговли ЛС – объектов исследования (рис. 4). Особое внимание при этом было уделено документации СМК, организации мероприятий, необходимых для постоянного улучшения качества обслуживания покупателей и повышения персональной ответственности работников. Кроме того, оценивалась работа по обеспечению проведения инструктажей по вопросам методов обработки данных, полученных от покупателей при применении ЛП.
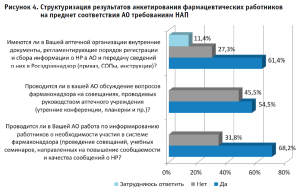
Установлено, что большинство АО отвечают требованиям НАП. Однако анализ СОП АО по ФНЗ позволил выявить ряд серьезных недочетов:
- не проработан раздел «Нормативные ссылки», включающий утратившие силу нормативные правовые акты, что, в свою очередь, свидетельствует об отсутствии работы по актуализации документов СМК;
- большинство проанализированных СОП не предусматривают назначение ответственного по ФНЗ;
- не предусмотрено проведение обучения сотрудников, а также контроля результатов таких мероприятий;
- не определена ответственность за своевременную актуализацию СОП. Данный аспект является одним из основных в части управления документацией СМК, так как, в случае изменения законодательства, выявления несоответствий СОП необходимо своевременно пересматривать. В случае отсутствия ответственного лица за обновление СОП, процедура рискует «устареть», что приведет к нарушению требований законодательства;
- во всех исследуемых СОП не предусмотрена оценка результативности мероприятий, проводимых в АО в части ФНЗ. Это свидетельствует об отсутствии процессного подхода в управлении – еще одного важного принципа СМК.
Полученные данные были положены в основу разработки рекомендаций по совершенствованию СОП по ФНЗ в АО. Примерная структура и содержание документа приведены в таблице 2.

Как следует из таблицы 2, рекомендуемая форма СОП является традиционной. А вот наполненность разделов, как правило, свидетельствует о том, разработана и внедрена СМК в организации формально или нет. При этом особое внимание следует уделить разделу «Оценка результативности». В нем, с учетом регуляторных требований, должны быть зафиксированы:
1) наличие приказа о назначении ответственного по ФНЗ, утверждены его полномочия и обязанности;
2) все необходимые для осуществления ФНЗ действия и мероприятия задокументированы и оформлены в виде СОП;
3) наличие приказа о назначении лица, ответственного за регулярную актуализацию СОП;
4) ретроспективный анализ записей и данных по ФНЗ в установленных формах за прошедшие периоды;
5) наличие приказа об утверждении графиков и журналов прохождения обучения и проверки знаний сотрудников;
6) рабочие места специалистов обеспечены персонализированным доступом в АИС Росздравнадзора или определены альтернативные способы передачи информации;
7) наличие в достаточном количестве бланков-извещений о НР или отсутствии ТЭ ЛП для «первостольников» и посетителей АО;
8) наличие в торговом зале доступной для посетителей информации о системе ФНЗ.
Для более объективной оценки организация ФНЗ в АО была также проанализирована с позиции конечного потребителя. С этой целью было опрошено 390 человек. Среди опрошенных пациентов случаи с возникновением НР возникали у меньшей половины – 43%, в том время как отсутствие ТЭ ЛП отмечали у себя около 68% опрошенных респондентов.
Ответы на вопросы, отражающие информированность пациентов о ФНЗ, позволили выявить недостаточную работу в исследуемой области, проводимую как органами исполнительной власти, так и непосредственно на местах – специалистами системы здравоохранения. Так, на вопрос «Как Вы считаете, при отсутствии ТЭ или возникновении НР, куда необходимо обращаться?», большинство респондентов (61%) указало врача, выписавшего ЛП, в то время как обращение в АО, где был приобретен ЛП, указало только 9% пациентов (рис. 5).
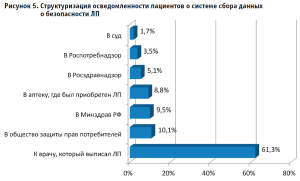
66% респондентов ответили, что не знают о существовании телефона горячей линии, а 56% – не знают о специальном сайте Росздравнадзора в сети Интернет, через которые можно передавать подобные сведения. На прямой вопрос о необходимости сообщения информации о безопасности ЛП напрямую специалисту АО, 60% респондентов ответили, что никогда не обращались по такому поводу в аптеку. Таким образом, фактическая роль провизора/фармацевта в данном вопросе для пациентов остается незначительной, что говорит о необходимости активизации работы в этом направлении в АО.
Статистическая обработка результатов анкетирования посетителей АО позволила выявить следующие статистически значимые закономерности:
- наиболее активно проявили себя респонденты более молодого возраста (от 18 до 35 лет), они заинтересованы возможностью сообщения о НР или отсутствии ТЭ ЛП лечащему врачу и специалисту АО посредством горячей линии и сайта Росздравнадзора;
- ответы респондентов средней возрастной группы (от 36 до 64 лет) показали, что для них более оптимальным является возможность сообщения самостоятельно в Росздравнадзор. Интерес для них также представляет соответствующая информация в торговом зале АО и СМИ;
- старшее поколение более заинтересовано в разъяснениях относительно возможности сообщения о НР или отсутствии эффективности ЛП самостоятельно – через телефон горячей линии;
- все респонденты, независимо от возраста, выразили готовность к диалогу со специалистом АО по вопросам ФНЗ и выражают надежду, что информирование в медицинских и АО будет проводиться более активно.
Заключение
Проведенное исследование показало, что АО – полноценный участник системы ФНЗ, который должен соответствовать всем установленным законодательным и нормативным требованиям. В этой связи особое внимание необходимо уделить надлежащей практике ФНЗ и НАП, в том числе, документации СМК. Объем и качество собранной в АО информации о НР напрямую зависит от уровня владения профессиональными компетенциями, поэтому очень важно продумать систему обучения, вовлеченности и мотивации сотрудников, непосредственно взаимодействующих с посетителями.
Необходимо обеспечить в свободном доступе для потребителей бланки форм-извещений, информацию о безопасности ЛП в виде постеров, буклетов и брошюр, содержащих сведения о НР и системе ФНЗ, инструкцию и алгоритм действий при обнаружении НР.
Проведение всех необходимых организационных, методических, обучающих и контрольных мероприятий на уровне АО будет способствовать совершенствованию качества предоставления фармацевтических услуг, повышению персональной ответственности сотрудников, информированности населения в вопросах ФНЗ, что, в конечном итоге, позволит увеличить поток спонтанных сообщений по безопасности ЛП.
- Доклад об осуществлении государственного контроля (надзора) в сфере охраны здоровья граждан и об эффективности такого контроля (надзора) в 2020 году // Официальный сайт Федеральной службы по надзору в сфере здравоохранения – URL: https://www.roszdravnadzor.gov.ru/spec/about/plans (дата обращения: 05.05.2022).
- Итоговый доклад о правоприменительной практике при осуществлении федерального государственного контроля (надзора) в сфере обращения лекарственных средств для медицинского применения // Официальный сайт Федеральной службы по надзору в сфере здравоохранения – URL: https://www.roszdravnadzor.gov.ru/spec/about/plans (дата обращения: 05.05.2022).
- Приказ Министерства здравоохранения РФ от 31.08.2016 № 647н «Об утверждении Правил надлежащей аптечной практики лекарственных препаратов для медицинского применения» // КонсультантПлюс. – URL: http://www.consultant.ru/document/cons_doc_LAW_210618/ (дата обращения 19.04.2022).
- Приказ Росздравнадзора от 15.02.2017 № 1071 «Об утверждении Порядка осуществления фармаконадзора» // КонсультантПлюс. – URL: http://www.consultant.ru/document/cons_doc_LAW_214216/ (дата обращения 19.04.2022).
- Приказ Минтруда России от 09.03.2016 № 91н «Об утверждении профессионального стандарта “Провизор”» // КонсультантПлюс. – URL: http://www.consultant.ru/document/cons_doc_LAW_196697/ (дата обращения 06.04.2022).
- Приказ Минтруда России от 22.05.2017 № 427н «Об утверждении профессионального стандарта “Провизор-аналитик”» // КонсультантПлюс. – URL: http://www.consultant.ru/document/cons_doc_LAW_217937/ (дата обращения 06.04.2022).
- Приказ Минтруда России от 22.05.2017 № 428н «Об утверждении профессионального стандарта “Специалист в области управления фармацевтической деятельностью”» // КонсультантПлюс. – URL: http://www.consultant.ru/document/cons_doc_LAW_217941/ (дата обращения 06.04.2022).
- Приказ Минтруда России от 31.05.2021 № 349н «Об утверждении профессионального стандарта “Фармацевт”»// КонсультантПлюс. – URL: http://www.consultant.ru/document/cons_doc_LAW_389037/ (дата обращения 06.04.2022).
