НОРМАТИВНОЕ ПРАВОВОЕ РЕГУЛИРОВАНИЕ ОБРАЩЕНИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ
О направлениях совершенствования механизма заключения долгосрочных контрактов со встречными инвестиционными обязательствами. Часть 2 – особенности отраслевого законодательства при реализации федеральных офсетных контрактов
1 — Федеральное государственное бюджетное образовательное учреждение высшего образования «Санкт-Петербургский химико-фармацевтический университет» Министерства здравоохранения Российской Федерации (ФГБОУ ВО СПХФУ Минздрава России), 197022, Российская Федерация, г. Санкт-Петербург, ул. Профессора Попова, д. 14, лит. А.
ORCID: https://orcid.org/0000-0003-4609-0155
2 — Федеральное государственное бюджетное образовательное учреждение высшего образования «Санкт-Петербургский химико-фармацевтический университет» Министерства здравоохранения Российской Федерации (ФГБОУ ВО СПХФУ Минздрава России), 197022, Российская Федерация, г. Санкт-Петербург, ул. Профессора Попова, д. 14, лит. А.
ORCID: https://orcid.org/0000-0001-5061-0729
3 — Федеральное государственное бюджетное образовательное учреждение высшего образования «Санкт-Петербургский химико-фармацевтический университет» Министерства здравоохранения Российской Федерации (ФГБОУ ВО СПХФУ Минздрава России), 197022, Российская Федерация, г. Санкт-Петербург, ул. Профессора Попова, д. 14, лит. А.
ORCID: https://orcid.org/0000-0001-6297-9304
4 — Федеральное государственное бюджетное образовательное учреждение высшего образования «Санкт-Петербургский государственный университет» (СПБГУ), 199034, г. Санкт-Петербург, Университетская наб., д.7/9.
ORCID: https://orcid.org/0000-0002-7765-4876
5 — Северо-Западный институт управления – филиал Федерального государственного бюджетного образовательного учреждения высшего образования «Российская академия народного хозяйства и государственной службы при Президенте Российской Федерации» (СЗИУ – филиал РАНХИГС), 199178, Санкт-Петербург, Средний просп. Васильевского острова, д. 57/43.
ORCID: https://orcid.org/0009-0008-7764-7845
В текущих экономических условиях возникает существенная потребность развития и совершенствования механизмов, которые способны ускорить темпы технологического развития, национального суверенитета и независимости Российской Федерации в реальном секторе экономики. Для бюджетной системы, в том числе для решения задач системы здравоохранения в части лекарственного обеспечения, одним из таких механизмов выступает долгосрочный контракт со встречными инвестиционными обязательствами. Реализация такого типа контрактов способна внести существенный вклад в снижение доли импортных товаров в структуре внутреннего потребления и повышение валового внутреннего продукта Российской Федерации, обеспечить дальнейшее развитие необходимой инфраструктуры, в том числе в фармацевтической отрасли, что, в свою очередь, позволит обеспечить стабильность поставок и доступность необходимых товаров, работ и услуг. В настоящем исследовании авторы поэтапно раскрывают и углубляют особенности путей развития данного инструмента на федеральном уровне, сформированные в первой части исследования.
Ключевые слова: контрактная система в сфере закупок для обеспечения государственных и муниципальных нужд, контракт со встречными инвестиционными обязательствами, офсетный контракт, орфанные лекарственные препараты, изготовление лекарственных препаратов, экстемпоральные лекарственные препараты, производственные аптеки, редкие (орфанные) заболевания, высокозатратные нозологии, фармацевтическая помощь
Введение
В предыдущей статье [1] было продемонстрировано ограниченное применение офсетных контрактов на региональном уровне, при одновременном существенном росте расходов бюджетов субъектов Российской Федерации на лекарственную терапию, что обосновало необходимость поиска решений для оптимизации бюджетных затрат и повышения доступности лекарственных препаратов для медицинского применения (далее – ЛП) для населения страны. Исходя из предыдущего тезиса, в исследовании были представлены пути федерализации государственных контрактов со встречными инвестиционными обязательствами поставщиков (исполнителей) по созданию, модернизации, освоению производства такого товара и (или) по созданию, реконструкции имущества (недвижимого имущества или недвижимого имущества и движимого имущества, технологически связанных между собой), предназначенного для оказания такой услуги (далее – офсетный контракт).
В настоящем исследовании проанализированы взаимосвязи лекарственного обеспечения пациентов с редкими (орфанными) заболеваниями, а также правовые коллизии при реализации офсетных контрактов, связанные с их ценообразованием и соответствием клиническим рекомендациям. Авторы приходят к выводу, что при совершенствовании механизма заключения офсетных контрактов необходимо гармонизировать отраслевое регулирование в сфере обращения лекарственных средств (далее – ЛС) и нормативные императивы офсетных контрактов.
Кроме того, в работе сформулированы предложения по повышению доступности и внедрению методов персонализированной медицины посредством реализации офсетных контрактов в сфере изготовления ЛП и возможности снижения нагрузки на бюджеты субъектов Российской Федерации в части обеспечения лиц с редкими (орфанными) заболеваниями.
Результаты и обсуждение Ценообразование офсетных контрактов. Недостаточная гармонизация Федерального закона от 5 апреля 2013 г. № 44-ФЗ (далее – ФЗ-44)1 с положениями Федерального закона от 12 апреля 2010 г. № 61-ФЗ (далее – ФЗ-61)2 может вызвать сложности в реализации офсетных контрактов в фармацевтической отрасли в части определения начальной максимальной цены контракта. В частности, в отношении производимых ЛП, подлежащих государственной регистрации (далее – зарегистрированный ЛП), и их ценового регулирования в случае отнесения к перечню ЖНВЛП осуществляется безотносительно факта заключения офсетного контракта. При регистрации цены на ЛП перечня ЖНВЛП используется, в том числе, метод сравнения цен в референтных государствах: в сравнении с ними цена в Российской Федерации должна быть минимальной. Цена на ЛП перечня ЖНВЛП также должна соответствовать иным критериям, закрепленным в постановлении Правительства Российской Федерации от 29 октября 2010 г. № 8653 и других нормативных правовых актах.
В указанных условиях потенциальному поставщику (инвестору) де-факто неизвестна фактическая цена продажи товаров, при этом в строительство, модернизацию, освоение производства которых вкладываются значительные инвестиции (от 100 млн руб.). За период создания, модернизации производства цена на взаимозаменяемые ЛП может снизиться вдвое или более, что приведет к убыточности проекта. Проблема актуальна не только для офсетных контрактов, но и для специальных инвестиционных контрактов.
Таким образом, целесообразно дополнительно разработать проект внесения изменений в законодательство о нормативном правовом регулировании регистрации цен на ЛП перечня ЖНВЛП, освоение производства которых будет осуществляться в рамках офсетных контрактов. Особые правила для таких ЛП должны действовать в пределах срока действия офсетного контракта, а после его истечения перерегистрацию цен на ЛП следует осуществлять на общих условиях. В качестве альтернативного варианта может быть рассмотрена разработка и принятие в нормативном правовом поле типовой формы офсетного контракта, предусматривающего в том числе регулирование в части изменений объема закупаемой продукции по соглашению сторон в большем объеме, чем это предусмотрено ФЗ-44 на сегодняшний день.
Такой инструмент и условия необходимы для случаев, если фактически установлено наличие более экономически эффективного ЛП для заказчика офсетного контракта и наличия возможностей для поставщика (инвестора) требовать соразмерного увеличения объема закупок, гарантируемых заказчиком.
Как известно, на текущий момент принят Федеральный закон от 30.01.2024 № 1-ФЗ4, посвященный гармонизации регулирования обращения лекарственных средства на рынке ЕАЭС, который в том числе ввел принцип обоснования орфанности заболевания, не отнесенного в соответствии с Федеральным законом от 21 ноября 2011 года № 323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации» (далее – ФЗ-323)5 к редким (орфанным) заболеваниям, а также ввел необходимость предоставления подробной информации о диагностике, профилактике или лечении такого заболевания. Представляется целесообразным предусмотреть возможность прохождения ускоренной процедуры экспертизы ЛС в целях государственной регистрации ЛП, включая государственную регистрацию и перерегистрацию предельных отпускных цен производителей на ЛП, включенные в перечень ЖНВЛП, производство которых создается, модернизируется и осваивается по офсетному контракту. При этом, безусловно, применение ускоренных процедур не должно сказываться на качестве, глубине оценки эффективности и безопасности фармацевтической продукции, а также приводить к созданию угрозы нарушения исключительных прав на изобретения.
Офсетные контракты – клинические рекомендации и стандарты лечения. В силу реализации норм п. 15 ст. 37 ФЗ-323, назначение и применение ЛП, медицинских изделий и специализированных продуктов лечебного питания, не входящих в соответствующие стандарты оказания медицинской помощи или не предусмотренных клиническими рекомендациями, допускаются только при наличии определенных показаний (индивидуальной непереносимости, по жизненным показаниям) по решению врачебной комиссии. Применительно к рискам, возникающим при исполнении офсетных контрактов, отметим, что наличие обязательств по приобретению произведенных или изготовленных ЛП (ст. 56 ФЗ-61) в рамках офсетного контракта не синхронизировано с наличием такого ЛП в стандартах оказания медицинской помощи и клинических рекомендациях. Текущая практика локализации ЛП в рамках офсетных контрактов ориентируется исключительно на ЛП, входящие в перечень ЖНВЛП, что проистекает из текущего регулирования – возможности использования средств бюджетов субъектов Российской Федерации. В случаях исключения ЛП из перечня ЖНВЛП, соответствующих стандартов оказания медицинской помощи и клинических рекомендаций возникает или может возникнуть ситуация, когда субъекты Российской Федерации продолжают нести обязанность по его закупке, однако медицинские организации не могут или не смогут назначать и применять необходимый вид лекарственной терапии иначе, чем по решению врачебной комиссии. Синхронизация положений ФЗ-44, ФЗ-61 и ФЗ-323 в этой части позволила бы как поставщику (инвестору), так и заказчику действовать при заключении и исполнении офсетного контракта в состоянии большей определенности, что положительно скажется на эффективности использования такого инструмента. При этом, в случае с обеспечением лиц с редкими заболеваниями, значительная часть видов необходимой лекарственной терапии не включена в перечень ЖНВЛП, что является определенной сложностью в части локализации данных видов ЛП с использованием указанного механизма.
На текущий момент Фонд поддержки детей с тяжёлыми жизнеугрожающими и хроническими заболеваниями, в том числе редкими (орфанными) заболеваниями «Круг добра» (далее – Фонд) располагает средствами, которые возможно направлять на необходимую помощь детям по всем нозологическим группам и формам редких заболеваний, в том числе относящихся к социальным гарантиям субъектов Российской Федерации по перечню жизнеугрожающих и хронических прогрессирующих редких заболеваний, приводящих к сокращению продолжительности жизни граждан или их инвалидности [1]. В то же время необходимо рассматривать дополнительные возможности, связанные с постепенным расширением помощи и лечения взрослых пациентов на федеральном уровне, включая тех подопечных Фонда, кто перешел рубеж 18 лет и переходного периода 19 лет.
Здесь также важно рассмотреть ряд вопросов, связанных с состоянием и тенденциями законодательно-нормативного регулирования применения лекарственных препаратов вне инструкции [2]. С учетом того, что изготавливаемые ЛП не подлежат государственной регистрации и регистрации в рамках общего рынка ЛС, представляется актуальным уточнение положений законодательства и определение уровня внедрения соответствующих положений по вопросам назначения и применения фактически вне инструкции по медицинскому применению и, главное, определение концептуальных основ как эффективности, безопасности изготавливаемых ЛП для взрослого и детского населения, так и непосредственных инструментов мониторинга за деятельностью производственных аптек, основываясь на принципах инспектирования.
Возможности снижения нагрузки на бюджеты субъектов Российской Федерации в части обеспечения лиц с редкими (орфанными) заболеваниями. Согласно пп. 10 ч. 1 ст. 16 ФЗ-323, к полномочиям органов государственной власти субъектов Российской Федерации в сфере охраны здоровья относится организация обеспечения граждан ЛП и специализированными продуктами лечебного питания для лечения заболеваний, включенных в перечень жизнеугрожающих и хронических прогрессирующих редких заболеваний, приводящих к сокращению продолжительности жизни или инвалидности, предусмотренный ч. 3 ст. 44 ФЗ-323 (далее – Перечень ПП РФ 403). При этом, согласно ч. 2 той же статьи «отправной точкой» является иной и более широкий перечень редких заболеваний, распространенных на территории РФ, который формируется уполномоченным федеральным органом исполнительной власти (Минздравом России) на основании статистических данных и размещается на его официальном сайте в сети «Интернет»6. Именно на основании последнего осуществляется выборка и Правительством Российской Федерации утверждается Перечень ПП РФ 403. Финансовое обеспечение граждан зарегистрированными ЛП для лечения заболеваний, включенных в Перечень ПП РФ 403 (за исключением заболеваний, указанных в п. 21 ч. 2 ст. 14 ФЗ-323), осуществляется за счет средств бюджетов субъектов Российской Федерации, в рамках постановления Правительства Российской Федерации от 26 апреля 2012 г. № 4037.
По состоянию на 09 апреля 2024 года размещено два перечня редких заболеваний, распространенных на территории РФ8 и содержащих 265 и 267 групп и нозологических форм, которым присвоен соответствующий код Международной классификации заболеваний (МКБ-10). Наряду с этим еще 16 октября 2023 года9 была размещена форма «Информация для внесения заболевания в Перечень редких заболеваний для размещения на официальном сайте Министерства здравоохранения Российской Федерации», а также перечень редких заболеваний, распространенных на территории РФ, содержащих 282 группы и нозологические формы. По состоянию на 06 августа 2024 года, в данном перечне содержится 291 заболевание [3].
Как было указано ранее, данные перечни являются статистическими и не предполагают за собой государственных гарантий. Для пациентов, которым диагностировано заболевание из этих перечней, в настоящий момент отсутствуют нормативно закрепленные государственные гарантии по льготному лекарственному обеспечению. Исключением является единственный случай, когда пациент относится к одной из категорий «федеральных льготников», определенных ст. 6.1 Федерального закона от 17 июля 1999 г. № 178-ФЗ10, обладающих правом на получение государственной социальной помощи в виде набора социальных услуг. При этом очевидно, что текущих и направляемых средств из федерального бюджета недостаточно: 01 февраля 2024 года норматив финансовых затрат установлен на уровне 1211,3 рубля в месяц на одного федерального льготника11, что приводит к необходимости привлечения средств бюджетов субъектов РФ для реализации данных социальных гарантий.
Одновременно с этим, для обеспечения пациентов с редкими заболеваниями льготными ЛП, которые входят в соответствующие стандарты оказания медицинской помощи в объеме не менее, чем это предусмотрено перечнем ЖНВЛП, существует ряд программ и источников финансирования:
- региональные бюджеты в рамках постановления Правительства Российской Федерации от 26 апреля 2012 г. № 403 (на текущий момент 17 редких нозологических групп и форм);
- бюджеты в рамках программы ВЗН, которая состоит из средств федерального бюджета (12 из 14 нозологий относятся к редким заболеваниям, обеспечение которых осуществляется по 34 международным непатентованным наименованиям (МНН)), также с 1 января 2023 года из средств Фонда (по программе ВЗН для детей в возрасте до 18 лет);
- средства Фонда (58 из 84 тяжелых жизнеугрожающих и хронических заболеваний относятся к редким заболеваниям, по которым обеспечиваются лица до 19 лет по 67 из 68 МНН соответственно, а также незарегистрированными ЛП на территории РФ по 26 МНН12).
Кроме того, наблюдается значительное количество пересечений обеспечения ЛП льготных категорий граждан с редкими (орфанными) заболеваниями в структуре источников финансирования, например, муковисцидоз [4]. С другой стороны, финансирование несовершеннолетних граждан, страдающих муковисцидозом, осуществляется за счет средств бюджетов субъектов РФ по рецептам врачей бесплатно и с 50-процентной скидкой, согласно постановлению Правительства РФ от 30 июля 1994 № 89013, а также в соответствии с региональными нормативными правовыми актами, определяющими гарантии субъекта РФ. Так, например, в соответствии с Законом Санкт-Петербурга от 22 ноября 2011 г. № 728-13214 за счет средств регионального бюджета устанавливаются различные меры социальной поддержки для обеспечения ЛП пациентов, страдающих муковисцидозом, вне зависимости от возраста. Следовательно, в зависимости от финансовых возможностей каждого субъекта РФ, могут формироваться различные объемы социальных гарантий и значительная группа нуждающихся граждан, не включенных в действующие льготные программы и формуляры федерального и регионального уровней ввиду отсутствия унификации.
Текущие подходы в отношении обеспечения лиц с редкими заболеваниями приводят к поликомпонентности, множественности источников финансирования и в целом неопределенности, а также возникновению случаев, когда в рамках разных программ, в том числе программы ВЗН, пациенты обеспечиваются теми же ЛП. В результате мы наблюдаем факты правового дисбаланса и дискриминации льготных категорий граждан по признаку заболевания, что не отвечает принципам социально ориентированного государства, которым, безусловно, является Российская Федерация.
Комплексно рассматривая сложившуюся практику, мы полагаем, что возникновение угрозы невыполнения возложенных на органы государственной власти субъектов РФ в сфере охраны здоровья полномочий по обеспечению лиц с редкими заболеваниями заключается в том, что общий принцип допуска на рынок высокозатратных ЛП неэффективен: за принятые решения об обеспечении пациентов орфанными ЛП, обладающими эксклюзивным статусом и высокой стоимостью, в последующем в ряде случаев ответственность несут именно субъекты РФ, что приводит к снижению качества функционирования системы лекарственного обеспечения и нарушению конституционного принципа равенства в части доступности ряда ЛП для пациентов.
Вместе с тем растет количество судебных дел и решений в отношении полномочий органов государственной власти субъектов РФ в данной сфере лекарственного обеспечения, а для пациентов обращение в суд, фактически, является способом получить необходимую лекарственную терапию. Также сохраняются вопросы эффективности использования бюджетных ресурсов при необходимости перераспределения закупленных объемов ЛП между субъектами РФ. Органы государственной власти субъектов РФ остаются без каких-либо возможностей управления и формирования инструментария для оптимизации затрат в данных сегментах ЛП. В целом, в рамках всеобщей системы лекарственного обеспечения, данная практика не является эффективной для надлежащего исполнения полномочий органов государственной власти субъектов РФ в сфере охраны здоровья и организации обеспечения граждан ЛП для лечения заболеваний, включенных в Перечень ПП РФ 403.
Стоит признать, что сложившаяся практика отражается в нарастающей и сохраняющейся высокой нагрузке на бюджеты субъектов РФ, в том числе влияя на увеличение объема государственного долга субъектов РФ по бюджетным кредитам, необходимость списания которых на 2/3 задолженности озвучено Президентом Российской Федерации В.В. Путиным 29 февраля 2024 года в рамках ежегодного послания к Федеральному Собранию Российской Федерации15.
Несмотря на то, что ст. 31 Федерального закона от 31 июля 1998 г. № 145-ФЗ16 установлены принципы самостоятельности бюджетов, где органы государственной власти субъектов РФ наделены правом и обязанностью самостоятельно осуществлять бюджетный процесс, определять направления своих расходных обязательств с учетом имеющихся доходных источников, ряд субъектов РФ не способен выдержать высокую финансовую нагрузку, что не позволяет в полной мере исполнять возложенные на них обязательства по финансированию закупок необходимых ЛП в полном объеме. Позиция Минфина России по вопросу передачи полномочий по лекарственному обеспечению лиц с редкими заболеваниями на федеральный уровень также исходит из текущих норм разграничения полномочий в области лекарственного обеспечения населения17 и может быть рассмотрена только с учетом перераспределения бюджетных источников, а также, вероятно, будет взаимоувязана с новыми подходами при модернизации действующей фискальной системы, позволяющей перейти к более справедливой и дифференцированной системе налогообложения – развитию прогрессивной шкалы, введенной с 1 января 2021 года.
Говоря о решении общих задач как для системы здравоохранения, так и промышленности России, в отношении редких заболеваний предоставление финансовой поддержки из федерального бюджета в виде дотаций бюджетам субъектов Российской Федерации также не позволяет эффективным образом реализовать централизацию потребности в ЛП и достичь высокого уровня оптимизации затрат, поскольку каждому региону нецелесообразно формировать самостоятельные офсетные контракты, так как высока вероятность того, что не будет определен поставщик (исполнитель) на сформированные объемы в виде минимального количества товара, возможность производства которого может быть обеспечена создаваемым, модернизируемым, осваиваемым производством. Однако, говоря о минимальных объемах услуги, возможность оказания которой может быть обеспечена с использованием создаваемого, реконструируемого имущества (недвижимого имущества или недвижимого имущества и движимого имущества, технологически связанных между собой), гиперлокальная (региональная) фармацевтическая инфраструктура в сфере изготовления ЛП способна обеспечивать потребности субъектов РФ, что автоматически приведет к вопросам доступа к сырью фармацевтического качества, прежде всего к фармацевтическим субстанциям, произведенным для реализации и включенным в государственный реестр лекарственных средств. В связи с этим при разработке комплекса согласованных мер по разрешению сложившейся ситуации в части лекарственного обеспечения пациентов с редкими заболеваниями должны найти свое отражение предложения о возможных мерах повышения доступности фармацевтического сырья для производственных аптек (рассмотрено далее). Таким образом, текущий децентрализованный подход не предоставляет возможностей для органов государственной власти субъектов РФ и не позволяет повысить эффективность при осуществлении:
- закупок по целому ряду востребованной медицинской продукции, в том числе необходимых ЛП, приобретаемых Минздравом России или подведомственным ему казенным учреждением как для взрослых, так и для детей, в том числе для целей деятельности Фонда;
- закупок Фонда по перечням не зарегистрированной на территории РФ медицинской продукции, в том числе необходимых ЛП.
Представляется целесообразным передать полномочия субъектов РФ на федеральный уровень в части финансового обеспечения граждан зарегистрированными в установленном порядке на территории Российской Федерации ЛП для лечения заболеваний, включенных в Перечень ПП РФ 403 (за исключением заболеваний, указанных в п. 21 ч. 2 ст. 14 ФЗ-323), в частности, в адрес Фонда.
Отметим, что при Фонде создан и успешно функционирует Экспертный совет, который является постоянно действующим консультативным органом, наделенным полномочиями по утверждению перечня тяжелых жизнеугрожающих и хронических заболеваний и перечня категорий детей с указанными заболеваниями, формированию перечней медицинской продукции, в том числе востребованных ЛП. Экспертный совет компетентен принимать решения о формировании резерва ЛП, рассматривать заявки об оказании медицинской помощи. Федерализация обеспечения лиц, страдающих жизнеугрожающими и хроническими прогрессирующими редкими заболеваниями, приводящими к сокращению продолжительности жизни и инвалидности, позволит упорядочить принципы лекарственного обеспечения и приведет к гармонизации текущих излишне диверсифицированных источников финансирования.
Реализация данных предложений возможна посредством внесения изменений в Указ № 16, Устав Фонда, а также внесение изменений в ФЗ-323, в частности, по отношению к порядкам обеспечения лиц с редкими заболеваниями, включая положения ст. 83, а также внесение изменений в ст. 44 в части передачи полномочий Фонду по формированию перечня редких заболеваний на основании статистических данных, размещения его на официальном сайте в сети «Интернет», что при комплексном подходе позволит:
- повысить качество и надлежащим образом структурировать категории редких заболеваний и потребности как взрослого, так и детского населения;
- создать и развить Федеральный персонифицированный регистр, включающий актуализируемый перечень редких заболеваний с привязкой к конкретным видам востребованной медицинской продукции, в том числе ЛП, что станет основой для прогнозирования соответствующих потребностей, планирования бюджетов на плановый период и долгосрочную перспективу, а также будет основой для совершенствования перечня стратегически значимых лекарственных средств и перечня критической промышленной продукции в отрасли фармацевтической промышленности Российской Федерации;
- разработать и внедрить единые процедуры закупки и обеспечения пациентов с редкими заболеваниями;
- ввести единую систему учета и централизовать отчетность Фонда в адрес Минздрава России, в том числе в рамках Единой информационной системы в сфере здравоохранения и закупок, включая соответствующие подсистемы;
- обеспечить стабилизацию стремительно растущих государственных затрат в сегменте орфанных ЛП, производителями и поставщиками которых являются компании из перечня иностранных государств и территорий, совершающих в отношении Российской Федерации, российских юридических лиц и физических лиц недружественные действия, утвержденный распоряжением Правительства Российской Федерации от 5 марта 2022 г. № 430-р18;
- усовершенствовать законодательство в сфере охраны здоровья граждан, страдающих редкими заболеваниями, и оказания им медицинской помощи в виде лекарственного обеспечения независимо от финансовой обеспеченности субъекта РФ, в котором они проживают;
- снизить финансовую нагрузку на бюджеты субъектов РФ и направить высвободившиеся средства субъектов на улучшение оказания медицинской помощи и лекарственного обеспечения для льготных категорий граждан;
- сформировать долгосрочную потребность, определить для фармацевтической отрасли стратегические, критически значимые цели и задачи по номенклатуре и уровню локализации медицинской продукции, в том числе необходимых ЛП.
Возможности повышения доступности и внедрения методов персонализированной медицины посредством реализации офсетных контрактов в сфере изготовления лекарственных препаратов. Наряду с заключением офсетных контрактов на поставку ЛП с фармацевтическими производителями, целесообразно рассматривать возможность заключения офсетных контрактов с аптечными или медицинскими организациями, имеющими в своей структуре производственные аптеки, посредством заключения государственных контрактов на оказание услуг (выполнение работ – в случае внесения изменений в ст. 1114 ФЗ-44) по изготовлению и отпуску ЛП, включающих встречные инвестиционные обязательства по созданию соответствующей высокотехнологичной инфраструктуры аптечных и медицинских организаций или реконструкции имущества (недвижимого имущества или недвижимого имущества и движимого имущества, технологически связанных между собой) [5, 6].
Ключевым преимуществом создания и развития современной, высокотехнологичной инфраструктуры (производственных аптек) является способность предоставить новые возможности для медицинской (клинической) практики за счет вариативности состава, доступности широкого диапазона дозировок, лекарственных форм, потенциального снижения нежелательных реакций и побочных действий, включая реализацию возможностей врачей по управлению длительностью курса лекарственной терапии. Дополнительно возможно рассматривать реализацию инструментов по оперативному устранению рисков возникновения дефектуры или дефицита ЛП. Вместе с тем в ряде случаев можно достичь оптимизации затрат бюджетов всех уровней, включая средства граждан на зарегистрированные готовые лекарственные формы за счет перехода на персонализированные (индивидуальные) курсы лечения, что повышает качество оказываемой медицинской и фармацевтической помощи.
Источником финансирования закупки услуг (работ) по изготовлению ЛП и внутриаптечной фасовке зарегистрированных ЛП для обеспечения потребностей медицинских организаций на территории субъектов РФ в рамках офсетных контрактов может являться как бюджет субъекта РФ, так и федеральный бюджет. В связи с тем, что Правительство субъекта РФ не распоряжается средствами территориальных фондов обязательного медицинского страхования, но в соответствии с п. 4 ст. 26 ФЗ-323 осуществляет платежи на дополнительное финансовое обеспечение реализации территориальной программы обязательного медицинского страхования в пределах базовой программы обязательного медицинского страхования, представляется целесообразным рассмотреть возможность выработки механизма заключения офсетных контрактов, согласовав данные решения с Федеральным фондом обязательного медицинского страхования (рис. 7).
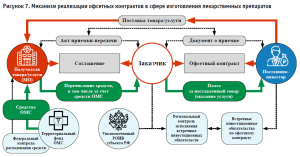
На сегодняшний день актуальными и востребованными направлениями в части удовлетворения индивидуальных потребностей пациентов и клинической практики являются:
- обеспечение изготовления и повышение доступности «традиционного ассортимента» изготовленных ЛП;
- обеспечение изготовления и повышение доступности ЛП, применяющихся при оказании педиатрической и неонатальной медицинской помощи;
- обеспечение изготовления и повышение доступности противоопухолевых лекарственных препаратов и иммуномодуляторов, в том числе применяющихся при оказании медицинской помощи взрослому и детскому населению по профилю «Онкология»;
- обеспечение изготовления и повышение доступности орфанных ЛП;
- развитие инфраструктуры для осуществления внутриаптечной (индивидуальной) фасовки зарегистрированных ЛП из крупных (балк) фасовок с целью перехода к учету курсовых доз, в том числе в рамках амбулаторного отпуска и льготного лекарственного обеспечения.
Например, потребность по номенклатуре индивидуально изготавливаемых ЛП, востребованных в педиатрической и неонатологической практике, включает 259 лекарственных форм, изготавливаемых на основе 215 МНН (из них 11 комбинаций МНН), из которых педиатрами отмечался высокий спрос на 193 лекарственные формы на основе 139 МНН (из них 7 комбинаций МНН), неонатологами отмечается высокая востребованность 50 лекарственных форм на основе 36 МНН (из них 1 комбинация МНН). Для целей уточнения потребности в объеме оказания услуг (работ) по изготовлению ЛП и внутриаптечной фасовке зарегистрированных ЛП потребуется привлечение главных внештатных специалистов Минздрава России и органов государственной власти субъектов РФ в сфере здравоохранения.
Выводы
Перед Российской Федерацией стоит важнейшая задача по повышению национальной лекарственной безопасности с целью улучшения состояния здоровья граждан и снижения доли импортируемых ЛП, закупаемых за счет бюджетов всех уровней. В сфере обеспечения лекарственной безопасности ряд стратегических документов федерального и регионального уровней содержат основные императивы, связанные с обеспечением поддержки развития и создания современной фармацевтической инфраструктуры по наиболее актуальным и востребованным ЛП, в том числе ЛП, производство которых должно быть обеспечено по «полному циклу».
Представленные в виде двух взаимосвязанных работ результаты относятся к сфере развития системы здравоохранения, лекарственного обеспечения, осуществлению фармацевтической деятельности и производства лекарственных средств на территории Российской Федерации, реализации промышленной и инновационной политики, а также соответствующих областей государственного регулирования. Развитие механизма офсетных контрактов позволяет успешно стимулировать кооперацию и выстраивание производственно-технологических цепочек, в том числе в фармацевтической отрасли.
Реализация разработанных предложений позволит:
- значительно увеличить масштаб и сферы применения офсетных контрактов, в том числе за счет их федерализации;
- обеспечить согласованность между ценами на ЛП, зафиксированными в офсетном контракте, и предельными отпускными ценами, зарегистрированными в соответствии с ФЗ-61;
- синхронизировать обязательства закупки ЛП по офсетным контрактам с их включением в стандарты оказания медицинской помощи и клинические рекомендации;
- оптимизировать затраты бюджетов всех уровней на закупку орфанных ЛП и существенно увеличить количество обеспеченных граждан;
- разработать и внедрить новые формы осуществления закупок в сфере лекарственного обеспечения, а также расширить ответственность поставщиков инновационных ЛП перед национальной системой здравоохранения РФ;
- расширить возможности и практику применения офсетных контрактов, в том числе на изготавливаемые ЛП.
___________________________________________________________________________
1 Федеральный закон от 5 апреля 2013 г. № 44-ФЗ «О контрактной системе в сфере закупок товаров, работ, услуг для обеспечения государственных и муниципальных нужд». URL: https://docs.cntd.ru/document/499011838 (дата обращения: 26.03.2024 г.)
2 Федеральный закон от 12 апреля 2010 г. № 61-ФЗ «Об обращении лекарственных средств». URL: https://docs.cntd.ru/document/902209774 (дата обращения: 15.04.2024).
3 Постановление Правительства Российской Федерации от 29 октября 2010 г. № 865 «О государственном регулировании цен на лекарственные препараты, включенные в перечень жизненно необходимых и важнейших лекарственных препаратов» и иных нормативных правовых актах. URL: https://docs.cntd.ru/document/902243056 (дата обращения: 15.04.2024).
4 Федеральный закон от 30.01.2024 N 1-ФЗ «О внесении изменений в Федеральный закон “Об обращении лекарственных средств”» и статьи 1 и 4 Федерального закона «О внесении изменений в Федеральный закон “Об обращении лекарственных средств”» и Федеральный закон «О внесении изменений в Федеральный закон “Об обращении лекарственных средств”». URL: https://docs.cntd.ru/document/1304778181
5 Федеральный закон от 21 ноября 2011 г. № 323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации». URL: https://docs.cntd.ru/document/902312609 (дата обращения: 15.05.2024)
6 URL: https://minzdrav.gov.ru/documents/9641-perechen-redkih-orfannyh-zabolevaniy.
7 Постановление Правительства Российской Федерации от 26 апреля 2012 г. № 403 «О порядке ведения Федерального регистра лиц, страдающих жизнеугрожающими и хроническими прогрессирующими редкими (орфанными) заболеваниями, приводящими к сокращению продолжительности жизни граждан или их инвалидности, и его регионального сегмента». URL: https://docs.cntd.ru/document/902344557.
8 URL: https://minzdrav.gov.ru/documents/9641-perechen-redkih-orfannyh-zabolevaniy.
10 Федеральный закон от 17 июля 1999 г. № 178-ФЗ «О государственной социальной помощи». URL: https://docs.cntd.ru/document/901738835 (дата обращения: 16.04.2024).
11 Постановление Правительства Российской Федерации от 11 апреля 2024 г. № 454 «Об установлении норматива финансовых затрат в месяц на одного гражданина, получающего государственную социальную помощь в виде социальной услуги по обеспечению в соответствии со стандартами медицинской помощи по рецептам врача (фельдшера) лекарственными препаратами для медицинского применения, медицинскими изделиями, а также специализированными продуктами лечебного питания для детей-инвалидов в 2024 году». URL: https://www.consultant.ru/document/cons_doc_LAW_474601/ (дата обращения: 16.04.2024).
12 На дату проведения исследования: 15 апреля 2024 г.
13 Постановление Правительства РФ от 30 июля 1994 г. № 890 «О государственной поддержке развития медицинской промышленности и улучшении обеспечения населения и учреждений здравоохранения лекарственными средствами и изделиями медицинского назначения». URL: https://docs.cntd.ru/document/9006396 (дата обращения: 15.04.2024).
14 Закон Санкт-Петербурга от 22 ноября 2011 г. № 728-132 «Социальный кодекс Санкт-Петербурга». URL: https://docs.cntd.ru/document/891859785 (дата обращения: 15.04.2024).
15 URL: http://kremlin.ru/events/president/news/73585.
16 Федеральный закон от 31 июля 1998 г. № 145-ФЗ «Бюджетный кодекс Российской Федерации» URL: https://docs.cntd.ru/document/901714433 (дата обращения: 15.04.2024).
17 URL: https://www.kommersant.ru/doc/6648505.
18 Распоряжение Правительства Российской Федерации от 5 марта 2022 г. № 430-р «О перечне иностранных государств и территорий, совершающих в отношении Российской Федерации, российских юридических лиц и физических лиц недружественные действия». URL: https://docs.cntd.ru/document/728367755 (дата обращения: 15.04.2024).
- Захарочкина Е.Р., Ряженов В.В., Смолярчук Е.А., Кудлай Д.А., Бехорашвили Н.Ю., Заверячев С.А., Сологова С.С. Cостояние и тенденции законодательно-нормативного регулирования применения лекарственных препаратов вне инструкции. Терапевтический архив. 2024; 96(4): 396–406. DOI: 10.26442/00403660.2024.04.202692
- Отчет Фонда «Круг добра» за 2023 год // Фондкругдобра.рф URL: https://static-0.minzdrav.gov.ru/system/attachments/attaches/000/067/051/original/%C2%AB%D0%9A%D1%80%D1% 83%D0%B3_%D0%B4%D0%BE%D0%B1%D1%80%D0%B0%C2%BB_2023_%D0%B3%D0%BE%D0% B4.pdf?1719317950 (дата обращения: 25.06.2024).
- Перечень редких (орфанных) заболеваний, Минздрав России, 31 мая 2024, № б/н.– URL: https://minzdrav.gov.ru/documents/9774-perechen-redkih-orfannyh-zabolevaniy
- Юрочкин Д.С., Мамедов Д.Д., Эрдни-Гаряев С.Э., Махова О.А., Молчанова C.Ю. О направлениях совершенствования механизма заключения долгосрочных контрактов со встречными инвестиционными обязательствами. Часть 1 – пути федерализации офсетных контрактов // Вестник Росздравнадзора. – 2024. – № 3. – С. 6–21.
- Кондратьева Е.И., Воронкова А.Ю., Каширская Н.Ю., Красовский С.А., Старинова М.А., Амелина Е.Л., Авдеев С.Н., Куцев С.И. Российский регистр пациентов с муковисцидозом: уроки и перспективы // Пульмонология. – 2023. – № 33 (2). – С. 171–181. DOI: 10.18093/0869-0189-2023-33-2-171-181.
- Основы формирования единой гармонизированной системы нормативного правового регулирования в области обращения лекарственных препаратов, изготавливаемых аптечными организациями: Монография / И.А. Наркевич, В.С. Фисенко, З.М. Голант, Д.С. Юрочкин, Д.Д. Мамедов, С.Э. Эрдни-Гаряев, А.А. Лешкевич. – СПб.: Медиапапир, 2023. – 292 с. – ISBN 978-5-00110-344-8. – EDN PZEVDF.
- Фаррахов А.З., Соломатина Т.В., Мамедов Д.Д., Юрочкин Д.С., Голант З.М., Наркевич И.А. Основы формирования стратегии развития сегмента изготовления и отпуска лекарственных препаратов в Российской Федерации // Вестник Росздравнадзора. – 2023. – № 6. – С. 6–17. – EDN NANOAC.
