КЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ
Модель прогнозирования клинических и экономических последствий окклюзии лучевой артерии после диагностических и лечебных коронарных вмешательств
1 — ФБОУ ВО «Российская академия народного хозяйства и государственной службы при президенте Российской Федерации», 119571, Российская Федерация, г. Москва, просп. Вернадского, д. 82.
dr.ognerubov@gmail.com
ORCID: https://orcid.org/0000-0002-4781-2773
2 — ФГАОУ ВО «Национальный исследовательский университет ИТМО», 197101, Российская Федерация, г. Санкт-Петербург, Кронверкский проспект, д. 49, лит. А.
gbeh@list.ru
ORCID: https://orcid.org/0009-0006-1995-3890
3 — ФГАОУ ВО «Национальный исследовательский университет ИТМО», 197101, Российская Федерация, г. Санкт-Петербург, Кронверкский проспект, д. 49, лит. А.
kalindan12@mail.ru
ORCID: https://orcid.org/0009-0002-6082-5680
4 — ФБОУ ВО «Российская академия народного хозяйства и государственной службы при президенте Российской Федерации», 119571, Российская Федерация, г. Москва, просп. Вернадского, д. 82.; ФГБОУ ДПО РМАНПО Минздрава России, 125993, Российская Федерация, г. Москва, ул. Баррикадная, д. 2/1, стр. 1.; ФГБУ «Информационно-методический центр по экспертизе, учету и анализу обращения средств медицинского применения» Федеральной службы по надзору в сфере здравоохранения, 109012, Российская Федерация, г. Москва, Славянская площадь, д. 4. стр.1.
eaberseneva@gmail.com
ORCID: https://orcid.org/0000-0003-3481-6190
5 — ФГБУ «Национальный медицинский исследовательский центр кардиологии имени академика Е.И. Чазова» Министерства здравоохранения Российской Федерации, 121552, Российская Федерация, г. Москва, ул. Академика Чазова, д. 15а.
vrv280699@gmail.com
ORCID: https://orcid.org/0009-0006-4453-8621
6 — ФГБУ «Национальный медицинский исследовательский центр кардиологии имени академика Е.И. Чазова» Министерства здравоохранения Российской Федерации, 121552, Российская Федерация, г. Москва, ул. Академика Чазова, д. 15а.
semaver@yandex.ru
ORCID: https://orcid.org/0000-0002-7936-3634
7 — ФГБУ «Национальный медицинский исследовательский центр кардиологии имени академика Е.И. Чазова» Министерства здравоохранения Российской Федерации, 121552, Российская Федерация, г. Москва, ул. Академика Чазова, д. 15а.
samkoan@mail.ru
ORCID: https://orcid.org/0000-0003-1808-3484
8 — ФГБУ «Национальный медицинский исследовательский центр кардиологии имени академика Е.И. Чазова» Министерства здравоохранения Российской Федерации, 121552, Российская Федерация, г. Москва, ул. Академика Чазова, д. 15а.
ev.merkulov@list.ru
ORCID: https://orcid.org/0000-0001-8193-8575
В настоящей работе представлено описание прогностической модели окклюзии лучевой артерии, разработанной на основе методов машинного обучения, для применения после внутрисосудистых диагностических и лечебных коронарных вмешательств. Данная модель демонстрирует высокую точность прогнозирования риска окклюзии лучевой артерии, опираясь на комплексную систему предикторов, включающую такие клинически значимые факторы, как сахарный диабет 2 типа, демографические характеристики (пол, возраст), антропометрические параметры (вес, рост), а также поведенческие и медицинские анамнезы (курение, артериальная гипертензия). Полученные результаты имеют значительный потенциал для клинической практики, способствуя ранней диагностике и оптимизации терапевтических стратегий для пациентов с окклюзией лучевой артерии, что, в свою очередь, помогает улучшить качество и продолжительность их жизни.
Ключевые слова: окклюзия лучевой артерии, ишемическая болезнь сердца, чрескожное коронарное вмешательство, коронароангиография, феморальный доступ
Введение
Ишемическая болезнь сердца (ИБС) считается одной из основных причин заболеваемости и смертности в развитых странах. Хотя за последние семь десятилетий смертность от ИБС во всем мире снизилась, она по-прежнему является причиной трети и более всех смертей у лиц старше 55 лет [1]. Коронароангиография стала золотым стандартом диагностики и определения стратегии лечения атеросклеротического поражения коронарных артерий.
Коронароангиография может быть выполнена через бедренную, лучевую или локтевую артерии. Общая бедренная артерия долгое время была стандартным местом доступа для проведения коронарной ангиографии и чрескожного коронарного вмешательства (ЧКВ). Однако осложнения в месте доступа, такие как кровотечение, гематома, артериовенозная фистула и псевдоаневризма, не являются редкостью после процедур с использованием феморальной артерии [2]. Осложнения кровотечения связаны с повышенным риском смерти, инфаркта миокарда (ИМ), инсульта, тромбоза стента и увеличением стоимости вмешательства [3].
Лучевая артерия анатомически более доступна для гемостаза, чем бедренная. Она лежит на площадке лучевой кости и легко поддается компрессии снаружи [4]. Несмотря на многочисленные преимущества, лучевой доступ связан с определенными недостатками, такими как боль или сосудистые осложнения. Окклюзия лучевой артерии (ОЛА) является основным осложнением, ограничивающим использование доступа в будущем [5].
В ранних исследованиях частота окклюзии лучевой артерии после ангиографии варьировала от менее чем 1% до 33% [6]. Cтоит заметить, что, если в исследовании включались все пациенты и все операторы, независимо от опыта и используемых устройств во время вмешательства, частота ОЛА была 22,8% [7].
Лучевой доступ также снижает расходы стационара одновременно с уменьшением неблагоприятных последствий для пациентов [8]. Чистая экономия расходов всегда была в пользу лучевого доступа. Исследование Mitchel M.D. и соавт. показало, что чтобы довести чистую стоимость бедренного доступа до стоимости лучевого, потребовалось бы снижение всех осложнений катетеризации бедренной артерии более чем на 60 % [8].
Для поиска предикторов ОЛА традиционно в исследованиях [8,9] использовались методы логистической регрессии и многофакторный анализ. Однако сейчас есть возможность использовать более продвинутые методы машинного обучения для повышения ценности предсказательной модели окклюзии лучевой артерии. Таким образом, целью настоящего исследования было изучение предикторов окклюзии лучевой артерии и ее экономических последствий после КАГ и ЧКВ методами машинного обучения.
Материалы и методы
В рамках настоящего исследования были сформированы две когорты пациентов. В первую (n=1000) вошли пациенты, у которых в анамнезе выполнялись коронароангиография (КАГ) или чрескожное коронарное вмешательство (ЧКВ), и они были госпитализированы для проведения второго этапа вмешательства. Средний временной интервал между предыдущим вмешательством и госпитализацией, а также включением в исследование, составил 3,4±1,3 месяцев. Таким образом, окклюзия лучевой артерии в данной группе была диагностирована ретроспективно. Вторая когорта (n=1000) состояла из пациентов, которым были проведены КАГ и/или ЧКВ, после чего они были рандомизированы методом конвертов для получения различных сроков гемостаза: до пяти часов (n=500) и 12–24 часа (n=500). Из общего числа (1284) пациентов, включенных в проспективное исследование, 284 были исключены в соответствии с заранее установленными критериями отбора.
Всем пациентам выполнялось УЗИ артерий предплечья. Для поиска биохимических предикторов ОЛА были проанализированы уровни общего холестерина, холестерина липопротеидов низкой (ХС ЛНП) и высокой плотности (ХС ЛВП), триглицеридов в сыворотке крови.
Клинико-анамнестическая характеристика пациентов, включенных в исследование, представлена в таблицах 1 и 2.
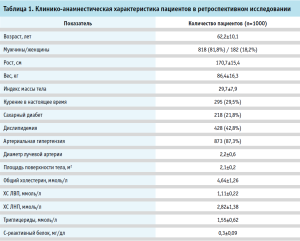
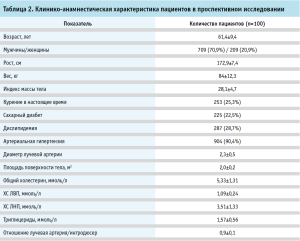
На основании полученных данных была разработана предсказательная модель ОЛА. В модель были включены 2000 пациентов. Выборки для обучения и тестирования модели были сформированы следующим образом: 1400 пациентов составили обучающую выборку, а оставшиеся 600 пациентов – тестовую выборку. Перед обучением моделей проводилась предобработка данных, включающая их нормализацию.
Для статистической обработки результатов был использован статистический пакет R 3.4.4 software (R Core Team, Vienna, Austria). Разведочный анализ данных производился в Python: для построения моделей использовался модуль Catboost 1.2.3, для проверки статистических гипотез – подмодуль stats библиотеки scipy 1.12.0. При сравнении для количественных характеристик, распределенных по нормальному закону, использовался t-критерий Стьюдента для независимых выборок. Для количественных характеристик, имеющих ненормальное распределение, использовался критерий Манна-Уитни. Для качественных характеристик использовался критерий χ2. Статистически значимыми считались различия при р < 0,05.
Многофакторный анализ проводился методом логистической регрессии с бинарной зависимой переменной (1 – нет события, 2 – есть событие). Для решения задачи классификации были использованы следующие модели машинного обучения: логистическая регрессия, метод случайного леса (Random Forest), простой вероятностный классификатор (Naive Bayes) ансамбля стохастического градиентного бустинга с открытым исходным кодом (LightGBM). Результаты оценки моделей по метрикам AUC (площадь под кривой (AUC), мера способности модели различать классы: 0 – нет окклюзии лучевой артерии, 1 – есть окклюзия лучевой артерии) и F1-мера:
F1-мера = 2 × (Точность × Отзыв) / (Точность + Отзыв),
где:
Точность – правильные положительные прогнозы окклюзии лучевой артерии по отношению к общему количеству окклюзий;
Отзыв – истинное число предсказанных окклюзий лучевой артерии по отношению к общему количеству фактических окклюзий).
При значении AUC ≤ 0,5 предсказательная способность классификатора считается неудовлетворительной.
Была выявлена проблема дисбаланса классов, что снижало производительность моделей. Для решения данной проблемы был применен метод увеличения числа примеров миноритарного класса SMOTE (Synthetic Minority Over-sampling Technique).
Результаты
Частота ОЛА в группе ретроспективного анализа составила 21,8% (n = 218). При анализе в ретроспективной группе у пациентов без ОЛА стоимость вмешательства была 81,2 тыс. рублей (95% ДИ 75,5–87,5), а с ОЛА – 96,7 (95% ДИ 86,1– 100,9). Расчет доверительных интервалов производился с использованием bootstrap. Между выборками наблюдается статистически значимая разница (p = 0.0027, Mann-Whitney U test)
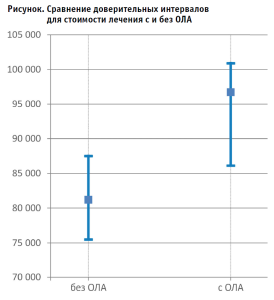
Частота окклюзии лучевой артерии при методике короткого гемостаза составила 1,4%, при традиционном – 10,1% (р < 0,01). В группе ретроспективного контрольного исследования частота окклюзии лучевой артерии составила 21,6%.
Методом логистической регрессии был выполнен поиск факторов, связанных с ОЛА. В модель были включены данные о росте, весе, поле пациента, наличии курения, сахарного диабета 2 типа и артериальной гипертензии. Площадь под кривой при анализе (AUC) = 0.73, F1-мера = 0.65. Метод случайного леса (Random Forest) показал AUC = 0.74, F1-мера = 0.69. Простой вероятностный классификатор (Naive Bayes): AUC = 0.83, F1-мера = 0.67. Градиентный бустинг (LightGBM): AUC = 0.8625, F1-мера = 0.8563.
После применения SMOTE (аугментации) модель LightGBM показала результаты с AUC = 0.893 и F1-мерой = 0.87. Градиентный бустинг (catboost) без SMOTE: AUC = 0.922, F1-мера = 0.75.
Обсуждение
Исследования I. Bernat и соавторов демонстрируют, что факторы риска, ассоциированные с окклюзией лучевой артерии (ОЛА), можно классифицировать на модифицируемые и немодифицируемые [9]. К немодифицируемым факторам риска относятся несколько исходных характеристик пациента, включая возраст, женский пол, низкий индекс массы тела, диабет, этническую принадлежность (в частности, южноазиатское происхождение) и предыдущие вмешательства через лучевую артерию [8]. Процедурные факторы риска включают повторные неудачные попытки радиальных пункций, увеличенное соотношение оболочки к артерии, отсутствие предварительной обработки аспирином, отсутствие или низкие дозы перипроцедурной внутрисосудистой антикоагуляции, окклюзионный («непроходимый») гемостаз и более длительное время гемостаза [10, 11]. В результирующую модель настоящего исследования вошло несколько факторов: наличие сахарного диабета 2 типа, курения, артериальной гипертензии, пол, вес, рост, возраст.
В недавно опубликованном анализе Applegate et al. оценивались затраты, связанные с ТР и ТФ-коронарографией [12]. Радиальная стратегия ассоциировалась с выгодой в 228 долларов США на процедуру для одного пациента (лучевой доступ: 8888 ± 7994 долларов США и феморальный доступ: 9116 ± 8299 долларов США). Ретроспективный анализ данных 20% всех первичных ЧКВ, собранных в американском регистре PREMIER, показал аналогичные результаты [13]. Общие внутрибольничные расходы были на 553 доллара ниже в группе лучевого доступа [11 736 долларов США (95% ДИ: 11 200 – 12 272 долларов США) и 12 288 долларов США у феморального доступа (95% ДИ: 12 102 – 12 474 долларов США), p=0,03].
Авторами настоящего исследования было дополнительно установлено, что наличие у пациента окклюзии хотя бы одной лучевой артерии повышает стоимость будущего вмешательства на 15,4 тыс. рублей.
Традиционно в медицинских исследованиях используется метод логистической регрессии для построения предсказательных моделей ОЛА. В работе S. Zhang и соавт. предсказывали наличие ишемической болезни сердца по результатам общих и биохимических анализов крови, при этом использовали ансамбль стохастического градиентного бустинга с аугментацией данных [14]. Эти методы значительно улучшили эффективность классификации классификатора логистической регрессии с точки зрения точности, запоминания, точности, F1 меры и AUC при использовании для обнаружения ИБС. Лучшие показатели точности, запоминания, F1 мера, AUC составили 94,7%, и 0,98, соответственно. В нашей работе также методика аугментации позволила повысить предсказательную ценность модели до AUC: 0.8625, F1-мера: 0.8563. Без применения метода предобработки данных у модели LightGBM было AUC: 0.8625 F1-мера: 0.8563.
Выводы
В рамках нашего исследования были выявлены независимые предикторы окклюзии лучевой артерии (ОЛА), включающие пол, сахарный диабет 2 типа, курение, артериальную гипертензию, возраст, рост и вес пациента. Эти результаты представляют собой значимый вклад в клиническую практику, так как способствуют более точной идентификации пациентов с повышенным риском ОЛА, что, в свою очередь, позволяет оптимизировать выбор профилактических стратегий.
Особое внимание следует уделить потенциальной значимости открытой лучевой артерии в контексте повторных чрескожных коронарных вмешательств (ЧКВ), гемодиализных шунтов, инвазивного гемодинамического мониторинга и использования в качестве артериального шунта. Учитывая эти факторы, разработка и внедрение эффективных методов профилактики ОЛА приобретает критическое значение.
Таким образом, полученные результаты представляют собой важный шаг в направлении повышения эффективности профилактики и лечения ОЛА, что имеет важное значение для улучшения исходов медицинских вмешательств и повышения качества жизни пациентов.
Ограничения
Необходимо обратить внимание на некоторые ограничения данного исследования. Поскольку дизайн части исследования представляет собой ретроспективный реестр, а не рандомизированное исследование, нельзя исключить возможность предвзятого отбора. Наше исследование представляет собой опыт одного центра с ограниченным числом пациентов. В связи с этим, выводы, сделанные на основе данного исследования, могут не быть экстраполированы на более широкую популяцию без дополнительных подтверждений.
- Клинические рекомендации Стабильная ишемическая болезнь сердца. – 2020 (04.09.2020). – Утверждены Минздравом России.
- Valgimigli M., Gagnor A., Calabro P. et al. (2015) Radial versus femoral access in patients with acute coronary syndromes undergoing invasive management: a randomised multicentre trial. Lancet (London, England) 385: 2465–2476.
- Mitchell M.D., Hong J.A., Lee B.Y., Umscheid C.A., Bartsch S.M., Don C.W. Systematic review and cost-benefit analysis of radial artery access for coronary angiography and intervention. Circ Cardiovasc Qual Outcomes. 2012 Jul 1; 5(4): 454-62. DOI: 10.1161/CIRCOUTCOMES.112.965269. Epub 2012 Jun 26. PMID: 22740010; PMCID: PMC3430729.
- Ахрамович Р.В., Семитко С.П., Азаров А.В., Мельниченко И.С., Аналеев А.И., Чернышева И.Е., Третьяков А.А., Иоселиани Д.Г. Окклюзия радиальной артерии после первичного коронарного вмешательства при различных вариантах лучевого доступа. Патология кровообращения и кардиохирургия. 2020; 24(3S): 33–42. DOI: 10.21688/1681-3472-2020-3S-33-42.
- Ахрамович Р.В., Семитко С.П., Азаров А.В., Аналеев А.И., Мельниченко И.С., Чернышева И.Е., Третьяков А.А., Иосе- лиани Д.Г. Сравнительный анализ применения дорсопальмарного (модифицированного дистального) и трансрадиального доступов при первичных чрескожных коронарных вмешательствах у пациентов с острым коронарным синдромом. Альманах клинической медицины. 2022; 50. DOI: 10.18786/2072-0505-2022-50-034.
- Uhlemann M., Mobius-Winkler S., Mende M. et al. (2012) TheLeipzig prospective vascular ultrasound registry in radial artery catheterization: impact of sheath size on vascular complications. J Am Coll Cardiol Intv 5: 36–43.
- Огнерубов Д.В., Проваторов С.И., Меркулов Е.В., Терещен- ко А.С., Купина К.И., Погорелова О.А., Трипотень М.И., Балахонова Т.В., Кайралиев Д.М., Гроссман А.Э., Осокина А.К., Потехина А.В., Самко А.Н. Анализ ПРИчин развития Окклюзии лучевой артерии и способов ее предотвращения при использовании Радиального доступа для Интервенционных вмешательств. Результаты исследования АПРИОРИ. Российский кардиологический журнал. 2021; 26(12): 4695. DOI: 10.15829/1560-4071-2021-4695.
- Eid-Lidt G., Rivera Rodri’guez A., Jimenez Castellanos J., Farjat Pasos J.I., Estrada Lo’pez K.E., Gaspar J. Distal Radial Artery Approach to Prevent Radial Artery Occlusion Trial. JACC Cardiovasc Interv. 2021 Feb 22; 14(4): 378–385. DOI: 10.1016/j.jcin.2020.10.013.
- Bernat I., Aminian A., Pancholy S. et al. (2019) Best practices for the prevention of radial artery occlusion after transradial diagnostic angiography and intervention: an international consensus paper. J Am Coll Cardiol Intv 12: 2235–2246.
- Mitchell M.D., Hong J.A., Lee B.Y., Umscheid C.A., Bartsch S.M., Don C.W. Systematic review and cost-benefit analysis of radial artery access for coronary angiography and intervention. Circ Cardiovasc Qual Outcomes. 2012 Jul 1; 5(4): 454-62. doi: 10.1161/CIRCOUTCOMES.112.965269. Epub 2012 Jun 26. PMID: 22740010; PMCID: PMC3430729.
- Pancholy S.B., Bernat I., Bertrand O.F., Patel T.M. (2016) Prevention of radial artery occlusion after transradial catheterization: the PROPHET-II randomized trial. J Am Coll Cardiol Intv 9: 1992–1999.
- G.N. Hahalis, M. Leopoulou, G. Tsigkas, et al. Multicenter randomized evaluation of high versus standard heparin dose on incident radial arterial occlusion after transradial coronary angiography: the SPIRIT OF ARTEMIS study J Am Coll Cardiol Intv, 11 (2018), pp. 2241–2250.
- Applegate, M. Sacrinty, P. Schafer, J. Smith, S. Gandhi, M. Kutcher, et al. Cost effectiveness of radial access for diagnostic cardiac catheterization and coronary intervention Catheter Cardiovasc Interv, 82 (4) (2013), pp. E375-E384, 10.1002/ccd.24696.
- D.M. Safley, A.P. Amin, J.A. House, D. Baklanov, R. Mills, H. Giersiefen, et al.Comparison of costs between transradial and transfemoral percutaneous coronary intervention: a cohort analysis from the Premier research database American Heart Journal, 165 (2013), pp. 303–309.
- Coronary Artery Disease Detection Model Based on Class Balancing Methods and LightGBM Algorithm. May 2022. Electronics 11(9): 1495 DOI: 10.3390/electronics11091495.
