ЛЕКАРСТВЕННОЕ ОБЕСПЕЧЕНИЕ
Анализ фармацевтического рынка в рамках сегмента лекарственных препаратов для терапии педиатрических пациентов с Сovid-19
1 — Федеральное государственное бюджетное образовательное учреждение высшего образования «Рязанский государственный медицинский университет им. акад. И.П. Павлова» Министерства здравоохранения Российской Федерации, 390026, Российская Федерация, г. Рязань, ул. Высоковольтная, д. 9.
2 — Федеральное государственное бюджетное образовательное учреждение высшего образования «Санкт-Петербургский государственный химико-фармацевтический университет» Министерства здравоохранения Российской Федерации, 197022, Российская Федерация, г. Санкт-Петербург, ул. Профессора Попова, д. 14 лит. А.
3 — Федеральное государственное бюджетное образовательное учреждение высшего образования «Рязанский государственный медицинский университет им. акад. И.П. Павлова» Министерства здравоохранения Российской Федерации, 390026, Российская Федерация, г. Рязань, ул. Высоковольтная, д. 9.
Авторами проведен многовекторный анализ российского фармацевтического рынка в рамках сегмента препаратов для терапии педиатрических пациентов с COVID-19. Показано, что на национальном рынке в сегменте препаратов для терапии COVID-19 у педиатрических пациентов представлено 546 торговых наименований лекарственных препаратов. Доля позиций российского происхождения составляет 60,44%. Максимальной (65,46%) величиной в структуре ассортиментной матрицы характеризуется кластер противомикробных препаратов системного действия. Структуризация ассортимента по лекарственным формам демонстрирует преобладание (70,54%) позиций, применяемых парентерально. Анализ возрастных ограничений к применению препаратов у детей с COVID-19 в преломлении к современным этическим нормам фиксирует распространенную практику off-label-назначений. Анализ структуры зарегистрированных активных фармацевтических субстанций с идентификацией 87% импортируемых позиций демонстрирует значительную зависимость российской фарминдустрии от поставок сырья из зарубежных стран. Представленный ассортимент лекарственных препаратов достаточен для терапии неосложненного COVID-19 легкой и средней степени тяжести у детей. Социально значимыми векторами развития национального фармацевтического рынка в анализируемом сегменте является разработка российских препаратов из группы рекомбинантных моноклональных антител человека класса IgG1, а также организация полного цикла производства лекарственных препаратов. Риски клинического применения лекарственных препаратов у детей с COVID-19 обусловлены необходимостью соблюдения точности дозирования согласно возрасту пациента, приемлемостью для педиатрической практики с учетом специфики растущего и развивающегося организма, а также распространенной практикой off-label-назначений.
Ключевые слова: терапия педиатрических пациентов с COVID-19, лекарственные препараты для лечения детей с COVID-19, ассортиментная матрица препаратов для лечения COVID-19 у детей
Введение
На сегодняшний день неоспоримым представляется тот факт, что SARS-CoV-2 отличается от известных ранее представителей семейства Coronaviridae спецификой эпидемиологии, характером течения инфекционного процесса, а также особенностями проявления в детской популяции. Социально-экономическая значимость проблемы разработки эффективных способов локализации коронавируса с высокой вирулентностью, а также лимитирования ключевых звеньев патогенеза COVID-19 у детей обусловлена высокими показателями заболеваемости, а также вероятностью прогрессирования осложнений, развивающихся на фоне инфекционной патологии после перенесенного острого заболевания COVID-19 [1].
Современный уровень развития педиатрии предполагает выбор рациональной и всесторонне обоснованной в отношении ребенка медицинской технологии в соответствии с принципами доказательной медицины, базирующейся на использовании лекарственных препаратов с приемлемым профилем безопасности, а также клинической и клинико-экономической эффективностью в детской популяции1 [2].
Цель работы – провести анализ российского фармацевтического рынка в рамках сегмента препаратов для терапии педиатрических пациентов с COVID-19 для определения социально значимых направлений развития рынка в анализируемом сегменте.
Материал и методы
Материалами для исследования служили данные Государственного реестра лекарственных средств (ГРЛС) по состоянию на 01.12.2024 г. Для проектирования максимально корректного дизайна исследования сформирован информационный массив, характеризующий ассортиментную матрицу лекарственных препаратов для терапии педиатрических пациентов с COVID-19 в рамках национального фармацевтического рынка Российской Федерации. Оценка базы данных, включающей 546 позиций, в разрезе АТХ-классификации, а также инструкций по медицинскому применению лекарственных препаратов, клинических рекомендаций, ориентированных на педиатрическую практику, проводилась методом контент-анализа.
Группировку, ранжирование и систематизацию применяли в рамках анализа ассортиментной матрицы лекарственных препаратов. Графический анализ использован для визуализации данных. Обработка данных осуществлялась с использованием MS Excel 2021.
Результаты
Установлено, что клинический протокол лечения детей с коронавирусной инфекцией COVID-19 включает 38 международных непатентованных наименований (МНН) лекарственных препаратов [3]. В преломлении к контенту российских клинических рекомендаций обращает на себя внимание отсутствие на национальном рынке, а также в структуре сформированной матрицы отдельных позиций. Так, комбинации казиривимаб+имдевимаб, сотровимаб и бамланивимаб+этесевимаб, рекомендованные к применению у детей в качестве этиотропных средств, не имеют государственной регистрации и не включены в ГРЛС2. При этом стоит отметить, что 98,35% позиций присутствуют в перечне жизненно необходимых и важнейших лекарственных препаратов (ЖНВЛП)3.
Анализ ассортиментной матрицы препаратов для лечения COVID-19 у детей позволил установить, что в обращении на национальном рынке находится 546 торговых наименований из четырех фармакотерапевтических групп (табл. 1). Важно отметить, что максимальный удельный вес в структуре ассортимента составляют препараты, применяемые для патогенетической терапии детей с коронавирусной инфекцией (91,58%). Позиции, рекомендованные в качестве средств этиотропной терапии, охватывают лишь 8,42%.
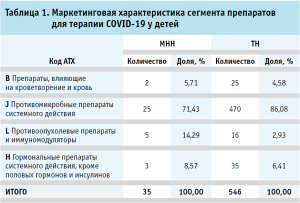
Результаты структурного анализа предложения в разрезе международных непатентованных наименований демонстрируют, что по количеству зарегистрированных препаратов лидируют цефтриаксон (10,07%), линезолид (8,97%), а также амоксициллин+клавулановая кислота (8,42%). Оценка ассортимента по локализации держателя регистрационного удостоверения позволяет констатировать значительное преобладание юридических лиц, зарегистрированных на территории Российской Федерации (72,71%). Выпуск российских препаратов обеспечивают 86 предприятий. Общее число держателей регистрационных удостоверений в сегменте препаратов, применяемых для терапии коронавирусной инфекции у педиатрических пациентов, составляет 182.
Показано, что 60,44% препаратов для терапии детей с коронавирусной инфекцией представлены российскими производителями, 39,56% – зарубежного происхождения (табл. 2). Структура импорта сформирована 32 странами-поставщиками. При этом семь стран предлагают 28% импортируемых позиций. Обращает на себя внимание то обстоятельство, что превалирующее число препаратов зарубежного происхождения производится в Индии (12,73%), Республике Беларусь (6,78%), Китае (3,47%), Австрии (1,98%), Италии (1,49%), Кипре (1,32%) и Португалии (1,16%). Вклад других стран-поставщиков составляет менее 1%. Среди производителей активных фармацевтических субстанций лидирующие позиции занимают Китай (43,90%), Индия (21,81%) и Россия (12,87%). Последнее указывает на выраженную зависимость российской фарминдустрии от поставок сырья из зарубежных стран.

Анализ ассортиментной матрицы лекарственных препаратов в рамках категорий позволяет утверждать, что в группе L «Противоопухолевые препараты и иммуномодуляторы» отсутствуют российские аналоги анакинры и канакинумаба, применяемые у детей из группы риска при тяжелой и крайне тяжелой степени заболевания. Следует отметить, что национальная фарминдустрия не выпускает позиции с противомикробной активностью на основе комбинации «цефтазидим+авибактам», а также цефтаролина фосфамила, применяемых в педиатрической практике при жизнеугрожающих состояниях у детей, включая потенциальную вероятность развития инфекции, вызванной синегнойной палочкой, а также в условиях развития пневмонии различной этиологии при наличии факторов риска [1,3].
Стоит подчеркнуть, что возможность применения препарата в детской практике в значительной степени определяется возрастом пациентов (рис. 1). В свете данных рассуждений обращает на себя внимание ограничение числа позиций для применения на ранних периодах развития организма.
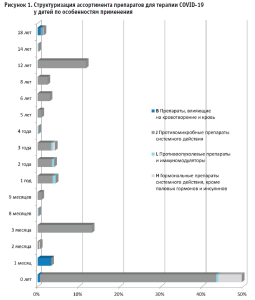
Результаты контент-анализа демонстрируют, что восемь препаратов (1,46%) с ремдесивиром, иммуноглобулином человека нормальным, а также далтепарином натрия разрешены к применению у пациентов с 18 лет, что, в свою очередь, формирует практику off-label-назначений в педиатрии во всех возрастных группах.
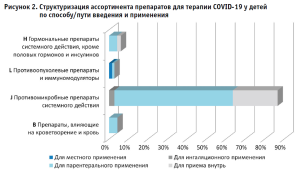
Сравнительная оценка вклада способа/пути введения и применения в общую структуру ассортимента лекарственных препаратов для терапии COVID-19 у детей указывает на тот факт, что наибольший удельный вес имеют парентеральные формы (70,54%). Стоит отметить, что категория B «Препараты, влияющие на кроветворение и кровь» включает в себя только инъекционные лекарственные формы. Препараты для местного применения (1,56%) присутствуют только в категории L «Противоопухолевые препараты и иммуномодуляторы», а препараты с ингаляционным путем введения (2,77%) характерны для позиций группы J «Противомикробные препараты системного действия». Лекарственные препараты для внутреннего применения составляют 25,13% структуры ассортимента (рис. 2).
В результате систематизации полученных данных построен макроконтур российского фармацевтического рынка в рамках сегмента лекарственных препаратов для терапии педиатрических пациентов с COVID-19 (рис. 3).
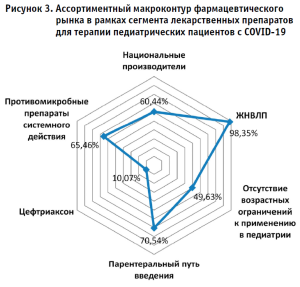
Основные параметры ассортимента демонстрируют, что формирование рынка осуществляется преимущественно (60,44%) российскими компаниями-производителями. При этом макроконтур регистрирует превалирование препаратов категории J «Противомикробные препараты системного действия» (65,46%), среди которых в структуре предложения лидирует цефтриаксон (10,07%). Наиболее широко представлены лекарственные препараты с парентеральным путем введения, охватывающие 70,54% предложения, что, в свою очередь, подчеркивает актуальность изменения вектора традиционных фармацевтических разработок в сторону формирования номенклатуры целевых для педиатрии лекарственных препаратов, в т.ч. в виде пероральных корригированных форм. Важно подчеркнуть, что 49,63% позиций разрешены к применению в педиатрии во всех возрастных группах, 98,35% препаратов для терапии коронавирусной инфекции у детей входят в перечень ЖНВЛП.
Заключение
Полученные результаты дают основания полагать, что представленный ассортимент лекарственных препаратов достаточен для терапии неосложненного COVID-19 легкой и средней степени тяжести у детей. Социально значимыми векторами развития национального фармацевтического рынка в анализируемом сегменте является разработка российских препаратов из группы рекомбинантных моноклональных антител человека класса IgG1, ориентированных на этиотропную терапию коронавирусной инфекции в условиях тяжелой и критической степени тяжести заболевания, а также организация полного цикла производства лекарственных препаратов. Риски клинического применения лекарственных препаратов у детей с COVID-19 обусловлены необходимостью соблюдения точности дозирования согласно возрасту пациента, приемлемостью для педиатрической практики с учетом специфики растущего и развивающегося организма, а также распространенной практикой off-label-назначений.
_______________________________________________________________________
1 Рекомендация Коллегии Евразийской экономической комиссии от 21.12.2021 № 30 «О Руководстве по фармацевтической разработке лекарственных средств для применения в педиатрической практике». Доступно по: https://www.consultant.ru/document/cons_doc_LAW_404523/ Ссылка активна на 01.12.2024.
2 Государственный реестр лекарственных средств. – URL: https://grls.rosminzdrav.ru/GRLS.aspx/ (дата обращения: 01.12.2024).
3 Распоряжение Правительства РФ от 12.10.2019 N 2406-р (ред. от 16.04.2024) «Об утверждении перечня жизненно необходимых и важнейших лекарственных препаратов, а также перечней лекарственных препаратов для медицинского применения и минимального ассортимента лекарственных препаратов, необходимых для оказания медицинской помощи». URL: https://www.consultant.ru/document/cons_doc_LAW_335635/ (дата обращения: 01.12.2024).
- Principles of Rational COVID-19 Therapy in Pediatrics / O. D. Nemyatykh, M. A. Maistrenko, D. D. Demchenko [et al.] // Journal of Clinical Medicine. – 2023. – Vol. 12, No. 14. – P. 4731. – DOI 10.3390/jcm12144731. – EDN CMKWJK.
- Немятых, О.Д. Перспективы оптимизации лекарственного обеспечения педиатрических пациентов на основе развития фармацевтического рынка в сегменте лекарственных препаратов для детей / О. Д. Немятых, Е. А. Ковалева, И. А. Наркевич // Разработка и регистрация лекарственных средств. – 2024. – Т. 13, № 4. – С. 272–283. – DOI 10.33380/2305-2066-2024-13-4-1839. – EDN GKYMKV.
- Клинический протокол лечения детей с новой коронавирусной инфекцией (COVID-19), находящихся на стационарном лечении в медицинских организациях государственной системы здравоохранения города Москвы / Османов И.М., Алексеева Е.И., Мазанкова Л.Н., Захарова И.Н. [и др.]; Под редакцией А.И. Хрипуна. – М.: ГБУ «НИИОЗММ ДЗМ», 2021. – 92 с.
